
16. 0.1mol/LNaOH溶液和0.1mol/LNH4Cl溶液等体积混合后,溶液中离子浓度大小顺序正确的是
A.c(Na+)>c(Cl-)>c(OH-)>c(H+) B.c(Na+)=c(Cl-)>c(H+)>c(OH-)
C.c(Cl-)>c(Na+)>c(OH-)>c(H+) D.c(Na+)=c(Cl-)>c(OH-)>c(H+)
15. 现有浓度为1 mol/L的五种溶液:①HCl,②H2SO4,③CH3COOH,④NH4Cl,⑤NaOH,由水电离出的C(H+)大小关系正确的是
A.④>③>①=⑤>② B.①=②>③>④>⑤
C.②>①>③>④>⑤ D.④>③>①>⑤>②
14. pH相同的氨水、NaOH和Ba(OH)2溶液,分别用蒸馏水稀释到原来的X、Y、Z倍,稀释后三种溶液的pH仍然相同,则X、Y、Z的关系是
A. X=Y=Z B. X<Y=Z C. X>Y=Z D.X=Y<Z
13. 下列事实一定能说明HF是弱酸的是
①常温下NaF溶液的pH大于7; ②用HF溶液做导电性实验,灯泡很暗;
③HF与NaCl不能发生反应; ④常温下0.1mol/L的HF溶液的pH为2.3
⑤HF能与Na2CO3溶液反应,产生CO2气体 ⑥HF与水能以任意比混溶
⑦1mol/L的HF水溶液能使紫色石蕊试液变红
A.①②⑦ B.②③⑤ C.③④⑥ D.①④
12. 下列方程式书写正确的是
A. H2S的电离方程式H2S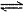 2H++S2-
2H++S2-
B. HCO3-在水溶液中的电离方程式:HCO3-+H2O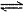 H3O++CO32-
H3O++CO32-
C.CO32-的水解方程式:CO32-+2H2O H2CO3+2OH-
H2CO3+2OH-
D. NaHSO4在水溶液中的电离方程式:NaHSO4 Na++H++SO42一
Na++H++SO42一
11. pH=13的强碱与pH=2的强酸溶液混合,所得混合液的pH=11,则强碱与强酸的体积比为
A.1:9 B.9:1 C.1:11 D.11:1
10. 下列溶液一定呈中性的是
A.pH=7的溶液 B.使石蕊试液呈紫色的溶液
C.c(H+)=c(OH-)=10-6mol/L溶液 D.酸与碱恰好完全反应生成正盐的溶液
9. 下列实验操作中正确的是
A.用托盘天平称取3.25gNaCl
B.测定未知NaOH溶液浓度时,酸式滴定管需用标准酸液润洗2-3次
C.用量筒量取10.51mL盐酸
D.先将pH试纸用蒸馏水润湿后,再测定溶液的pH
8. 相同温度下,物质的量浓度均为1mo /L的盐酸、硫酸和醋酸,导电能力由强到弱的顺序是
/L的盐酸、硫酸和醋酸,导电能力由强到弱的顺序是
A.盐酸=硫酸=醋酸 B.盐酸>硫酸>醋酸
C.硫酸>盐酸>醋酸 D.醋酸>盐酸>硫酸
7. 在一个盛有20mL0.1mol/LNaOH溶液和10mLH2O的容器中, 逐滴加入0.1mol/LHCl溶液, 当容器中的碱溶液恰好被加入的酸溶液中和时,容器内溶液的总体积约是
A .40mL B. 50mL C. 60mL D. 70mL
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com