
15.下列实验不能先用蒸馏水润湿试纸的是
( )
A.用品红试纸检验SO2
B.用淀粉碘化钾试纸检验Cl2
C.用红色石蕊纸检验NH3
D.用pH试纸测定某溶液的pH值
14.根据以下事实得出的判断一定正确的是
( )
A.HA的酸性比HB的强,则HA溶液的 pH一定比HB溶液的小
B.A+和B-的电子层结构相同,则A原子的核电荷数比B原子的大
C.同温下 ,A盐溶解度比B盐大,则A盐溶液的物质的量浓度比B盐溶液的大
D.A原子失去的电子比B原子的多,则A单质的还原性比B单质的强
13.在标准状况下,进行甲、乙、丙三组实验:三组各取60mL 同浓度盐酸溶液,加入同一种镁铝合金粉末,产生气体,有关数据列表如下: 
|
实验序号 |
甲 |
乙 |
丙 |
|
合金质量/mg |
510 |
770 |
918 |
|
气体体积/mL |
560 |
672 |
672 |
则下列说法正确的是
( )
A.甲组和乙组的实验中,盐酸均是过量的 
B.盐酸的物质的量浓度为0.8 mol·L―1 
C.合金中镁铝的物质的量之比为1∶1 
D.丙组中铝的物质的量为0.009 mol
12.如下图所示的装置,C、D、E、F、X、Y都是惰性电极。将电源接通后,向(乙)中滴入酚酞溶液,在E极附近显红色。则以下说法不正确的是
(
)

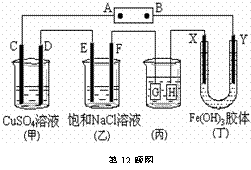





A.电源B极是正极
B.(甲)、(乙)装置的C、D、E、F电极均有单质生成,其物质的量比为1∶2∶2∶2
C.欲用(丙)装置给铜镀银,H应该是Ag,电镀液选择AgNO3溶液
D.装置(丁)中Y极附近红褐色变浅,说明氢氧化铁胶粒带正电荷
11.将0.4mol·L-1 HCN溶液和0.2 mol·L-1的NaOH溶液等体积混合后,溶液pH
>7,下列关系中正确的是
(
)
A.c(HCN)<c(CN-) B.c(Na+)<c(CN-)
C.c(HCN)-c(CN-)=c(OH-) D.c(HCN)+
c(CN-)=0.2 mol·L-1
10.在某稀溶液中含有0.2mol HNO3和x mol H2SO4,向其中加入19.2g 铜粉,充分反应后产生的气体在标准状况下的体积为4.48L,则x值至少为
( )
A.0.6 B.0.4 C.0.3 D.0.2
9.下列制取硫酸铜的实验设计能体现“经济、高效、环保”精神的是
( )
A.铜与浓硫酸共热 
B.用铜片为阳极,石墨为阴极,电解稀硫酸
C.先灼烧废铜屑生成氧化铜,然后再用浓硫酸溶解
D.适当温度下,使铜片在持续通入空气的稀硫酸中溶解
8. 下列离子反应方程式正确的是
( )
A.用两个铜电极电解饱和食盐水:2Cl-+2H2O  2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
B.实验室用浓盐酸与MnO2反应制Cl2:MnO2+2H++2Cl- 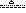 Cl2↑+ Mn2+ + H2O
Cl2↑+ Mn2+ + H2O
C.NH4HCO3溶液中加入少量NaOH溶液:HCO3-
+ OH-
= CO32-
+ H2O
D.Ca(HCO3)2溶液中加入足量KOH溶液:Ca2+ + HCO3-+OH-= CaCO3↓+H2O
7.向含Fe3+、Fe2+、Mg2+、NH4+的水溶液中,加入足量的Na2O2固体,充分反应后再加入过量的稀盐酸,上述离子数目没有明显变化的是
( )
A.Fe2+ B.Mg2+ C.Fe3+ D.NH4+
6.50g浓度为C mol•L-1,密度为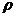 g•cm-3的硫酸中加入一定量的水稀释成0.5C mol•L-1,
g•cm-3的硫酸中加入一定量的水稀释成0.5C mol•L-1,
则加入水的体积为
( )
A.小于50mL B.等于50 mL C.大于50
mL D.等于50/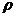 mL
mL
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com