
2ЎўФЪMgЎўMgOЎўMg(OH)2ЎўH2SO4әНCuSO4ИЬТәЦРЈ¬ДЬЙъіЙMgSO4өД·Ҫ·ЁУР(ЎЎЎЎ )
A. 3ЦЦЎЎЎЎЎЎ ЎЎЎЎЎЎЎЎ ЎЎB. 4ЦЦЎЎЎЎЎЎ ЎЎЎЎЎЎ ЎЎЎЎC. 5ЦЦЎЎЎЎЎЎЎЎЎЎ ЎЎЎЎ D. 6ЦЦ
1ЎўіЈОВПВЈ¬Ді·ҙУҰM + N ЎъЎЎ СО + Л®Ј¬ЖдЦРMЎўNөДАаұрІ»ҝЙДЬКЗ ЎЎ(ЎЎ )
ЎЎ A. ЛбЎўјоЎЎЎЎЎЎ B.өҘЦКЎўСх»ҜОпЎЎ C.Сх»ҜОпЎўЛбЎЎЎЎ D.Сх»ҜОпЎўјо
(¶ю)ёҙ·ЦҪв·ҙУҰ·ўЙъәННкіЙөДМхјю
іхЦР»ҜС§ЦРЛщЙжј°өҪөДёҙ·ЦҪв·ҙУҰЈ¬ЦчТӘКЗЛбЎўјоЎўСОөИ»ҜәПОпФЪИЬТәЦР·ўЙъөД·ҙУҰЈ¬ХвАа·ҙУҰөДКөЦККЗ»ҜәПОпАлҪвЙъіЙөДАлЧУФЪИЬТәЦРПа»ҘЦ®јд·ўЙъБЛ·ҙУҰЎЈөұБҪЦЦОпЦКФЪИЬТәЦР»ҘПаҪ»»»АлЧУКұЈ¬ТхСфАлЧУҪбәПЙъіЙДСөзАлөДОпЦКЈ¬ИзіБөнЎўЖшМеЎў»тЛ®өИЈ¬ҫН»бКЗИЬТәЦРөДХвР©АлЧУГчПФјхЙЩЈ¬·ҙУҰҫНПтЧЕДСөзАлөДОпЦК--іБөнЎўЖшМеЎў»тЛ®өД·ҪПтҪшРРЎЈ
Хл¶ФЙПКцЗйҝцЈ¬ОТГЗҝЙТФҪ«іхЦРҪЧ¶ОЛщЙжј°өҪөДёҙ·ЦҪв·ҙУҰ·ўЙъәННкіЙөДМхјю№йДЙОӘПВБРБҪҫд»°Јә
·ўЙъМхјюЈәОЮЛбІОјУЈ¬јоСОТӘИЬ
НкіЙМхјюЈәЙъіЙЎь(ЖшМе)ЎўЎэ(іБөн)»тЛ®ЎЈ
ОКМвМҪҫҝ
ОКМв1ЎЎ ёҙ·ЦҪв·ҙУҰІ»ДЬЙъіЙөДОпЦККЗЎЎЎЎЎЎЎЎЎЎ ЎЈ
ўЩ өҘЦКЎЎ ўЪ Сх»ҜОпЎЎ ўЫ ЛбЎЎ ўЬ јоЎЎ ўЭ СО
AЎўўЩўЪЎЎЎЎЎЎ BЎўўЪўЬЎЎЎЎЎЎ CЎўўЫўЭЎЎЎЎЎЎЎЎ DЎўўЩ
[·ЦОц]ёҙ·ЦҪв·ҙУҰөДЙъіЙОпЈ¬ёщҫЭ№ШПөНјҪв¶БҝЙЦӘЈ¬ҝЙТФКЗСОәНЛ®ЎўЛбәНСОЎўјоәНСОЎўСОәНСОЈ¬ЖдЦРТЧ·ЦҪвөДЛбУЦЙъіЙСх»ҜОпәНЛ®Ј¬ИзH2CO3Ј¬ҝЙ·ЦҪвіЙCO2әНH2OЎЈ
[ҙр°ё] D
ОКМв2ПВБРёчј¶ОпЦКЈ¬ДЬФЪЛбРФИЬТәЦРИЛБҝ№ІҙжЈ¬ЗТИЬТәКЗОЮЙ«ЎўНёГчөДКЗ(ЎЎЎЎ )
A.Na2C03Ј¬MgS04Ј¬NaCIЎўK2S04ЎЎ B.CuS04Ўў KCIЎўNaN03Ўў CaCl2
[·ЦОц]ҪвҙрұҫМвКұУҰМШұрЧўТвМвЦРөДёҪјУМхјюЎ°ЛбРФИЬТәЎұәНЎ°ОЮЙ«ЎўНёГчИЬТәЎұЎЈAЦРNa2C03І»ДЬФЪЛбРФ»·ҫіЦРҙжФЪ№КЕЕіэЈәBЦРCuS04ОӘА¶Й«Ј¬№КBҙнОуЈ»CЦРNa2S04әНBaCl2ҝЙ·ўЙъёҙ·ЦҪв·ҙУҰЈ¬јҙІ»ДЬҙуБҝ№ІҙжЈ¬№КCІ»Ц№И·ЎЈ
[ҙр°ё] D
ОКМв3ИзәОЦӨГчДі»Ҝ·КСщЖ·ОӘБтп§?УГ»ҜС§·ҪіМКҪұнКҫЎЈ
[·ЦОц]Бтп§јҙБтЛбп§Ј¬ЛьөД»ҜС§КҪОӘ(NH4)2S04Ј¬УЙNH4+әНSO2- 4№№іЙЈ¬Тт¶шРиУГ»ҜС§·Ҫ·Ё·Цұр»тН¬КұЦӨГчБҪЦЦАлЧУөДҙжФЪЎЈ
[ҙр°ё]УРБҪЦЦ·Ҫ·ЁЈәўЩјУБҪЦЦКФјБЈәCa(OH)2әНBaCl2
(NH4)2SO4+Ca(OH)2=CaS04+2NH3 1+2H20
(NH4)2S04+BaCl2=BaS04+2NH4C1
ўЪУГТ»ЦЦКФјБЈ»Ba(OH)2
(NH4)2S04+Ba(OH)2=BaS04Ўэ+2NH3Ўь+2H20
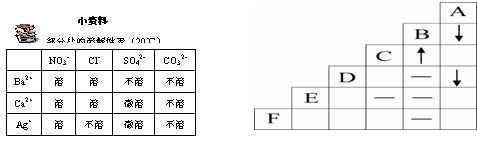
ОКМв4УРAЎўBЎўCЎўDЎўEЎўFБщЦЦОпЦКөДПЎИЬТәЈ¬ТСЦӘЛьГЗ·ЦұрКЗK2CO3ЎўBaCl2ЎўCa(NO3)2ЎўNaClЎўH2SO4ЎўAgNO3ЦРөДДіТ»ЦЦИЬТәЎЈПВНјОӘіЈОВКұЙПКцИЬТәБҪБҪ»мәПөДІҝ·ЦКөСйПЦПуЈ¬ЖдЦРЎ°ЎэЎұұнКҫЙъіЙіБөнЈ¬Ў°ЎьЎұұнКҫЙъіЙЖшМеЈ¬Ў°ЈӯЎұ ұнКҫОЮГчПФПЦПу»тЙъіЙОўИЬОпЎЈЗл»ШҙрПВБРОКМвЈә
(1)ФЪПВНјЦРөДҝХёсДЪУГЎ°ЎэЎұЎ°ЎьЎұЎ°ЈӯЎұұнКҫіц¶ФУҰ·ҙУҰөДКөСйПЦПуЎЈ
(2)FКЗЎЎЎЎЎЎЎЎЎЎЎЎ ЎЈ
 ЎЎ
ЎЎ
[·ЦОц]ёщҫЭЧуНјЦРөД·ҙУҰПЦПуҫЎҝЙДЬөДНЖ¶ПіцёчОпЦКЈәУЙУЪЖдЦРМхјюЧоЧгөДКЗBОпЦКЈ¬ёщҫЭЛьУлЖдЛьОпЦК·ҙУҰөДПЦПуЈ¬ҝЙНЖІвКЗH2SO4ЎЈУЙҙЛЈ¬УлB·ҙУҰЙъіЙЖшМеөДCКЗK2CO3Ј¬УлB·ҙУҰЙъіЙіБөнөДAКЗBaCl2ЎЈКЈПВөДОпЦКЦРУлA·ҙУҰЙъіЙіБөнөДDОпЦКТтёГКЗAgNO3ЎЈФЩёщҫЭКЈПВөДNaClәНCa(NO3)2ЦРУлCОпЦК»мәПГ»УРПЦПуөДКЗNaClЈ¬ТтҙЛEКЗNaClЈ¬ДЗГҙFКЗCa(NO3)2ЎЈёщҫЭНЖ¶ПіцөДОпЦКәНРЎЧКБПЈ¬ФЪҝХёсЦРұкіцЖдЛьОпЦКјдПа»Ҙ·ҙУҰөДПЦПуЎЈ
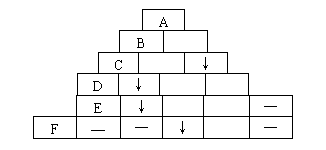 [ҙр°ё](1)ИзУТНјЛщКҫЈә
[ҙр°ё](1)ИзУТНјЛщКҫЈә
(2)ПхЛбёЖ[»тCa(NO3)2]
С§ТФЦВУГ
(Т»)ЎўЦШТӘ·ҙУҰ№жВЙ
1ЎўІҝ·ЦЛбРФСх»ҜОп + Л®ЎъЎЎ ә¬СхЛб
CO2 + H2O =====H2CO3
2ЎўІҝ·ЦјоРФСх»ҜОп+Л®Ўъ јоИЬТә
CaO + H2O =====Ca(OH)2
3ЎўЛбРФСх»ҜОп+јоИЬТә Ўъ СО + Л®
CO2 +Ca(OH)2====CaCO3Ўэ+ H2O
4Ўў јоРФСх»ҜОп + Лб Ўъ СО + Л®ЎЎ
ЎЎ CaOЎЎ + 2HCl ====CaCl2 + H2OЎЎ
5Ўў јо + Лб ЎъЎЎ СО + Л®ЎЎЎЎ
ЎЎЎЎ NaOH + HCl ==== NaCl+ H2OЎЎ
6ЎўСО + ЛбЎЎ ЎъЎЎ РВСО + РВЛб
ЎЎЎЎ AgNO3 + HCl ===ЎЎ AgCl Ўэ+ H NO3
7ЎўСОИЬТә + јоИЬТә Ўъ РВСО + РВјо
ЎЎЎЎ CuCl2 +2NaOH ===== 2NaCl + Cu(OH)2Ўэ
8ЎўСОИЬТә + СОИЬТәЎЎЎЎЎЎ РВСО + РВСО
ЎЎ Na2CO3ЎЎ + CaCl2ЎЎ =====ЎЎ CaCO3Ўэ + 2 NaClЎЎ
ЧўЈәЙПКц4~8ОеАа·ҙУҰКфёҙ·ЦҪв·ҙУҰЎЈ
ПЦҪ«ЙПНјЦРБҪЧЭРРЎ°ЛбРФСх»ҜОп-Лб-СОЎұЎўЎ°јоРФСх»ҜОп-јо-СОЎұЛщО§ИЖөДЗшУтДЪЈ¬°ьә¬өДЦШТӘ»ҜС§·ҙУҰҪв¶БИзПВЈә
3ЎўХвёц№ШПөНјУРКІГҙУГНҫЈҝ
2ЎўДгДЬҝҙіцЖдЦРөДЎ°°ВГоЎұВрЈҝ
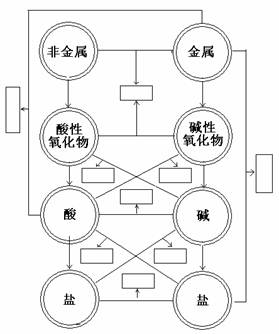 ПВНјКЗТ»ЦЦҫӯөдөДГиКцөҘЦКЎўСх»ҜОпЎўЛбЎўјоәНСОПа»Ҙ№ШПөөД№ШПөНјЎЈЛь°ьә¬ЧЕәЬ·бё»өДДЪИЭЎЈЗлЛјҝјПВБРОКМвЈә
ПВНјКЗТ»ЦЦҫӯөдөДГиКцөҘЦКЎўСх»ҜОпЎўЛбЎўјоәНСОПа»Ҙ№ШПөөД№ШПөНјЎЈЛь°ьә¬ЧЕәЬ·бё»өДДЪИЭЎЈЗлЛјҝјПВБРОКМвЈә
1Ўў·ҪҝтДЪУҰМоИлДЗТ»АаОпЦКЈҝ
15Ўў(1)УГТ»ҫд»°ёЕАЁТФЙПДЪИЭ(І»і¬№э10ёцЧЦ)(2·Ц)
ЎЎ (2)(5·Ц)ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com