
18.某学生用NaHCO3和KHCO3组成的某混合物进行实验,测得如下数据(盐酸的物质的量浓度相等),下列分析推理不正确的是( )
|
|
50mL盐酸 |
50mL盐酸 |
50mL盐酸 |
|
m(混合物) |
9.2g |
27.6g |
36.8g |
|
Vco2标况 |
2.24L |
3.36L |
3.36L |
A.盐酸的物质的量浓度为 3.0mol/L
B.根据表中数据不能计算出混合物中NaHCO3的质量分数
C.加入混合物9.2g时盐酸过量
D.27.6g混合物与盐酸反应时混合物过量
17.使H2在600mLO2和Cl2的混合气体中充分燃烧,待O2和Cl2耗尽后,用水吸收反应生成物,得200mL溶液,取出20mL溶液恰好与20mL 0.125mol/LNaOH溶液恰好中和则与原混合气体反应的H2的体积为( )
A.280mL B.600 mL C.920 mL D.1200 mL
16、防治禽流感时需大量使用过氧乙酸,含氯类消毒剂,氯氨是长效缓释有机氯消毒剂,其制备反应为NH3+HClO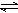 H2O+NH2Cl,下列有关氯氨(NH2Cl)的说法不正确的是( )
H2O+NH2Cl,下列有关氯氨(NH2Cl)的说法不正确的是( )
A.氯氨的消毒原理与漂白粉相似
B.氯氨在水中水解的最初产物是NH2OH(羟氨)和HCl
C.氯氨与浓盐酸混合后可产生Cl2
D.氯氨的电子式为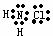
15. 已知:2CO(g)+O2(g)=2CO2(g) ΔH=-566
kJ/mol
已知:2CO(g)+O2(g)=2CO2(g) ΔH=-566
kJ/mol
Na2O2(s)+CO2(g)=Na2CO3(s)+
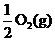 ΔH=-226 kJ/mol
ΔH=-226 kJ/mol
根据以上热化学方程式判断,下列说法正确的是( )
A.CO的燃烧热为283 kJ
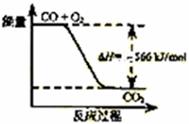
B.右图可表示由CO生成CO2的反应过程和能量关系
C.2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g) ΔH>-452 kJ/mol
D.CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为6.02×1023
14.气体X可能含有Cl2、HBr、CO2中的一种或几种,若将X通入AgNO3溶液,产生淡黄色沉淀,该沉淀不溶于稀硝酸,若将X通入澄清石灰水,不见沉淀生成,有关气体X正确说法是( )
A.一定含HBr,可能含Cl2和CO2 B.一定含HBr,一定不含Cl2和CO2
C. 一定含Cl2,CO2,可能含HBr D. 可能含CO2,一定不含Cl2,一定含HBr
13. 下列离子方程式与所述事实相符且正确的是( )
A、 Fe(OH)3溶于氢碘酸:Fe(OH)3 + 3H+ = Fe3+ + 3H2O
B.向Na2S2O3溶液中通入足量氯气:S2O32-+2Cl2+3H2O=2SO32-+4Cl-+6H+
C..向漂白粉溶液通入过量CO2: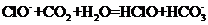
D.在强碱溶液中次氯酸钠与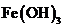 反应生成
反应生成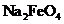 :
:
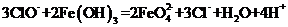
12.对于①ag纯净的Na2CO3;②ag Na2CO3和NaHCO3混合物,下列各种情况的描述正确的是( )
A. 分别与足量盐酸反应时,②放出的CO2多 B.分别与盐酸反应时,②消耗盐酸多
C.分别配成等体积的溶液,②的pH大 D.分别配成等体积的溶液,②的c(Na+)大
11.在下列给定条件的溶液中,一定能大量共存的一组离子是( )
A.无色溶液:Na+、K+、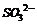 、ClO-
、ClO-
B.能使pH试纸呈红色的溶液:Na+、NH+4、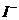 、
、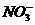
C.FeCl2溶液:K+、、Na+、、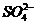 、、
、、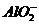
D.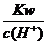 =0.1 mol/L的溶液:Na+、K+、
=0.1 mol/L的溶液:Na+、K+、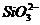 、
、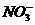
10.在一密闭容器中有HCHO、H2、O2的混合气体20g和足量Na2O2,用电火花引燃,使其完全反应,Na2O2增重8g,下列说法不正确的是( )
A.残留固体的成份为Na2O2、NaOH、Na2CO3
B.残留气体只有O2
C.原混合气体中氧元素的质量分数为60%
D.原混合气体中HCHO的质量一定小于8g
9.下列叙述正确的是(用NA代表阿伏加德罗常数的值) ( )
A. 1molHCl气体中的粒子数与0.5 mo1/L盐酸中溶质粒子数相等
B.78gNa2O2固体中,离子总数为3NA
C.1molCl2发生化学反应时,转移的电子数必为2 NA
D.CO和N2为等电子体,22.4L的CO气体与1mol N2所含的电子数相等
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com