
59、(6分)在开展研究性学习活动中,某研究小组的同学设计了如下实验装置,用来制取乙烯并探究乙烯和溴水的反应情况。
[实验目的]研究乙烯能否跟溴水发生反应。
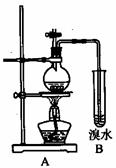 [实验过程]
[实验过程]
①装配好装置,检查装置的气密性;
②加入所需药品,迅速将浓硫酸和乙醇的混合液的温度升高到170℃;
③观察盛溴水的试管内溶液颜色的变化。
[实验原理、现象]
A装置中制取乙烯的化学方程式为 ▲ ;实验过程中,B装置中观察到的实验现象是 ▲ 。
[实验结果、讨论]
根据B中观察到的实验现象,同学们得出了乙烯能跟溴水发生反应的结论,但有的同学认为发生了加成反应,有的同学认为发生了取代反应。为验证该反应是加成反应而不是取代反应,某同学提出可用pH试纸测试反应前后溶液的酸性变化,理由是 ▲ 。
58、(6分)请按要求填空
(1)检验KCl溶液中是否含有SO42-离子,加入的试剂为 ▲ 。
(2)除去NaCl固体中混有的少量KNO3,所进行的实验操作依次为: ▲ 、蒸发、结晶、过滤。
(3)用已准确称量的1.06gNa2CO3固体配制0.10mol·L-1Na2CO3溶液100mL,所需要的仪器除烧杯、量筒、玻璃棒和胶头滴管外,还需要的仪器为 ▲ 。
57、(4分)汽车尾气主要含有CO2、CO、SO2、NO及汽油、柴油等物质,这种尾气越来越成为城市空气污染的主要来源,必须予以治理。治理的方法之一是在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂)。它的特点是使CO与NO反应,生成可参与大气生态环境循环的无毒气体,并促使汽油、柴油等物质充分燃烧及SO2的转化。
(1)汽油尾气中NO的来源 ▲ 。
A、汽油、柴油中含氮,是其燃烧产物
B、是空气中的N2与汽油、柴油的反应产物
C、是空气中的N2与O2在汽车汽缸内的高温放电环境下的反应产物
D、是汽车排出的高温尾气导致了空气中N2与O2发生化合反应
(2)写出CO与NO反应的化学方程式 ▲ 。
(3)“催化转换器”的缺点是在一定程度上提高了空气的酸度,其原因 ▲ 。
(4)控制或者减少城市汽车尾气污染的方法可以有 ▲ 。(多选)
A、开发氢能源 B、使用电动车 C、戴上呼吸面具 D、限制汽车数量
56、(6分)[本题包括2小题,每位同学只需选做一小题。若两题都做,按第(1)小题计分]
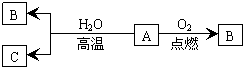 (1)已知A是应用最广泛、用量最大的一种金属单质,B是黑色固体,C是气体单质,在一定条件下有如右图转化关系:
(1)已知A是应用最广泛、用量最大的一种金属单质,B是黑色固体,C是气体单质,在一定条件下有如右图转化关系:
写出A、B、C各物质的化学式:A ▲ ,B ▲ ,C ▲ 。
(2)已知A是淀粉在一定条件下水解生成的最终产物,现有下列转化关系:

写出A的分子式 ▲ ,B的结构简式 ▲ ,C的结构简式 ▲ 。
55、(4分)(1)写出锌跟浓硫酸反应可生成SO2和H2的化学方程式: ▲ 。
(2)写出苯的硝化反应的方程式: ▲ 。
54、互为同分异构体,且可用银镜反应区别的是
A、淀粉和纤维素 B、蔗糖和麦芽糖 C、葡萄糖和蔗糖 D、葡萄糖和麦芽糖
试 卷 Ⅱ
请将本卷的答案用钢笔或圆珠笔写在答卷Ⅱ上。
53、下列各组混合物中,能用分液漏斗分离的是
A、乙醇和水 B、苯和苯酚
C、乙醛和乙酸 D、乙酸乙酯和饱和碳酸钠溶液
52、关于丙烯醛(CH2=CH-CHO)的叙述不正确的是
A、可使溴水和酸性高锰酸钾溶液褪色 B、与足量的氢气加成生成丙醛
C、能发生银镜反应 D、在一定条件下可氧化成酸
51、-CH3、-OH、-COOH和-C6H5四种基团中的不同基团两两组合,所形成的有机物中,具有酸性的物质有
A、1种 B、2种 C、3种 D、4种
50、将一定量的某醇等分成两份,取一份完全燃烧可生成0.2mol二氧化碳,另一份与足量的金属钠反应生成0.1mol氢气,则该醇可能是
A、甲醇 B、乙醇 C、丙二醇 D、丙醇
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com