
24£Æ(9∑÷)
°°°°°° ∂Ã÷Ð∆⁄‘™Àÿº◊°¢““°¢±˚°¢∂°°¢ŒÏ‘⁄‘™Àÿ÷Ð∆⁄±Ì÷–µƒŒª÷√»Á”“±ÌÀ˘ 棨∆‰÷–∂°À˘¥¶µƒ÷˜◊Â–Ú ˝ «∆‰÷Ð∆⁄–Ú ˝µƒ»˝±∂£¨ªÿ¥œ¬¡–Œ £∫
°°°°°° (1)º◊‘⁄‘™Àÿ÷Ð∆⁄±Ì÷–µƒŒª÷√°°°°°°°°°°°°°°°° °£
°°°°°° (2)‘≠◊”∞Îæ∂£∫º◊°°°°°° ∂°(ÃÓ°∞>°±ªÚ°∞<°±)°£
°°°°°° (3)““”ÎŒÏ◊È≥…ªØ∫œŒÔµƒµÁ◊” Ω «°°°°°°°° £¨∆‰÷–ªØ—ߺ¸µƒ¿ý–Õ «°°°°°°°°°°°°°°°°
(ÃÓ°∞º´–‘°±ªÚ°∞∑«º´–‘°±)π≤º€º¸°£
°°°°°° (4)‘™Àÿµƒ∑«Ω Ù–‘£∫º◊°°°° ±˚(ÃÓ°∞>°±ªÚ°∞<°±)£¨œ¬¡– ¬ µƒÐÀµ√˜∏√Ω·¬€µƒ «°°°°°° °£
a£Æ±˚µƒ«‚ªØŒÔŒ»∂®£¨º◊µƒ«‚ªØŒÔ≤ªŒ»∂®
b£Æ±˚µƒ◊Ó∏þº€—ıªØŒÔ∂‘”¶µƒÀÆªØŒÔ ««øÀ·£¨º◊µƒ «»ıÀ·
c£Æ±˚µƒ◊Ó∏þº€—ıªØŒÔ∂‘”¶µƒÀƪ،ԓ◊»Ð”⁄ÀÆ£¨º◊µƒƒ—»Ð
°°°°°° (5)º◊”ΌϖŒ≥…µƒªØ∫œŒÔ”ÎÀÆ∑¥”¶…˙≥…¡Ω÷÷À·£¨∑¥”¶µƒªØ—ß∑Ω≥Ã Ω «
°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
23£Æ(8∑÷)
°°°°°° ”√98%(√Ð∂»Œ™1£Æ84 g£Øcm3)µƒ≈®¡ÚÀ·≈‰÷∆3 mol£ØLµƒœ°¡ÚÀ·100 mL°£≈‰÷∆≤Ÿ◊˜ø…∑÷Ω‚≥…»Áœ¬º∏≤Ω£∫
°° °°°° A£ÆºÏ≤È»ð¡ø∆ø «∑Ò¬©ÀÆ£ª
°° °°°° B£Æ”√…Ÿ¡ø’Ù¡ÛÀÆœ¥µ”°°°°°°°°°°°°°°°°°° 2~3¥Œ£¨Ω´»Ð“∫◊¢»Î»ð¡ø∆ø£ª
°° °°°° C£ÆΩ´¿‰»¥÷¡ “Œ¬µƒœ°¡ÚÀ·◊¢»Î°°°°°°°°°° ÷–£ª
°° °°°° D£Æ∏˘æðº∆À„£¨”√¡øÕ≤»°°°°°°°°°°°°° mL≈®¡ÚÀ·£ª
°° °°°° E£ÆΩ´≈®¡ÚÀ·—ÿ…’±≠±⁄¬˝¬˝◊¢»Î ¢”–’Ù¡ÛÀƵƒ…’±≠÷–£¨≤¢≤ª∂œ”√≤£¡ß∞ÙΩ¡∞Ë£ª
°° °°°° F£Æ∏«…œ»ð¡ø∆ø»˚◊”£¨’Òµ¥£¨“°‘»£ª
°° °°°° G£Æ”√Ω∫Õ∑µŒπеŒº”’Ù¡ÛÀÆ÷¡°°°°°°°°°°°°°° °°°°°°°°°°°°°°°°°°°°°°°°£ª
°° °°°° H£ÆºÃ–¯Õ˘»ð¡ø∆ø÷––°–ƒµÿµŒº”’Ù¡ÛÀÆ£¨ π“∫√ÊΩ”Ω¸øÃ∂»œþ°£
ªÿ¥œ¬¡–Œ £∫
°° (1)ÕÍ≥……œ ˆÃÓø’°£
°° (2)’˝»∑µƒ≤Ÿ◊˜À≥–Ú «£∫A°˙D°˙°°°°°°°° °˙°°°°°°°° °˙°°°°°°°° °˙°°°°°°°° °˙G°˙F°£°°°°
°° (3)”…”⁄¥ÌŒÛ≤Ÿ◊˜£¨ª· πÀ˘≈‰œ°¡ÚÀ·≈®∂»∆´–°µƒ «°°°°°°°°°°°°°°°° (ÃÓ–¥±ý∫≈)°£
 a£Æ”√¡øÕ≤¡ø»°≈®¡ÚÀ· ±£¨∂¡ ˝ ±—ˆ ”
a£Æ”√¡øÕ≤¡ø»°≈®¡ÚÀ· ±£¨∂¡ ˝ ±—ˆ ”
b£Æ»ð¡ø∆ø÷–”–…Ÿ–Ì’Ù¡ÛÀÆ
c£Æ◊™“∆»Ð“∫π˝≥Ã÷–”–“∫ÃÂÕ‚Ω¶
22£Æ(8∑÷)
°°°°°° ∫œ≥…∞±π§“µ∂‘ªØ—ß∫Õπ˙∑¿π§“µæþ”–÷ÿ“™“‚“°£
°° °°°° (1) µ—È “”˚”√œ¬ÕºÀ˘ æ◊∞÷√(º–≥÷πÃ∂®◊∞÷√¬‘»•)÷∆±∏≤¢ ’ºØ∞±∆¯°£
¢Ÿ«Î‘⁄Õº÷–…’∆øƒ⁄ªÊ≥ˆµºπÐÀ˘»±≤ø∑÷°£
¢⁄ ‘πÐ÷–∑¥”¶µƒªØ—ß∑Ω≥Ã Ω «
°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
¢€Œ™Œ¸ ’∂ý”ýµƒ∞±∆¯£¨…’±≠÷–µƒ ‘º¡ «°°°°°°°°°°°° °£
°°°°°° (2)∞±”–∫Ð∂ý÷ÿ“™–‘÷ °£ °°°°
¢ŸΩ´∑”ٻГ∫µŒº”µΩ∞±ÀÆ÷–»Ð“∫≥ ∫Ï…´£¨∆‰‘≠“Ú «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
¢⁄πе¿π§»À‘¯æ≠”√≈®∞±ÀƺϗȬ»∆¯πе¿ «∑Ò¬©∆¯£¨»Á≥ˆœ÷∞◊—ã¨Àµ√˜”–¬»∆¯–π¬∂£¨Õ¨ ±ªπ”–“ª÷÷œý∂‘∑÷◊”÷ ¡øŒ™28µƒ∆¯ÃÂ…˙≥…£¨∏√∑¥”¶µƒªØ—ß∑Ω≥Ã Ω «°°°°°°°°°°°°°°°°°°°°°° °£
(3)–¥≥ˆ∞±µƒ¡Ω÷÷”√Õæ°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
21£Æ”√CH4¥þªØªπ‘≠NOxø…“‘œ˚≥˝µ™—ıªØŒÔµƒŒ€»æ°£“—÷™£∫
 ¢Ÿ
¢Ÿ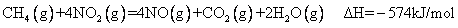
¢⁄
°°°°
¢€
°°°°°° œ¬¡–Àµ∑®≤ª’˝»∑µƒ «°°
°° °°°° A£Æµ»ŒÔ÷ µƒ¡øµƒCH4≤Œº”∑¥”¶£¨∑¥”¶¢Ÿ¢⁄◊™“∆µƒµÁ◊” ˝œýÕ¨
°° °°°° B£Æ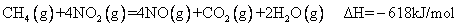
°° °°°° C£Æ0.2 mol CH4ªπ‘≠NO2÷¡N2£¨«“…˙≥…H2O(g)∑≈≥ˆµƒ»»¡øŒ™173£Æ4kJ
°° °°°° D£Æ»Ù”√4£Æ48 L(±Í◊º◊¥øˆ)CH4ªπ‘≠NO2÷¡N2£¨’˚∏ˆπ˝≥Ã÷–◊™“∆µÁ◊”1£Æ60mol
µ⁄IIæÌ(∑«—°‘Ò±ææÌπ≤58∑÷)
20£Æ‘™ÀÿXµƒµ•÷ º∞X”ÎY–Œ≥…µƒªØ∫œŒÔƒÐ∞¥œ¬ÕºÀ˘ 浃πÿœµ∑¢…˙◊™ªØ°£‘ÚXŒ™

°°°°°° A£Æµ± ±£¨Xø…ƒÐ «C°°°° °°°°°° B£Æµ±
±£¨Xø…ƒÐ «C°°°° °°°°°° B£Æµ± ±£¨Xø…ƒÐ «Al°°°°
±£¨Xø…ƒÐ «Al°°°°
C£Æµ± ±£¨Xø…ƒÐ «S°°°° °°°°°° D£Æµ±
±£¨Xø…ƒÐ «S°°°° °°°°°° D£Æµ± ±£¨Xø…ƒÐ «Na
±£¨Xø…ƒÐ «Na
19£Æ‘⁄»ðª˝“ª∂®µƒ√б’»ð∆˜÷–£¨∑¥”¶A(?)+B(g) C(g)+2D(g)¥ÔµΩ∆Ω∫‚∫Û£¨…˝∏þŒ¬∂»»ð∆˜ƒ⁄∆¯Ãµƒ√Ð∂»‘ˆ¥Û£¨‘Úœ¬¡–– ˆ“ª∂®’˝»∑µƒ «°°
C(g)+2D(g)¥ÔµΩ∆Ω∫‚∫Û£¨…˝∏þŒ¬∂»»ð∆˜ƒ⁄∆¯Ãµƒ√Ð∂»‘ˆ¥Û£¨‘Úœ¬¡–– ˆ“ª∂®’˝»∑µƒ «°°
°° °°°° A£Æ’˝∑¥”¶ «Œ¸»»∑¥”¶£¨«“A≤ª «∆¯Ã¨°°°°
°°°°°° B£Æ’˝∑¥”¶ «∑≈»»∑¥”¶£¨«“A «∆¯Ã¨
°° °°°° C£Æº”»Î…Ÿ¡øC£¨ŒÔ÷ Aµƒ◊™ªØ¬ ‘ˆ¥Û
°°°°°° D£Æ∏ƒ±‰—π«ø∂‘∏√∆Ω∫‚µƒ“∆∂،ޔ∞œÏ
18£Æ“—÷™£∫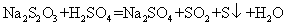 £¨œ¬¡–∏˜◊È µ—È÷–◊Óœ»≥ˆœ÷ªÎ◊«µƒ «°°
£¨œ¬¡–∏˜◊È µ—È÷–◊Óœ»≥ˆœ÷ªÎ◊«µƒ «°°
|
µ—È |
∑¥”¶Œ¬∂»/°Ê |
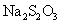 »Ð“∫ »Ð“∫ |
ϡ |
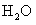 |
||
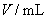 |
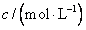 |
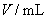 |
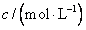 |
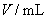 |
||
|
A |
25 |
5 |
0.1 |
10 |
0.1 |
5 |
|
B |
25 |
5 |
0.2 |
5 |
0.2 |
10 |
|
C |
35 |
5 |
0.1 |
10 |
0.1 |
5 |
|
D |
35 |
5 |
0.2 |
5 |
0.2 |
10 |
17£Æ∞—A°¢B°¢C°¢DÀƒ÷÷ŒÔ÷ ∑≈‘⁄√б’»ð∆˜÷–∑¥”¶£¨∑¥”¶«∞∫Û∏˜ŒÔ÷ µƒ÷ ¡øº˚œ¬±Ì£∫
|
°° |
A |
B |
C |
D |
|
∑¥”¶«∞÷ ¡ø/g |
19.7 |
8.7 |
23.6 |
0.4 |
|
∑¥”¶∫Û÷ ¡ø/g |
¥˝≤‚ |
17.4 |
2 |
3.6 |
œ¬¡–Àµ∑®≤ª’˝»∑µƒ «°°°°
°° A£ÆAŒ™≤˙ŒÔ
°° B£ÆŒÔ÷ C“ª∂® «ªØ∫œŒÔ
°° C£Æ¥À∑¥”¶≤ª“ª∂® «—ıªØªπ‘≠∑¥”¶
°° D£Æ»ÙA°¢Cµƒƒ¶∂˚÷ ¡ø÷Ʊ»Œ™97£∫108£¨‘ÚA°¢Cµƒº∆¡ø ˝÷Ʊ»Œ™1£∫2
16£Æ‘™Àÿ‘⁄‘™Àÿ÷Ð∆⁄±Ì÷–µƒŒª÷√ƒÐ∑¥”≥‘™Àÿµƒ‘≠◊”Ω·ππ∫Õ–‘÷ °£œ¬¡–Àµ∑®’˝»∑µƒ «
°° °°°° A£ÆÕ¨“ª‘™Àÿ≤ªø…ƒÐº»±Ìœ÷Ω Ù–‘£¨”÷±Ìœ÷∑«Ω Ù–‘
°° °°°° B£Æµ⁄»˝÷Ð∆⁄‘™Àÿµƒ◊Ó∏þ’˝ªØ∫œº€µ»”⁄À¸À˘¥¶µƒ÷˜◊Â–Ú ˝
°° °°°° C£ÆÕ¨“ª÷Ð∆⁄‘™Àÿ£¨µÁ◊”≤„ ˝œýÕ¨£¨ªØ—ß–‘÷ “≤œýÕ¨
°° °°°° D£ÆÕ¨÷˜◊‘™Àÿ£¨◊ÓÕ‚≤„µÁ◊” ˝∫ժؗߖ‘÷ ÕÍ»´œýÕ¨
15£ÆNAŒ™∞¢∑¸º”µ¬¬Þ≥£ ˝£¨œ¬¡–Àµ∑®’˝»∑µƒ «
°° °°°° A£Æ1 L l mol£ØL¥◊À·»Ð“∫÷–∫¨”–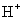 ˝Œ™NA
˝Œ™NA
°°°°°° B£Æ±Í◊º◊¥øˆœ¬£¨2£Æ24 L NH3∫¨µÁ◊”◊Ð ˝Œ™NA
°° °°°° C£Æ≥£Œ¬≥£—πœ¬£¨1 molÎ≤∆¯∫¨”–µƒ‘≠◊” ˝Œ™2NA
°° °°°° D£Æ“ª∂®Ãıº˛œ¬£¨24£Æ5 L¬»∆¯÷–À˘∫¨π≤”√µÁ◊”∂‘µƒ ˝ƒø≤ªø…ƒÐŒ™NA
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com