
4. 如图,水平放置的三棱柱的侧棱长和底边长均为2,且侧棱 ,正视图是边长为2的正方形,该三棱柱的侧视图面积为( )
,正视图是边长为2的正方形,该三棱柱的侧视图面积为( )
 A.
A. 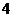 B.
B. 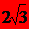 C.
C.
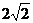 D.
D.
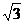 ……
……
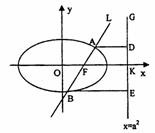
3.已知函数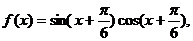 则下列判断正确的是 ( )
则下列判断正确的是 ( )
A.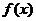 的最小正周期为2π,其图象的一条对称轴为
的最小正周期为2π,其图象的一条对称轴为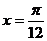
B.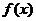 的最小正周期为2π,其图象的一条对称轴为
的最小正周期为2π,其图象的一条对称轴为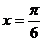
C. 的最小正周期为π,其图象的一条对称轴为
的最小正周期为π,其图象的一条对称轴为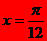
D.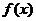 的最小正周期为π,其图象的一条对称轴为
的最小正周期为π,其图象的一条对称轴为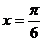
2. 已知命题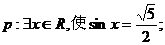
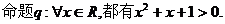 给出下列结论:
给出下列结论:
①命题“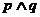 ”是真命题 ②命题“
”是真命题 ②命题“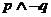 ”是假命题
”是假命题
③命题“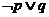 ”是真命题; ④命题“
”是真命题; ④命题“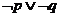 ”是假命题
”是假命题
其中正确的是 ( )
A.②③ B.②④ C.③④ D.①②③
1.复数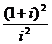 = ( )
= ( )
A.2 B.-2 C.-2i D.2i
27、(10分)根据《中学化学》2009.9的文章《推理与实验不相符的两个问题》介绍:
将足量的铜片与一定量的浓硫酸共热反应,会不会出现随反应的进行硫酸浓度变稀而使反应停止,最终铜和硫酸都有剩余?
某研究性学习小组按下图定性实验简易装置进行实验探究,部分现象如下:
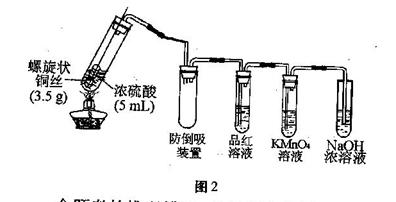
观察到:开始加热(浓硫酸未沸腾)时铜表面由光亮变黑,且黑色小颗粒扩散到浓硫酸中,并不断增多,当浓硫酸加热至沸腾时,黑色小颗粒逐渐溶解,溶液呈浅蓝色,继续加热时浅蓝色溶液逐渐变为灰白色悬浊液,液体量越来越少,最后全部变为灰白色固体。
查资料知:①浓硫酸沸腾温度为338℃,这是硫酸和水的恒沸点温度。②胆矾失去全部结晶水的温度为150℃.
请回答:(1)写出灰白色固体化学式
(2)反应过程中,可观察到品红溶液、KMnO4溶液褪色,这分别体现反应产生气体的 、
性质,其中气体与KMnO4溶液反应离子方程式:
(3)由上分析知:铜与浓硫酸共热,浓硫酸浓度 (填“会”或“不会”)变稀,因此 (填“会”或“不会”)出现反应自动停止,最终铜和硫酸都有剩余的现象。
(4)由上结论计算:将5ml 98%(密度为1.84g/cm3)的浓硫酸与足量的铜共热反应,产生气体的物质的量为( )
A.0.092mol B.0.046 mol C.小于0.046 mol D.大于0.046 mol,小于0.092 mol
诏安一中、长泰一中、龙海二中、平和一中、南靖一中五校联考
26、(13分)Fenton法常用于处理含难降解有机物的工业废水,通常是在调节好PH和Fe2+浓度的废水中加入H2O2,所产生的羟基自由基能氧化降解污染物。现运用该方法降解有机污染物p-CP,探究有关因素对该降解反应速率的影响。
[实验设计]控制p-CP的初始浓度相同,恒定实验温度在298K或313K(其余实验条件见下表),设计如下对比试验
(1) 请完成以下实验设计表(表中不要留空格)。
|
实验 编号 |
实验目的 |
T/K |
PH |
c/10-3mol·L-1 |
|
|
H2O2 |
Fe2+ |
||||
|
① |
为以下实验作参考 |
298 |
3 |
6.0 |
0.30 |
|
② |
探究温度对降解反应速率的影响 |
|
|
|
|
|
③ |
|
298 |
10 |
6.0 |
0.30 |
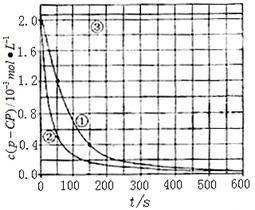
[数据处理]实验测得p-CP的浓度随时间变化的关系如右上图
(2)请根据右上图实验①曲线,计算降解反应在50~150s内的反应速率:
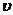 (p-CP)= mol·L-1·s-1
(p-CP)= mol·L-1·s-1
[解释与结论]
(3)实验①、②表明温度升高,降解反应速率增大。但温度过高时反而导致降解反应速率减小,请从Fenton法所用试剂H2O2的角度分析原因: 。
(4)实验③得出的结论是:PH等于10时, 。
[思考与交流]
(5)实验时需在不同时间从反应器中取样,并使所取样品中的反应立即停止下来。根据上图中的信息,给出一种迅速停止反应的方法:
25、(12分)重铬酸钠(Na2Cr2O7)广泛用于合成颜料、媒染剂等,以铬铁矿(主要成分为Cr2O3,还含有FeO、Al2O3、SiO2等杂质)为原料制取重铬酸钠的流程图如下:
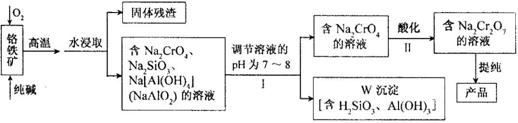
请回答下列问题。
⑴若Ⅰ中只用一种试剂调节溶液的pH,应选用 (填标号)。
A.稀硫酸 B.氧化钠固体 C.氢氧化钾溶液
⑵Ⅰ中,调节溶液pH后,如果溶液的pH过小,可能导致W沉淀部分溶解,原因是
(用离子方程式表示)。
⑶Ⅱ中,Na2CrO4转化为Na2Cr2O7的离子反应如下:
2CrO42-(黄色)+2H+ Cr2O72-(橙红色)+H2O
Cr2O72-(橙红色)+H2O
①该反应 氧化还原反应(填“是”或“不是”),反应的平衡常数表达式K= 。
②若往Na2Cr2O7溶液(橙红色)中加入足量NaOH固体,溶液 (填标号)。
A.变黄色 B.颜色不变 C.橙红色变深
③已知:25℃,Ag2CrO4的Ksp=1.12×10-12,Ag2Cr2O7的Ksp=2×10-7。25℃,往Ag2Cr2O7溶液中加入AgNO3溶液,最终只生成一种砖红色沉淀,该沉淀的化学式是 。
24、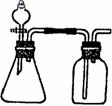 (9分)Ⅰ、利用下列各组物质制备和收集相应的气体,可采用如右下图所示装置(图中
(9分)Ⅰ、利用下列各组物质制备和收集相应的气体,可采用如右下图所示装置(图中
尾气处理装置略)的是 (填序号)。
① 石灰石和稀盐酸 ② 二氧化锰和浓盐酸
③ 铜和稀硝酸 ④ 铜和浓硫酸
⑤ 浓盐酸和浓硫酸 ⑥ 铝和烧碱溶液
Ⅱ、联氨(N2H4)及其衍生物是一类重要的火箭燃料。
N2H4与N2O4反应能放出大量的热。
(1)已知:2NO2(g) N2O4(g)
△H=-57.20kJ·mol-1。一定温度下,在密闭容器中反应2NO2(g)
N2O4(g)
△H=-57.20kJ·mol-1。一定温度下,在密闭容器中反应2NO2(g) N2O4(g)达到平衡。
N2O4(g)达到平衡。
其他条件不变时,下列措施能提高NO2转化率的是 (填字母)
A.减小NO2的浓度 B.降低温度 C.增加NO2的浓度 D.升高温度
(2)25℃时,1.00gN2H4(l)与足量N2O4(l)完全反应生成N2(g)和H2O(l),放出19.14kJ的热量。则反应2N2H4(l)+N2O4(l)=3N2(g)+4H2O(l)的△H= kJ·mol-1
Ⅲ、 镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd + 2NiOOH + 2H2O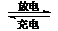 Cd(OH)2
+ 2Ni(OH)2
Cd(OH)2
+ 2Ni(OH)2
(3)该电池充电时阳极反应式:
(4)放电时负极附近溶液的碱性 (填“增强”或“减弱”或“不变”)
23、(12分)短周期元素X、Y、Z、W的原子序数依次增大,它们原子的最外层电子数均不少于最内层电子数。其中X是形成化合物种类最多的元素。Y固体单质与盐酸反应,再向反应后的溶液中加入一定量的烧碱溶液,最终溶液中有白色沉淀Q生成。Z元素的氧化物既能溶于稀硫酸,又能溶于浓NaOH溶液。W的最高价氧化物形成的水化物在自然界中酸性最强 填写下列空白:
填写下列空白:
(1)X的最高价氧化物的结构式为
(2)写出生成白色沉淀Q的化学方程式 ,
已知298K时,该物质的的Ksp=5.6×10-12,若此时测得溶液PH=13.00,则此温度下残留在溶液中的Y离子物质的量浓度为 。
(3)Z元素的氧化物溶于浓NaOH溶液的离子方程式:
(4)写出W单质的一种用途 。
(5)Y、Z、W四种元素的原子半径由大到小的顺序为 (用元素符号表示)
22、已知某可逆反应mA(g)+nB(g)  qC(g) △H ,在密闭容器中进行。如图所示反应在不同时间t,温度T和压强P与反应物B的体积分数的关系曲线。根据图象判断
qC(g) △H ,在密闭容器中进行。如图所示反应在不同时间t,温度T和压强P与反应物B的体积分数的关系曲线。根据图象判断
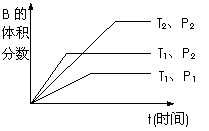 A.T1>T2,
△H>0, P1>P2, m+n>q
A.T1>T2,
△H>0, P1>P2, m+n>q
B.T1>T2, △H>0, P1<P2, m+n<q
C.T1<T2, △H<0, P1>P2, m+n>q
D.T1>T2, △H<0,,P1<P2, m+n>q
第Ⅱ卷(非选择题 共56 分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com