
4.下列关于文学常识的表述不正确的一项是
A.我国文学史向来以“风骚”并称,“风”指的是《诗经》中的“国风”,“骚”指的是《离骚》,它们分别开创我国诗歌现实主义和浪漫主义的传统。
B.《孔雀东南飞》是保存下来的我国古代最长的叙事诗,是古乐府民歌的代表作,与《木兰辞》并称为“乐府双璧”。
C.雨果是19世纪伟大的批判现实主义文学家,是法国文学史上最伟大的作家之一。《巴黎圣母院》是他创作的第一部长篇小说。
D.《家》是巴金小说的代表作,作品中的主人公觉新是一个充满朝气的叛逆者的典型。
3.下列各句中加点的成语使用不恰当的一项是
A.有人希望,黑人只要撒撒气就会满足;如果国处变不惊,毫无反应,这些人必会大失所望的。
B.由于剩余价值的发现,这里就豁然开朗了,而先前无论资产阶级经济学家或者社会主义批评家所做的一切研究都只是在黑暗中摸索。
C.但马克思在他所研究的每一个领域(甚至在数学领域)都有独到的发现,这样的领域是很多的,而且其中任何一个领域他都不是浅尝辄止。
D.试验既终,书籍束之高阁,毫不过问,敷衍三四年,潦草塞责,文凭到手,即可惜此活动于社会,岂非与求学初衷大相背驰乎?
2.下列词语中没有错别字的一项是
A. 迁徒 商榷 班驳 流觞曲水
B. 渺茫 落寞 俊峭 闻名遐迩
C. 风致 肄业 歧途 涸澈而鱼
D. 深邃 砥砺 真谛 安之若素
1. 下列词语中加点字的注音全都正确的一项是
A. 倩影(qiàn) 落蕊(ruǐ) 揠苗助长(yà)
B. 裨益(bēi ) 猗郁(yī) 纵横捭阖(bǎi)
C. 窈窕(yáo) 澄清(chéng) 夙兴夜寐(shù)
D. 着装(zháo) 豁达(huò ) 义愤填膺(yīn)
请考生用钢笔或黑色水性笔将自己的姓名班级等信息及所有答案填写在答题卡相应的位置上。
24.(10分)
(1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是 。
A.C(s)+H2O(g)=CO(g)+H2(g) △H>0
B.NaOH(aq)+HC1(aq)=NaC1(aq)+H2O(1) △H<0
C.2H2(g)+O2(g)=2H2O(1) △H<0
(2)以KOH溶液为电解质溶液,依据所选反应设计一个原电池,其负极的电极反应式为
。
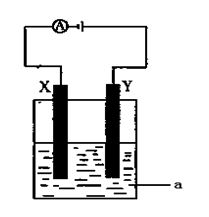 (3)电解原理在化学工业中有着广泛的应用。现将你设计的原电池通过导线与右图中电解池相连,其中a为电解液,X和Y均为惰性电极,则:
(3)电解原理在化学工业中有着广泛的应用。现将你设计的原电池通过导线与右图中电解池相连,其中a为电解液,X和Y均为惰性电极,则:
①若a为CuSO4溶液,则电解时的化学反应方程式为 。通过一段时间后,向所得溶液中加入0.2molCuO粉末,恰好恢复电解前的浓度和pH,则电解过程中转移的电子的物质的量为 。
②若电解含有0.04molCuSO4和0.04molNaCl的混合溶液400ml,当阳极产生的气体672 mL(标准状况下)时,溶液的pH = (假设电解后溶液体积不变)。
宁波市2009学年度第一学期期末试卷
23.(9分)氧化铜有多种用途,如用作玻璃着色剂、油类脱硫剂等,为获得纯净的氧化铜并探究其性质,某同学用工业硫酸铜(含硫酸亚铁等杂质)进行如下实验:
(1)制备氧化铜:
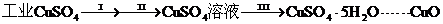
①步骤Ⅰ的目的是除去不溶性杂质。操作是 。
②步骤Ⅱ的目的是除去硫酸亚铁。操作是:滴加H2O2溶液,稍加热;Fe2+转化完全后,慢慢加入Cu2(OH)2CO3粉末,搅拌,以控制溶液pH=3.5;加热煮沸一段时间,过滤,用稀硫酸酸化滤液至pH=1。滴加H2O2的目的是 ,加入Cu2(OH)2CO3粉末的目的是 。
③步骤Ⅲ的目的是得到CuSO4·5H2O晶体,操作是将CuSO4·5H2O溶液加热蒸发至有晶膜出现时,停止加热, ,水浴加热烘干。采用水浴加热的原因是
。
(2)探究氧化铜性质:
①取A、B两支试管,往A中先加入适量CuO粉末,再分别向A和B中加入等体积的3%H2O2溶液,只观察到A中有大量气泡,结论是 。
②为探究试管A中反应的速率,收集气体并测定其体积必需的实验仪器除导管、橡皮塞、水槽外还必须有 。
22.(9分)物质A、E、F的焰色反应呈黄色,物质I的分子由4个原子组成并共含有10个电子,B、C、D、K在常温下都是气体单质,G在常温下是无色液体,反应①-⑤都是用于工业生产的反应,各有关物质之间的相互反应转化关系如下图所示:
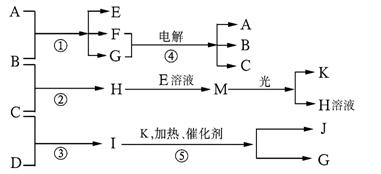
请填写下列空白:
(1)写出下列物质的化学式:B: ;J:_________。
(2)写出下列反应的方程式:
① 反应①的离子方程式: 。
② 反应⑤的化学方程式: 。
(3)在通常状况下,若1 g C气体在B气体中燃烧生成H气体时放出92.3 kJ热量,则2 mol H气体完全分解生成C气体和B气体的热化学方程式为:
。
21.(8分)常温下,将某一元酸HX和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
|
实验编号 |
HX物质的量 浓度(mol·L-1) |
NaOH物质的量 浓度(mol·L-1) |
混合溶液的pH |
|
甲 |
0.2 |
0.2 |
pH=a |
|
乙 |
C1 |
0.2 |
pH=7 |
|
丙 |
0.2 |
0.1 |
pH>7 |
|
丁 |
C2 |
C2 |
pH=10 |
请回答:
(1)不考虑其它组的实验结果,单从甲组情况分析,
若a 7(填>、<或=),则HX为强酸;
若a 7(填>、<或=),则HX为弱酸。
(2)在乙组混合溶液中离子浓度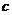 (X-)与
(X-)与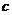 (Na+)的大小关系是
。
(Na+)的大小关系是
。
A.前者大 B.后者大 C.二者相等 D.无法判断
(3)从丙组实验结果分析,HX是 酸(选填“强”或“弱”)。
该混合溶液中离子浓度由大到小的顺序是 。
(4)丁组实验所得混合溶液中由水电离出的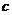
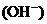 =
mol·L-1。
=
mol·L-1。
20.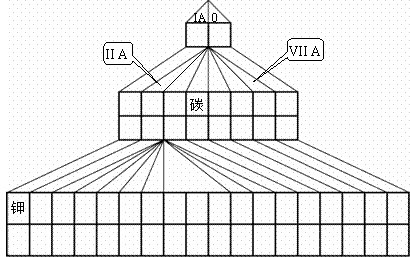 (10分)如图是元素周期表的另一种画法--塔式周期表,在上面标有部分族序数及部分元素,请回答下列问题:
(10分)如图是元素周期表的另一种画法--塔式周期表,在上面标有部分族序数及部分元素,请回答下列问题:
(1)请在图上把VA族涂黑。
(2)短周期元素中,A元素原子最外层电子数是次外层电子数的2倍;B元素最外层电子数是其内层电子总数3倍;C元素与B元素同族;D元素原子最外层有1个电子,D的阳离子与B的阴离子电子层结构相同,试回答:
①写出B、C元素的名称__________、___________;在塔式周期表相应位置标出D 元素的元素符号。
②写出一种由B、D元素组成的化合物的电子式: 。
③A的固态氧化物属于 晶体。(填“分子”、“原子”或“离子”)
④写出C的最高价氧化物的水化物与D的氧化物对应的水化物反应的离子方程式:
。
(3)在上述塔式周期表中列出了5行元素,每行所包含的元素种类分别为2、8、8、18、18,则未列出的第六行所包含的元素为________种。请根据行数与元素种数的关系,预言第八行最多可能含有__________种元素。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com