
1、电解--使直流电通过电解质溶液而发生氧化还原反应的过程。
电解时的能量转化:电能转变为化学能。
电解质的导电过程就是电解质的电解过程。
7.4 电解质溶液在通电情况下的变化
|
教学内容 |
教师活动 |
学生活动 |
说明 |
|
复习旧知:水的电解 |
出示电解水的实验装置并提问: 如果使直流电通过水(水中置有电解质,如Na2SO4),会看到怎样的实验现象? 写出反应的化学方程式。 为什么氢气和氧气分别在两个电极上产生呢? 水是弱电解质,能电离出H+和OH- 。当接通直流电时,与电源负极相连的电极带负电,吸引H+,发生反应:2H++2e→H2↑;与电源正极相连的电极就带正电,吸引OH-,发生反应: 4OH--4e→O2↑+ 2H2O |
回忆: 水被电解,分别在两极生成氢气和氧气,且气体的体积比为2:1。 2H2O  2H2↑+
O2↑ 2H2↑+
O2↑思考、分析、听讲。 |
OH-的电极反应可说明氧气的产生,因此教师应告知学生,但不要求学生掌握。 |
|
由水的电解归纳电解的原理 |
电解质的导电过程也就是电解质被电解的过程。 电解是电能转化为化学能的过程。 这种使直流电通过电解质溶液而发生氧化还原反应的过程叫做电解。 |
|
|
|
总结构成电解池的要素和阴、阳两极的反应 |
在这个装置中,与电源正极相连的碳棒为阳极,与电源负极相连的碳棒为阴极。电极材料为石墨。 电流从电源的正极流出,经过阳极通过电解质溶液流向阴极。 整个这套装置就是电解池。 |
观察水的电解的实验装置,比较,归纳。 |
|
|
提出问题:分析电解饱和食盐水时产物为什么是氢气、氯气、氢氧化钠 |
水的电解过程就是水电离出的两种离子在阴、阳两极的反应过程。 我们还学习过电解饱和食盐水。请根据提供的实验用品完成电解饱和食盐水的实验,填写教材p92-“思考与讨论”。并用分析水的电解的方法分析电解饱和食盐水的实验现象,写出电极反应式以及化学方程式。 |
实验:电解饱和食盐水。 将一块长方形滤纸平放在玻璃板上,用NaCl酚酞试液充分浸润,分别用旧2号电池芯作阴阳极,分别用滤纸两端将电极轻轻相向卷在其中,并接通电源。通电2分钟后,立即打开裹有碳棒的一端滤纸,发现滤纸变红,证明NaOH在阴极生成。再打开另一端,滴入一滴碘化钾-淀粉溶液,滤纸变蓝,证明阳极有氯气生成。 填写实验结果 |
本实验优点:药品用量少,电极产物检验方法简单,现象直观,节省时间。 |
|
讨论电解饱和食盐水时阴极和阳极产物的生成原因。并归纳饱和食盐水中四种离子的得失电子能力。 |
为什么在阴极酚酞会变红 ? 为什么阳极产生的是氯气而不是氧气? |
讨论: 溶液中的离子比纯水多了两种:Na+、Cl-。 阴极酚酞变红,说明OH-浓度大于H+,由此可推测H+发生电极反应转化为氢气,使水的电离平衡被破坏,电离出更多的OH-;还说明H+的得电子能力大于Na+。 阳极带正电,吸引阴离子,产物是氯气而不是氧气,说明发生电极反应的是Cl-而不是OH-,即失电子能力Cl-> OH-。 |
|
|
了解隔膜式电解槽 |
以电解饱和食盐水为基础的工业是一项重要的化学工业。看p93图7.2,与刚才学习的电解池进行对比,说明阳离子交换膜电解槽的优点。 |
看书、讨论。 具有电解池结构。不同之处是后者有阳离子交换膜将阴极室和阳极室分开。 优点:使OH-和Cl-及Cl2分开,能得到高纯度的烧碱,提高产品质量;减少了分离NaOH和NaCl的工序。 |
|
2.主要板书
2.流程说明
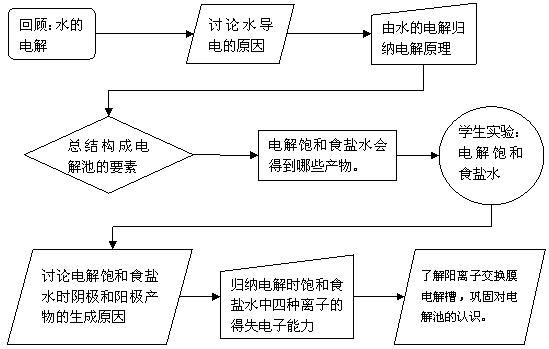
(1)回顾水的电解并讨论水导电的原因:以学生熟悉的知识作为起点,提出问题引导学生探究熟悉的现象背后隐含的本质,促使学生在分析水的导电原因的过程中,主动运用电解质概念、电离平衡以及平衡移动原理等知识从而深化理解。知道电解质电解的过程就是电解质导电的过程
(2)由水的电解归纳电解原理以及电解池构成:运用氧化还原反应理论,根据产物分析阴极、阳极离子的反应情况,归纳电解原理、电解池结构。
(3)电解饱和食盐水的实验以及产物分析:该实验在本套教材高一年级第一册第二章第一节“以食盐为原料的化工产品”中曾经演示过,当时侧重于观察电解时得到的产物。本课中,安排学生动手实验,观察的侧重点为电解的装置以及电解产物在电解池中产生的位置,以促使学生进一步认识电解过程中阴、阳极发生的反应、电解质溶液中离子的得失电子能力,感受氧化还原理论对于理解电解原理的指导作用。
(4)了解离子交换膜电解槽,巩固对电解池的认识。在认识离子交换膜电解槽所包含的常规电解池结构的基础上,感受工业生产中对电解槽所进行的技术创新带来的巨大优势。
1.流程图
电解水的实验用具一套 电解饱和食盐水的微型学生实验用品
2.难点
电解饱和食盐水的阴极区产物
1.重点
电解原理、饱和食盐水中离子的放电顺序
3.情感态度与价值观
(1)从对电解水、饱和食盐水实验现象的分析中,领悟宏观表象和微观本质的关系。
(2)通过对阳离子交换膜电解槽的认识,感受电解原理在工业生产中的应用和技术的进步。
2.过程与方法
通过电解饱和食盐水的实验,运用观察、分析、抽象、概括的思维方法探究电解池结构以及工作原理。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com