
31.(18分)耐火材料主要成分为MgO和A1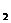 O
O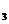 ,某厂用蛭石(主要成份为:MgO、Fe2O3、A12O3、SiO2)作原料生产耐火材料。化学课外小组同学用蛭石进行了以下实验:
,某厂用蛭石(主要成份为:MgO、Fe2O3、A12O3、SiO2)作原料生产耐火材料。化学课外小组同学用蛭石进行了以下实验:
Ⅰ.查阅资料得知0.1mol/L的离子浓度时,氢氧化物沉淀时的pH为
|
氢氧化物 |
Fe(OH)3 |
Mg(OH)2 |
AI(OH)3 |
|
|
开始沉淀时的pH |
2.3 |
10.4 |
4.0 |
开始溶解:7.8 |
|
完全沉淀时的pH |
3.7 |
12.4 |
5.2 |
完全溶解:10.8 |
Ⅱ.实验流程如下(固体A、F为一种成份):

请回答以下问题:
(1)写出下列物质化学式:试剂I___________________;固体F 。
(2)步骤②B生成C的离子方程式为 。
(3)要保证固体D杂质尽量少,步聚②调节溶液的pH合理范围是 :
A.12.4~13 B.10~10.8 C.3.7~5.2
 (4)固体D可用来生产合成氨的表面催化剂。右图表示无催化剂时NH
(4)固体D可用来生产合成氨的表面催化剂。右图表示无催化剂时NH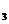 的百分含量随时间变化曲线,请在图上用虚线画出有催化剂时的曲线。
的百分含量随时间变化曲线,请在图上用虚线画出有催化剂时的曲线。
(5)已知:N2 (g)+3H2 (g)===2NH3 (g) ΔH= -a kJ·mol-1
2H2O(1)===2H2 (g)+O2 (g) ΔH= +b kJ·mol-1
则NH3被O2氧化为N2和H2O的热化学方程式为 。
0.1mol/LBa(NO3)2、3%H2O2、10%NaOH溶液、蒸馏水、品红溶液;仪器自选。
(1)提出假设
假设一:固体全部是Na2SO3; 假设二:固体全部是Na2SO4;
假设三 。
(2)设计实验方案(略);从绿色环保的角度,最好选用下列中的 (填序号)进行实验:
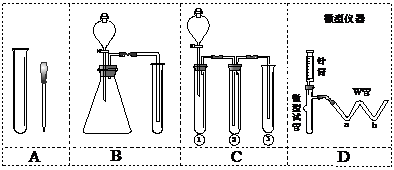
(3)进行实验:请在下表中用简要文字写出实验操作、预期现象和结论(写在答题卡上)。
|
实验步骤 |
预期现象和结论 |
|
步骤1: |
|
|
步骤2: |
|
|
步骤3: |
|
|
……… |
|
30.(18分)现有一瓶实验室放置已久的可能被氧化的Na2SO3固体,为了研究它的组成,请你参与同学们进行的如下探究活动:
可选用试剂:浓H2SO4、浓HNO3、10%盐酸、0.1mol/LH2SO4、0.1mol/L HNO3、0.1mol/LBaCl2、
23.对于反应:2SO2 (g)+O2 (g)  2SO3 (g) △H<0 ,下列有关曲线图示正确的是
2SO3 (g) △H<0 ,下列有关曲线图示正确的是

第Ⅱ卷(非选择题,共64分)
22.在下列下列说法正确的是
A.加入铝粉生成H2的溶液中,K+、Cu2+、SO42-、ClO-能大量共存
B.在c(OH-) = 10-2 mol·L-1的溶液中,NO3-、Ba2+、Cl-、Br-能大量共存
C.0.1 mol/L Na2CO3溶液中:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+)
D.0.1 mol/L Na2CO3溶液中:2c(Na+) =c(H2CO3)+c(CO32-)+c(HCO3-)
12.下列实验操作正确的是
①蒸馏时,应使温度计水银球应插入蒸馏烧瓶液体中
②测溶液pH时,用玻璃棒蘸取溶液点滴到放在表面皿上的pH试纸上
③制乙酸乙酯时,把乙醇和乙酸依次加入浓硫酸中
④制乙烯时,为防止暴沸,向反应液中加入碎瓷片
⑤滴定管洗净后经蒸馏水润洗,马上注入标准液进行滴定
⑥加热坩埚中的硫酸铜晶体,失水后在空气中冷却,再称量
⑦分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
A. ①③⑤⑦ B. ②④⑥ C. ②④⑦ D. ④⑤⑥⑦
11. 下列是某同学对相应反应的离子方程式所作的评价,其中评价合理的是
|
编号 |
化学反应 |
离子方程式 |
评价 |
|
A |
碳酸钙与 醋酸反应 |
CO32-+2CH3COOH = CO2↑+H2O+2CH3COO- |
错误。碳酸钙是弱电解质,不应写成离子形式 |
|
B |
苯酚钠溶液中 通入少量CO2 |
2C6H5O-+ CO2 + H2O → CO32- +2C6H5OH |
正确。 |
|
C |
NaHSO3的水解 |
HSO3-+H2O SO32-+H3O+ SO32-+H3O+ |
错误。水解方程式误写成电离方程式 |
|
D |
等物质的量的 FeBr2和Cl2反应 |
2Fe2++2Br-+2Cl2 = 2Fe3++Br2+4Cl- |
错误。Fe2+与Br-的物质的量之比与化学式不符 |
10.下列说法错误的是
①可燃冰和乙醇是较清洁的能源;②甲醇、乙二醇、丙三醇是同系物;③某烷烃叫做2-乙基丁烷;④镀锌铁比镀锡铁更耐腐蚀;⑤石钟乳的形成是因为石灰石在水中存在溶解平衡;⑥甘氨酸和丙氨酸可生成4种二肽;⑦蔗糖和萄萄糖均能发生银镜反应;
A.②③⑦ B.①④⑤ C.②③⑥ D.③④⑥
9. 科学家发现了如下反应:O2+PtF6=O2 (PtF6),其中O2(PtF6)为离子化合物,其中Pt为+5价。下列说法正确的是
A.O2 (PtF6) 中不存在共价键
B.O2 (PtF6)中氧元素的化合价是+l价
C.在此反应中,O2是氧化剂,PtF6是还原剂
D.在此反应中每生成1mol O2 (Pt F6),转移6.02×1023个电子
8.下列排列顺序正确的是
①热稳定性:H2O>NH3>CH4 ②离子半径:Na+>Mg2+>F-
 ③酸性:盐酸>硼酸>醋酸 ④结合质子能力:OH- >
> HCO3-
③酸性:盐酸>硼酸>醋酸 ④结合质子能力:OH- >
> HCO3-
A.①③ B.①④ C.②④ D.②③
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com