
3.突破难点
(1)分析讨论
①阴极附近溶液变红,说明有碱生成。从原子守恒的角度分析,只可能是NaOH。
②阳极生成了能使淀粉碘化钾试纸变蓝的气体,教师告诉学生,这是氯气。
③阴极气体点燃有爆鸣现象,是氢气生成。
④如何得出电解饱和食盐水的方程式?在目前高一的水平上(没有电解质、电离的概念,没有系统学习过氧化还原)只有用原子守恒“硬凑”出来:
反应物:NaCl和H2O,生成物:NaOH、Cl2和H2。从氯原子入手,应该在NaCl前配系数2,然后导出其余系数,得出完整的化学方程式。
(2)补充相关知识及概念
刚才在对电解饱和食盐水的实验进行分析的时候,我们谈到,食盐水中存在的不是NaCl分子,而是Na+和Cl-。这是怎么回事呢?请大家看课本P29的“资料库”。引出电离方程式的基本概念。
2.实验活动
教师用PPT的方式讲清楚实验的注意事项,关键是要把问题清楚地罗列出来,让同学们边实验边思考。具体内容可参考课本P28的“课堂实验”部分。若氢气收集不易,可省略此步。
1.情景引入
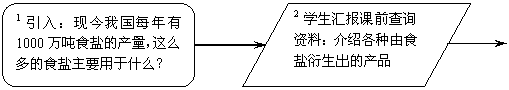
上一节课我们系统学习了有关粗盐提纯的知识,而且课本P25也提到了“我国目前海盐的年产量已超过1×107t,位居世界之首”。那么请问同学们,如此巨大的海盐产量,是否全部用来满足人民的食用了呢?下面我们请几位同学,将他们课前查找的资料向全班展示一下,以此我们来了解一下大量食盐的主要用途是什么……
3.流程图说明
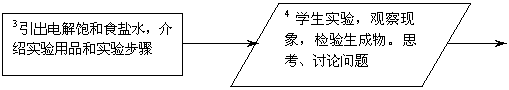
(1)实验步骤:先往U型管中加入饱和食盐水(注意留出上端空间),两边各加少许酚酞,再插入电极棒,告诉学生不同材质的电极分别是什么电极,要求学生用湿润的淀粉碘化钾试纸检验阳极产物,用小试管收集阴极气体,做爆鸣实验。
(2)电解时要学生观察三处实验现象:何处溶液变红;试纸是否变蓝;收集的气体能否爆鸣。告诉学生能让试纸变蓝的气体是氯气,让他们讨论得出化学方程式(利用质量守恒定律)。
(3)写出化学方程式,并用“中国现代化工之母”引出化学史话的教学。
(4)电离方程式强调两点:电荷守恒和离子团不拆开表达。在练习中注意给出的都是常见的强酸、强碱,如HCl、H2SO4、NaOH、NaCl等,不要涉及弱电解质。
(5)氢氧化钠的性质学生在初中已有所接触,可以让学生通过相关化学方程式进行归纳,教师则主要介绍烧碱的用途。
2.流程图



1.设计思想
因为本节课教学涉及到较多高一新生未掌握的知识,因此采用实验--探究的教学模式,尽量让学生通过对实验事实的认识,来掌握相关知识。
2.电脑、投影仪、多媒体设备
1.U型管、铁棒、碳棒、学生电源、淀粉碘化钾试纸、小试管、酒精灯、酚酞、饱和食盐水
2.电离方程式的书写。
1.电解饱和食盐水实验的完成及产物分析。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com