
1ЃЎЧщОАв§Шы
1)1777ФъЗЈЙњЛЏбЇМвРЭпЮ§(Antoine Lavoiser,1743-1794)ЬсГіСЫШМЩебѕЛЏРэТлЃЌЧтЦјдкбѕЦјжаШМЩеЪБЃЌЪВУДЮяжЪЗЂЩњСЫбѕЛЏЗДгІЃП
(2)ЧтЦјвВФмдкТШЦјжаШМЩеЃКH2
+ Cl2 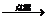 ЁЁ2HCl ЪЧбѕЛЏЛЙдЗДгІТ№ЃПCl2ПЩвдгУзібѕЛЏМСТ№ЃП
ЁЁ2HCl ЪЧбѕЛЏЛЙдЗДгІТ№ЃПCl2ПЩвдгУзібѕЛЏМСТ№ЃП
(3)ЙЄвЕСЖЬњЕФжївЊЗДгІЪЧЃКFe2O3 + 3CO 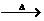 ЁЁ2Fe + 3CO2 дкЛЏбЇЗДгІЛљБОРраЭжаЪєгкФФжжРраЭЃП
ЁЁ2Fe + 3CO2 дкЛЏбЇЗДгІЛљБОРраЭжаЪєгкФФжжРраЭЃП
ЬжТлВЂШЯЪЖЃКРЭпЮ§ЬсГіЕФШМЩебѕЛЏРэТлгаЦфВЛзужЎДІЃЌЫФИібѕЛЏЗДгІЛљБОРраЭВЛФмАќКЌЩЯЪіЙЄвЕСЖЬњЕФЗДгІЃЌБиаыгааТЕФРэТлРДДњЬцШМЩебѕЛЏРэТлЃЌБиЖЈгааТЕФЛЏбЇЗДгІРраЭЕФЗжРрЗНЗЈЁЃ
3.СїГЬЫЕУї
(1)БОЩшМЦЗжСНИіВуДЮ,вЛЪЧвдЪЕЯпПђКЭЪЕЯпМ§ЭЗБэЪОЕФНЬбЇСїГЬЃЛЖўЪЧвдащЯпПђКЭащЯпМ§ЭЗБэЪОЕФШЫУЧШЯЪЖбѕЛЏЛЙдЗДгІЕФЙ§ГЬЃКaЮЊбѕЛЏЛЙдЗДгІЕФЁАЕУЪЇбѕЫЕЁБЃЌbЮЊбѕЛЏЛЙдЗДгІЕФЁАЛЏКЯМлЩ§НЕЫЕЁБЃЌcЮЊбѕЛЏЛЙдЗДгІЕФЁАЕУЪЇЕчзгЫЕЁБЃЌdЮЊЁАЖдИХФюНјааЁЎЬсСЖЁЏЁБЃЌeЮЊЁАБэДябЕСЗЁБЃЌfЮЊЁАзмНсгІгУЁБЁЃ
(2)aЕЅдЊЃКЛивфГѕжаЛЏбЇгаЙибЇЯАФкШнЃЌВЂДгЕУбѕКЭЪЇбѕЕФНЧЖШЗжЮіЯТСаЗДгІжаЕФбѕЛЏМСКЭЛЙдМСЃЌбѕЛЏЗДгІКЭЛЙдЗДгІЃЌВЂаЮГЩНсТлЁЃ
CuO + H2 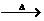 ЁЁCu
+ H2O
ЁЁCu
+ H2O
Fe2O3 + 3CO 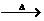 ЁЁ2Fe
+ 3CO2
ЁЁ2Fe
+ 3CO2
(3)bЕЅдЊЃКв§ЕМЗжЮіЩЯЪіСНИіЗДгІГ§СЫЗЂЩњЕУЪЇбѕвдЭтЃЌдкЗДгІЧАКѓЛЙгаЪВУДЗЂЩњСЫИФБфЃПЭЈЙ§ЬжТлЃЌбЇЩњздгЩЗЂбдЃЌЙиМќвЊв§ЕМЭЌбЇевЕНЁАЗДгІЧАКѓгадЊЫиЛЏКЯМлЗЂЩњСЫИФБфЁБЃЌВЂгыaЕЅдЊНсТлЙиСЊЃЌгаЯрЙиЗЂЯжЁЃ
(4)cЕЅдЊЃКЭЛЦЦФбЕуЕФДыЪЉЃК
ЂйжиЯжЗќДђЕчЖбЪЕбщЃЌШУбЇЩњЙизЂгаЕчСїВњЩњЃЌгыЕчзггаЙиЁЃ
ЂкЭЈЙ§ЖЏЛбнЪОв§ЕМбЇЩњЬНОПЛЏКЯМлИФБфгыЕУЪЇЕчзгЕФЙиЯЕЃЌВЂгыбѕЛЏЛЙдЗДгІЯрЙиСЊЃЌгаЯрЙиЗЂЯжЁЃ
(5)dЕЅдЊЃКСЊЯЕНсТл2КЭНсТл3ЃЌШУбЇЩњздМКбАевМЧвфЕФЗНЗЈЃК
(6)eЕЅдЊЃКвЊбЇЩњВЛПДНсТл2КЭНсТл3ЃЌНјааПкЭЗКЭЪщУцБэДябЕСЗЃЌФПЕФЪЧвЊбЇЩњЖдбѕЛЏЛЙдЗДгІЕФжиЕуФкШнМЧвфРЮЙЬЃЌРэНтзМШЗЃЌПЩНсКЯВЛЭЌРраЭЕФЗДгІНјааЗжЮіЁЃ
(7)fЕЅдЊЃКзмНсЪЧНјвЛВННЋБОПЮбЇЯАФкШнЕФНјвЛВНЩ§ЛЊЁЃгІгУЪЧЖдИХФюЕФбгЩьЃЌ
(8)ЭЈЙ§бЇЯАЃЌвЊбЇЩњПЮКѓећРэБОПЮбЇЯАФкШнЃЌаЮГЩжЊЪЖПђМм(жЊЪЖФПБъ)ЁЃ
(9)ЦфЫќНЈвщЃК
Н№ЪєФЦгыТШЦјЗДгІЕФЮЂЙлЖЏЛЃЌПЩСДНгЁАжабЇЛЏбЇзЪСЯЭјЁБЃЌЭјжЗЃК
http://www.e-file/271.htm
2.НЬбЇСїГЬ
 ЁЁ
ЁЁ
 ЁЁ
ЁЁ
 ЁЁ
ЁЁ
 ЁЁ
ЁЁ
 ЁЁ
ЁЁ
1.ЩшМЦЫМЯы
БОПЮЩшМЦЫМЯыЕФжївЊвРОнЪЧЬхбщНЬбЇЁЃЬхбщЪЧвЛИіШЫЖддИЭћЁЂвЊЧѓЕФИаЪмЃЌЪЧвЛжжЬиЪтЕФЛюЖЏЃЌИќЪЧвЛИіЙ§ГЬЃЌвВЪЧЛюЖЏЕФНсЙћЃЌМДЧзРњбЇЯАЙ§ГЬВЂЛёЕУЯргІЕФШЯЪЖКЭЧщИаЁЃЬхбщФмВњЩњЧщИаЃЌЪЧвЛжжгажИЯђвтвхЕФЛюЖЏЃЌЬхбщЪЧжїЬхгыПЭЙлЪРНчЗЂЩњЙиСЊзюжБНгЕФЗНЪНКЭЭООЖЃЌЬхбщзмЪЧЬхбщепздМКЕФЪТЃЌБиаыЧзЩэОРњЁЃ
БОПЮЩшМЦСЫДѓСПЕФбЇЩњЛюЖЏКЭЪІЩњЯрЛЅЛюЖЏЃЌвЊЭЌбЇЧзРњДгЁАИаОѕ(ЕУЪЇбѕ)ЁБЕНЁАБэЯѓ(ЛЏКЯМлИФБф)ЁБдйЕНЁАИХФюМДБОжЪ(ЕУЪЇЕчзг)ЁБЕФШЯЪЖЪТЮяЕФЙ§ГЬЁЃБОПЮЕФКѓАыВПЗжЃЌжївЊЪЧИХФюЕФгІгУЃЌЪЙбЇЩњНјвЛВНРэНтИХФюЕФЭтбгЁЃ
НЬбЇЖрУНЬхЯЕЭГЃЌ(PowerPointЁЂFlash MX)
2.ФбЕу
бѕЛЏЛЙдЗДгІЕФБОжЪЁЃ
1ЃЎжиЕу
ДгЛЏКЯМлЩ§НЕКЭЕчзгзЊвЦНЧЖШРДХаЖЯЁЂЗжЮібѕЛЏЛЙдЗДгІЁЃ
3.ЧщИаЬЌЖШгыМлжЕЙл
(1)ЭИЙ§ЛЏКЯМлБфЛЏЕФЯжЯѓЃЌПДЕНЕчзгзЊвЦЕФБОжЪЁЃДгЖјИаЮђЁАЭИЙ§ЯжЯѓПДБОжЪЁБетвЛБчжЄЮЈЮяжївхЙлЕуЁЃ
(2)ЭЈЙ§ЖдбѕЛЏЛЙдетвЛЖдЕфаЭУЌЖмЕФбЇЯАЃЌИаЮђЁАЖдСЂЭГвЛЁБЕФБчжЄЮЈЮяжївхЙлЕуЁЃ
2.Й§ГЬгыЗНЗЈ
(1)ЭЈЙ§ЗжЮібѕЛЏЛЙддРэЃЌОРњДгЁАЕУбѕгыЪЇбѕЁБЕНЁАЛЏКЯМлИФБфЁБЕНЁАЕчзгзЊвЦЁБЕФЗжЮіЙ§ГЬЃЌРэТлЬНОПЕФЛљБОЗНЗЈЃЛОРњЬсСЖИХФюЕФЙ§ГЬЃЌШЯЪЖзМШЗЁЂОЋСЖЕиУшЪіИХФюЁЂЩюПЬРэНтИХФюЁЂБШНЯБцЮіИХФюЕФЗНЗЈЁЃ
(2)УїАзЁАБэЯѓ(ЛЏКЯМлБфЛЏ)ЁБгыЁАБОжЪ(ЕчзгзЊвЦ)ЁБжЎМфЕФЙиЯЕЃЌФмДгБОжЪЩЯУшЪіВЂБэДявЛИібѕЛЏЛЙдЗДгІЁЃУїАзЁАЕчзгзЊвЦЁБВХЪЧЮяжЪМфЗЂЩњбѕЛЏЛЙдЗДгІЕФБОжЪвђЫиЁЃ
1.жЊЪЖгыММФм
(1)РэНтбѕЛЏЛЙдЗДгІЕФЪЕжЪЪЧЕчзгЕФзЊвЦЃЌРэНтдЊЫиЛЏКЯМлЩ§НЕгыбѕЛЏЛЙдЗДгІЁЂЕчзгЕУЪЇЕФЙиЯЕЁЃбЇЛсбѕЛЏЛЙдЗДгІЕФХаЖЯвдМАгУЛЏКЯМлЩ§НЕЛђЕчзгзЊвЦРДЗжЮібѕЛЏЛЙдЗДгІЁЃ
(2)бЇЛсгУЫЋЯпЧХКЭЕЅЯпЧХБэЪОбѕЛЏЛЙдЗДгІжаЕчзгЕФзЊвЦЁЃРэНтЫФжжЛљБОЗДгІРраЭгыбѕЛЏЛЙдЗДгІЕФЙиЯЕЁЃ
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com