
28.[有机化学基础]
(1)迷失香酸是从蜂花属植物中提取得到的酸性物质,其结构如图。请回答下列问题
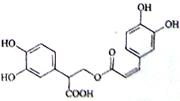 ①迷失香酸中含氧官能团的名称是
①迷失香酸中含氧官能团的名称是
______、______、__________。
②一定条件下,1mol迷失香酸最多能和
__________mol氢气发生加成反应
③一定条件下,迷失香酸可能发生的反应类型有______________。(填序号)
a.水解反应 b.取代反应 c.加成反应 d.消去反应
④迷失香酸的分子式为______________________________________。
⑤1mol迷失香酸与足量NaOH溶液共热,最多消耗NaOH ___________________ mol。
 (2)氯乙烯是合成聚氯乙
(2)氯乙烯是合成聚氯乙
烯(PVC)的单位。乙烯氧
氯化法是生产氯乙烯的主要
方法。分三步进行(如图所
示)
①下列关于乙烯、氯乙烯和聚氯乙烯的说法中,正确的是_________(填字母)。
A.都能在氧气中燃烧 B.都能发生加成反应使溴水退色
C.都能使酸性高锰酸钾溶液退色 D.氯乙烯分子中所有原子处于同一平面
②根据上图所示,从环境保护的角度分析,氧氯化法的有点是_______________
③某学生设计了下列反应:
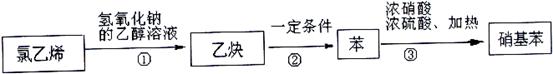
图中步骤①的反应类型为________________;
请写出图中步骤③的化学方程式___________________________________________。
④已知二氯乙烷与NaOH溶液共热可生成乙二醇(HO-CH2CH2-OH),请写出乙二醇与乙酸发生酯化反应的化学方程式______________________;该反应反应类型为_______
_____________。
⑤焚烧废旧塑料,造成大气污染。如聚氯乙烯在氧气中充分燃烧时可以排放二氧化碳、水和氯化氢,请写出其燃烧的化学方程式文____________________________________。
27.海水中蕴藏着丰富的资源。目前海水谈话的方法有冷冻法、电渗析和蒸馏。海水综合利用的流程图如下,请认真审题,回答以下问题:
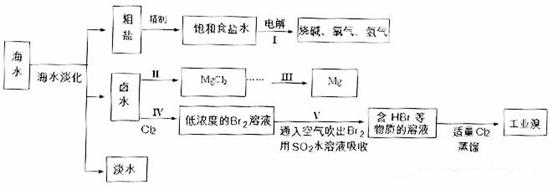
 (1)我校学生在实验室用右图装置模拟步骤I电解食盐水。
(1)我校学生在实验室用右图装置模拟步骤I电解食盐水。
(用铁和石墨做电极)
①a电极材料是_________(填铁、石墨):
阴极反应式为_______________。
②当阴极产生11.2mL气体时(标准状况),计算该溶液的pH
为__________;(忽略反应前后溶液体积的变化),用pH试纸测定
溶液pH的方法是_________________________________。
③检验阳极产生的气体的操作、现象和离子方程式
是__________________________。
④若将产生的氯气被生成的烧碱溶液完全吸收,可得“84消毒液”(若只含有一种溶质)该电解反应的化学方程式为_________________________________。
 (2)卤水中蕴含着丰富的镁资源,就MgCl2
(2)卤水中蕴含着丰富的镁资源,就MgCl2
粗产品的提纯,和冶炼镁的过程回答下列问题:
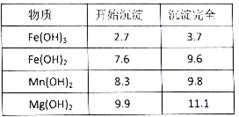
①已知MgCl2粗产品的溶液中含有Na+、Fe2+
、Fe3+和Mn2+,欲将Fe2+、Fe3+、Mn2+转化为Fe(
OH)3和Mn(OH)2沉淀除去(生成氢氧化物沉淀的
pH见表),控制溶液的pH为____________;将Fe2+转化为Fe3+最好选用的物是_________(填序号)。
a.Cl2 b.NaClO c.NaOH d.Fe
②步骤III中由MgCl2制得Mg的方法是_______________(用化学方程式表示)。
(3)卤水中还蕴含着丰富的溴资源。步骤IV中已获得Br2,步骤V中又用SO2水溶液吸收Br2,SO2将Br2还原为Br-时的吸收率可达95%,其目的是___________;离子方程式为________________。
26.乙醇的用途广泛,请根据乙醇的性质和用途回答下列相关问题:
(1)在常温常压下,lgC2H5OH燃烧生成CO2和液态H2O时放出29.71kJ热量,表示该反应的热化学方程式为________________________________________________。
(2)科学家研制了一种新型的乙醇电池。用酸性电解质(H+)作溶剂时的电池总反应为:
 ,随时蒸发生成的水,电解质溶液的PH值变化________(增大、减小、不变)。电池正极反应为___________________;电池负极反应为____________________。
,随时蒸发生成的水,电解质溶液的PH值变化________(增大、减小、不变)。电池正极反应为___________________;电池负极反应为____________________。
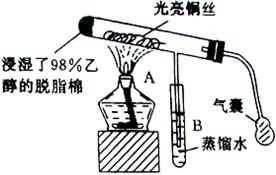 (3)“乙醇催化氧化”的实验装置如图所示:
(3)“乙醇催化氧化”的实验装置如图所示:
实验操作为:预先使棉花团浸透乙醇,并照图安装好
仪器,在铜丝的中间部位加热片刻后,用气囊有节奏
地鼓入空气,即可观察到以下明显的时间现象。
请回答以下问题:
①在实验过程中铜丝出现红色和黑色交替的现象,
说明在该实验过程中催化剂_______(参加/不参加)化
学反应;写出乙醇催化氧化过程的化学方程式______
______________,______________________。
②在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明乙醇催化氧化反应是_______________反应。
③B中蒸馏水收集到的物质可能有____________、___________(填物质的名称)欲验证B中得到的乙醇催化氧化的产物,可选择的试剂是________________(填序号)。
a.银氨溶液 b.重铭酸钾酸性溶液 c.溴水 d.氢氧化铜悬浊液
25.A-F六种元素中,除A外均为短周期元素,它们的原子结构或性质如表所示:
|
元素 |
结构或性质 |
|
A |
生活中常见的金属,它有两种氯化物,相对分子质量相差35.5 |
|
B |
二价阳离子与Ne原子具有相同的电子层结构 |
|
C |
形成化合物种类最多的元素之一,其单质为固体 |
|
D |
地壳中含量最多的元素 |
|
E |
与D同主族 |
|
F |
与E同周期,且最外层电子数等于电子层数 |
(1)A的某种氯化物的浓溶液可用于制作铜印刷电路板,反应的离子方程式:
______________________________________。
(2)CD2分子中化学键的类型是________________;固态CD2的用途是____________________________;能与上述某元素形成的物质发生置换反应的化学方程式是_________________________________________。
24. 如图所示,半径为R的光滑半圆环轨道与高为10R的光滑斜轨道放在同一竖直平面内,两轨道之间由一条光滑水平轨道CD相连,水平轨道与斜轨道间有一段圆弧过渡。在水平轨道上,轻质弹簧被
如图所示,半径为R的光滑半圆环轨道与高为10R的光滑斜轨道放在同一竖直平面内,两轨道之间由一条光滑水平轨道CD相连,水平轨道与斜轨道间有一段圆弧过渡。在水平轨道上,轻质弹簧被 、
、 两小球挤压,处于静止状态。同时释放两个小球,
两小球挤压,处于静止状态。同时释放两个小球, 球恰好能通过圆环轨道最高点
球恰好能通过圆环轨道最高点 ,
, 球恰好能到达斜轨道的最高点
球恰好能到达斜轨道的最高点 。已知
。已知 球质量为
球质量为 ,重力加速度为
,重力加速度为 。求:
。求:
(1) 球释放时的速度大小。
球释放时的速度大小。
(2) 球释放时的速度大小。
球释放时的速度大小。
(3)释放小球前弹簧的弹性势能。
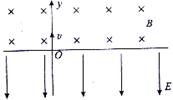
23.如图所示,在x轴上方有垂直于xy平面向里的匀强磁场,磁感应强度为B在x轴下方有沿y轴负方向的匀强电场,场强为E,一质量为m,电荷量为 的粒子从坐标原点
的粒子从坐标原点 沿着y轴正方向射出,射出之后,第三次到达
沿着y轴正方向射出,射出之后,第三次到达 轴时,它与点
轴时,它与点 的距离为
的距离为 ,
,
(1)画出粒子运动轨迹的示意图。
(2)求此粒子射出时的速度 和从射出到第三次到达
和从射出到第三次到达 轴,粒子运动的总时间。(重力不计)
轴,粒子运动的总时间。(重力不计)
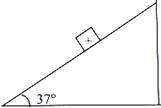
22.如图所示,一带电为 质量为
质量为 的小物快,处于一倾角为
的小物快,处于一倾角为 的光滑绝缘的固定鞋面上,当整个装置处于一水平方向的匀强电场中时,小物块恰好处于静止。若从某时刻起,只将电场强度大小减小为原来的一般,方向保持不变,求:
的光滑绝缘的固定鞋面上,当整个装置处于一水平方向的匀强电场中时,小物块恰好处于静止。若从某时刻起,只将电场强度大小减小为原来的一般,方向保持不变,求:
(1)原来电场强度的大小和方向。
(2)场强变化后,物块的加速度大小。
(3)场强变化后,物块下滑距离 时其电势能的变化。
时其电势能的变化。
(已自会 ,重力加速度为
,重力加速度为 )
)
21.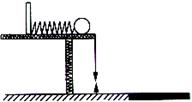 (1)为了测定一根轻弹簧压缩最短时储存的弹性势能的大小,可以将弹簧固定在光滑的凹槽的轨道一端,并将轨道固定在水平桌面的右边(如图所示),用钢球先将弹簧压缩至最短,而后突然释放,钢球将沿轨道飞出桌面,请回答以下问题:
(1)为了测定一根轻弹簧压缩最短时储存的弹性势能的大小,可以将弹簧固定在光滑的凹槽的轨道一端,并将轨道固定在水平桌面的右边(如图所示),用钢球先将弹簧压缩至最短,而后突然释放,钢球将沿轨道飞出桌面,请回答以下问题:
①为完成实验要求,除了钢球、弹簧、铅笔、复写纸、白纸、
铅垂线之外,还需要的器材有:____________________________。
②需要测定的物理量是______________________________。
③利用所测的物理量,计算弹簧最短时的性势能的表达式(已
知重力加速度为g)Ep=________________________。
(2)用金属制成的线材(如钢丝、钢筋)受到拉力会伸长,17世纪英国物理学家胡克发现,金属丝或金属杆在弹性限度内的伸长与拉力成正比,这就是著名的胡克定律,这个发现为后人对材料的研究奠定了重要的基础,现有一根用新材料制成的金属杆,长为4m,横截面积为0.8cm2,设计要求它受到拉力后的伸长不超过原长的1/1 000,由于这一拉力很大,杆又较长,直接测试有困难,就选用同种材料制成样品进行测试,通过测试取得数据如下:
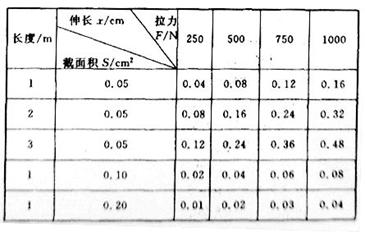
①根据测试结果,推导出线材伸长 与材料的长度
与材料的长度 、材料的横截面积
、材料的横截面积 及拉力
及拉力 的函数关系为______________。
的函数关系为______________。
②在寻找上述关系中,你运用那种科学研究方法?_____________。
③通过对样品的测试,求出新材料制成的金属细杆能承受的最大拉力约___________。
20.环型对撞机是研究高能粒子的重要装置,其核心部件是一个高真空的圆环状的空腔。若带电粒子初速可视为零,经电压为U的电场加速后,沿圆环切线方向注入对撞机的环状空腔内,空腔内存在着与圆环平面垂直的匀强磁场,磁感应强度大小为 。带电粒子将被局限在圆环状空腔内运动。要维持带电粒子在圆荒内做半径确定的圆周运动,下面的说法中正确的是(重力不计)
。带电粒子将被局限在圆环状空腔内运动。要维持带电粒子在圆荒内做半径确定的圆周运动,下面的说法中正确的是(重力不计)
A.对于给定的带电粒子,加速电压 越大,磁感应强度B越小
越大,磁感应强度B越小
B.对于给定的带电粒子,不管加速电压U多大,粒子运动的周期都不变
C.对于给定的加速电压,带电粒子的比荷q/m越大,磁感应强度B越大
D.对于给定的加速电压,带电粒子的比荷q/m越大,磁感应强度B越小
第II卷(非选择题 共180分)
本卷共10道题。
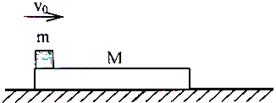
19.如图所示,质量为M的木板静置在光滑的水平面上,在M上放置一质量为m的物块,物块与木板的接触面粗糙。当物块 以初速度
以初速度 向右滑动时
向右滑动时
A.若使M固定不动,则m对M的摩擦力的冲量为零
B.不论M是否固定,m与M相互作用的冲量大小相等、方向相反
C.若M不固定,则m克服摩擦力做的功全部转化为内能
D.若M不固定,则m克服摩擦力做的功全部转化为木板M的动能
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com