
6.下列离子方程式正确的是 ( )
A.氢氧化钡溶液与硫酸溶液混合:
 ↓
↓
B.铁和稀硝酸反应: ↑
↑
C.将铜片放入氯化铁溶液中:
D.氯化铝溶液中加入过量氨水: ↓
↓
5.将足量的气体分别通入相应的溶液,下列实验一定可以得到沉淀的是 ( )
A.将SO2通入BaCl2溶液 B.将HCl通入NaAlO2溶液
C.将Cl2通入AgNO3溶液 D.将CO2通入Ca(OH)2溶液
4.下列有关化学反应过程或实验现象的叙述中,正确的是 ( )
A.氨气的水溶液可以导电,说明氨气是电解质
B.漂白粉和明矾都常用于自来水的处理,二者的作用原理是相同的
C.氯气可以使湿润的有色布条褪色,说明氯气具有漂白作用
D.在滴有酚酞的Na2CO3溶液中慢慢滴入BaCl2溶液,溶液的红色逐渐褪去
3.化学反应中通常伴随着能量变化,下列说法中错误的是 ( )
A.TNT(炸药)爆炸时将部分化学能转化为动能
B.电解熔融Al2O3时将部分化学能转化为电能
C.镁条燃烧时将部分化学能转化为光能
D.煤燃烧时将部分化学能转化为热能
2.难溶于水的非金属氧化物是 ( )
A.MnO2 B.CO2 C.NO2 D.SiO2
1.造成环境污染的主要原因是由于人类生产活动中过度排放有关物质。下列环境问题不是由所对应的物质引起的是 ( )
A.温室效应--二氧化碳 B.酸雨--二氧化硫
C.光化学烟雾--二氧化氮 D.臭氧层破坏--氧化碳
28.(8分)将3.2 g Cu溶于a mol/L过量的硝酸30 mL中,假设硝酸的还原产物只有NO和NO2,反应结束后,将所得溶液加水稀释至1000 Ml,测得c(NO3-)为0.2 mol/L。求:
(1)稀释后溶液中H+的物质的量浓度为 。
(2)生成的气体中NO2的物质的量为 ,NO的物质的量为 。(用含a的关系式表示)。
(3)用NaOH溶液吸收氮的氧化物是防止NOx污染的一种方法。原理为:
 2NO2+2NaOH=NaNO3+NaNO2+H2O
2NO2+2NaOH=NaNO3+NaNO2+H2O
NO2+NO+2NaOH=2NaNO2+H2O
若题中所述生成的混合气体能被NaOH溶液完全吸收,则a的取值范围为
。
27.(12分)
某化学兴趣小组采用下列方法测定Na2SO3样品中Na2SO4的质量分数。
[方法一]加热转化法
称取a g样品,置于硬质玻璃管中,通入足量的氧气加热到质量不再改变。
若冷却后称得固体质量为b g,则样品中Na2SO4质量分数为
[方法二]测SO2质量法
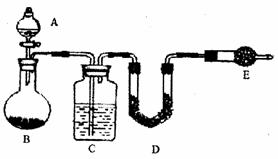
采用如图所示装置,通过实验测定生成SO2的质量。
(1)C中所装药品为 ;D中所装药品为 。
(2)E装置的作用为 。
[方法三]测沉淀质量法
第一步:称取e g样品,置于小烧杯中;
第二步:向小烧杯中加入足量稀盐酸,充分反应后加热;
第三步:向小烧杯中加入足量BaCl2溶液,然后过滤、洗涤:
第四步:干燥沉淀,称重为f g。
(1)第二步中加热的目的是 。
(2)简述洗涤沉淀的方法: 。
26.(12分)
某兴趣小组探究SO2气体的性质,他们使用的药品和装置如下图所示:
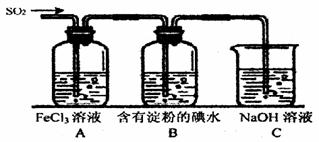
(1)SO2气体与Fe3+反应的还原产物是 (填离子符号),参加反应的SO2和Fe3+的物质的量之比是 。
(2)下列实验方案适用于在实验室制取所需SO2的是 (填序号)。
A.Na2SO3溶液与HNO3
B.Na2SO3浓溶液与浓硫酸
C.固体硫在纯氧中燃烧
(3)装置C的作用是 。
(4)若要从A中所得溶液提取晶体,必须进行的实验操作步骤:蒸发、冷却结晶、 、自然干燥,在这一系列操作中没有用到的仪器有 (填序号)。
A.蒸发皿 B.石棉网 C.漏斗 D.玻璃棒
(5)在上述装置中通入过量的SO2,为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入酸性KMnO4溶液,紫色褪去
方案②:往第二份试液中加入KSCN溶液不变红,再加入新制的氯水,溶液变红,
方案③:往第三份试液中加入用盐酸酸化的BaCl2溶液,产生白色沉淀
上述方案不合理的是 ,原因是 。
(6)能表明I一的还原性弱于SO2的现象是 。
25.(13分)
下图为各单质与化合物之间的转化关系,单质及化合物的组成元素均为常见的短周期元素。请回答:
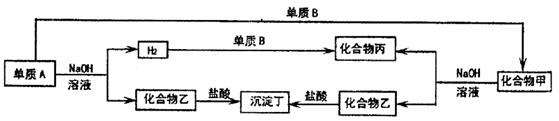
(1)若沉淀丁不溶于过量的盐酸,甲为 ,乙为 。
若沉淀丁能溶于过量的盐酸,丁为 。
(2)单质B的化学式为 ,丙的电子式为 。
(3)若沉淀丁不溶于过量的盐酸,写出A和NaOH溶液反应的化学方程式:
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com