
5.影响古希腊政治文明产生的相关因素中,最重要的客观条件是 ( )
A.古希腊的地理环境 B.东方文明的影响
C.发达的工商业经济 D.积极的殖民活动
4.1980年,日本北海道大学学者中野美代子首次提出“孙悟空护送唐僧西天取经”传说源于福建,后来有许多资料证明孙悟空的原型可能源自福建顺昌。下列选项中最能支持这一观点的是 ( )
A.顺昌宝山有与孙悟空相关的自然景观及民间传说
B.顺昌发现始建于元末明初的孙悟空兄弟合葬神墓
C.元代建阳出版了《西游记》雏形的《西游记平话》
D.顺昌民俗学者认为,孙悟空是我们福建顺昌县人
3.据《东京梦华录》记载:“中秋夜,贵家结饰台榭,民间争占酒楼玩月。”材料描绘的情景应该发生在今天的 ( )
A.南京 B.日本 C.开封 D.杭州
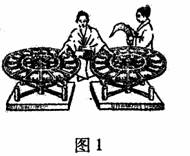
2.图l所示的技术发明,其积极作用在于 ( )
A.加速了造纸技术的改进
B.加快了纺纱捻线的速度
C.能够迅速测定地理方位
D.提高了印刷排版的效率
1.对以下八位帝王称号归类正确的是 ( )
A.谥号:周武王、隋文帝
 B.庙号:唐太宗、永乐帝
B.庙号:唐太宗、永乐帝
C.尊号:商纣王、秦始皇
D.年号:汉武帝、康熙帝
20.(15分)某课外小组利用H2还原黄色的WO3粉末测定W元素的相对原子质量,下图是测量装置的示意图,A中的试剂是盐酸。
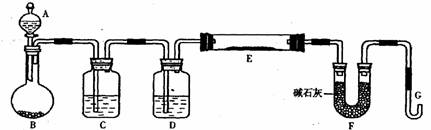
请回答下列问题:
(1)烧瓶中装入的试剂是锌粒,其中将发生反应的离子方程式是 ;
(2)试剂C是水,其作用是 ;
(3)试剂D是 ,其作用是干燥氢气;
(4)连接好装置后的实验操作依次是 (填操作序号)
①检验氢气纯度
②加热E
③检验装置气密性
④点燃G管溢出的气体
⑤从A瓶逐滴滴加液体
(5)从实验中测得了下列数据
①空E管的质量 ;
;
②E管和WO3的总质量 ;
;
③反应后E管和W粉的总质量 (冷却到温室称量);
(冷却到温室称量);
④反应前F管及内盛物的总质量 ;
;
⑤反应后F管及内盛物的总质量 ;
;
由以上数据可以列出计算W的相对原子质量的两个不同计算式(除W外,其他涉及的元素的相对原子质量均为已知):
计算1:Ar(W)= ;
计算2:Ar(W)= 。
19.(18分)氨在国民经济中占有重要的地位,2008年,我国氨产量接近500万吨。下图是合成氨的简要流程。
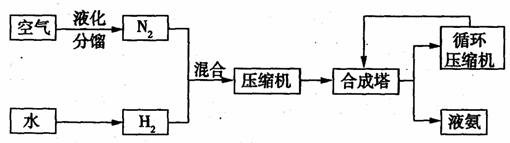
(1)下表是空气中部分气体的沸点。将空气液化加热分馏,依据下表数据判断,最先气化得到的气体是 。
|
气体名称 |
氨气 |
氧气 |
氦气 |
氖气 |
氩气 |
氪气 |
氚气 |
|
沸点/℃ |
-196 |
-183 |
-269 |
-264 |
-186 |
-153 |
-108 |
(2)天然气、重油、煤都可以与水反应制得氢气。下表是某合成氨厂采用不同原料的相对投资和能量消耗。
|
原料 |
天然气 |
重油 |
煤 |
|
相对投资费用 |
1.0 |
1.5 |
2.0 |
|
能量消耗/J·t-1 |
28 109 109 |
38 109 109 |
48 109 109 |
①依据上表信息,你认为采用 为原料最好。
②请写出甲烷在高温、催化剂的作用下与水蒸气反应生成氢气和一氧化碳的化学方程式: 。
③已知C(s)、CO(g)和H2(g)完全燃烧的热化学方程式分别为:
C(s)+O2(g)===CO2(g) △H=-394kJ·mol-1;
2CO(g)+O2(g)===2CO2(g)△H=-566kJ·mol-1;
2H2(g)+O2(g)===2H2O(g) △H=-484 kJ·mol-1;
试写出由C于水蒸气在高温条件下反应生成氢气与一氧化碳的热化学方程式
。
(3)下表是在某种催化剂作用下用体积比为1:3的氮、氢混合气反应应达到平衡时的一些实验数据。

|
0.1 |
10 |
20 |
30 |
60 |
100 |
||||||
|
200 |
15.3 |
81.5 |
86.4 |
89.9 |
95.4 |
98.8 |
||||||
|
300 |
2.2 |
52.0 |
64.2 |
71.0 |
84.2 |
92.6 |
||||||
|
400 |
0.4 |
25.1 |
38.2 |
47.0 |
65.2 |
79.8 |
||||||
|
500 |
0.1 |
10.6 |
19.1 |
26.4 |
42.2 |
57.5 |
||||||
|
600 |
0.05 |
4.5 |
9.1 |
13.8 |
23.1 |
31.4 |
|
|
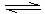 NH3的△H (填“>”、“<”或“无法判断”
NH3的△H (填“>”、“<”或“无法判断” 0,请简要说明理由
;
0,请简要说明理由
;
②该反应的化学平衡常数表达式为 。
③在300℃、10MPa下,合成氨反应达到平衡时,混合气体的体积是反应开始时的
倍。
18.(12分)有X、Y、Z、W四种短周期主族元素,原子序数依次增大。X元素与其它元素不在同一周期。Y、Z在同周期表中处于相邻位置,它们的单质在通常状况下均为无色气体。W原子的最外层电子数是核外电子层数的2倍。请回答:
(1)W在元素周期表位置 。
(2)写出X与Z形成的10电子阳离子的化学式 。
(3)由上述四种元素中的某两种元素所形成的具有漂白作用的物质的化学式是:
(任意写一种)。
(4)W的最高价氧化物的水化物有强氧化性,加热时金属铜可被它氧化,该反应的化学方程式为 。
(5)由X、Y、Z、W四种元素组成的多种无机酸酸式盐,写出其中一种与足量的NaOH溶液在加热条件下反应的离子方程式为: 。
17.(6分)工业上冶炼铝的原料是铝土矿(主要成份为Al2O3,杂质为Fe2O3、SiO2等)。某研究小组设计的提纯Al2O3的方案如下:

(1)写出X、Y的化学式:X ,Y ;
(2)通入过量CO2时反应的离子方程式为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com