
24. (6分)在6份0.01mol/L氨水中分别加入下列各物质:A.浓氨水 B.纯水 C.少量K2CO3 D.少量浓H2SO4 E.少量NaOH固体 F.少量Al2(SO4)3固体
(1)能使[OH-]减小、[NH4+]增大的是____(2)能使[OH-]增大、[NH4+]减小的是______
(3)能使[OH-]和[NH4+]都增大的是________
(4)能使[OH-]和[NH4+]都减小的是_______
23、(9分)常温下,将0.01molNH4Cl和0.002molNaOH溶于水配成1L溶液,
(1)该溶液中存在的三个平衡体系是____________________________________、
_____________________、__________________________________。
(2)溶液中共有 种不同的粒子。
(3)这些粒子中浓度为0.01mol/L的是
浓度为0.002mol/L的是 。
(4)物质的量之和为0.01mol的二种粒子是
_______________________________________。
(5) 和 两种粒子数量之和比OH-多0.008mol
22. (4分)物质的量浓度相同的 ① 氨水 ② 氯化铵 ③ 碳酸氢铵 ④ 硫酸氢铵 ⑤ 硫酸铵五种溶液中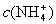 大小的顺序是__________________,溶液pH大小的顺序是__________________。
大小的顺序是__________________,溶液pH大小的顺序是__________________。
21、(6分)下列盐溶液能发生水解的用离子方程式表示,不能发生水解的写“不发生水解”字样,并说明溶液的酸碱性
K 2CO3 , 溶液呈 性;
Na2SO4 , 溶液呈 性;
CuCl2 , 溶液呈 性。
23、下列各组溶液,不用其它试剂,无法将它们区别开的是( )。
A.HCl、CuSO4、Mg(NO3)2、KOH B.NaBr、AgNO3、HCl、Na2CO3
C.H2SO4、NaCl、Na2SO4、Na2CO3 D.NaOH、MgSO4、Na2CO3、KHSO4
22.室温下,下列难溶化合物所形成的饱和溶液的物质的量浓度最大的是( )
A.CaCO3(Ksp=5.0×10-9) B.PbSO4(Ksp=2.53×10-8)
C.CuCl (Ksp=1.72×10-7) D.BaSO4(Ksp=1.1×10-10)
21.Fe2S3的溶度积表达式是( )
A.Ksp=c(Fe3+)·c(S2-) B.Ksp=c(Fe23+)·c(S32-)
C.Ksp=c2 (Fe3+)·c3 (S2-) D.Ksp=[2c (Fe3+)]2·[3c (S2-)] 3
20、为了配制NH4+的浓度与Cl-的浓度比为1:1的溶液,可在NH4Cl溶液中加入:
①适量的HCl;②适量的NaCl;③适量的氨水;④NaOH
A.①② B.③ C.③④ D.④
19、某酸碱指示剂(HIn)在水溶液中存在以下平衡:
HIn(aq) 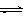 H+ +
In-(aq)
H+ +
In-(aq)
(红色) (蓝色)
下列物质的溶液中,能使指示剂显蓝色的是( )
A.稀硫酸 B.氯化铝溶液 C.稀氨水 D.饱和食盐水
18、向CH3COOH CH3COO- + H+ 的平衡体系中,加入下列物质能使醋酸的电离
程度和溶液的pH都变小的是( )
A .H2O B. CH3COONa C. NH3·H2O D. H2SO4
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com