
34. вбжЊЃКCH3CH2CH2CH3(g)+  O2(g)= 4CO2(g)+
5H2O(l) ІЄІЇ = -2878
kJЁЄmol-1
O2(g)= 4CO2(g)+
5H2O(l) ІЄІЇ = -2878
kJЁЄmol-1
(CH3)2CHCH3(g)+  O2(g)= 4CO2(g)+
5H2O(l) ІЄІЇ = -2869
kJЁЄmol-1
O2(g)= 4CO2(g)+
5H2O(l) ІЄІЇ = -2869
kJЁЄmol-1
ЯТСаЫЕЗЈе§ШЗЕФЪЧ( ЁЁ )
A. е§ЖЁЭщзЊЛЏЮЊвьЖЁЭщЕФЙ§ГЬЪЧвЛИіЮќШШЙ§ГЬ
B. е§ЖЁЭщЗжзгДЂДцЕФФмСПДѓгквьЖЁЭщЗжзг
C. е§ЖЁЭщЕФЮШЖЈадДѓгквьЖЁЭщ
D. е§ЖЁЭщЗжзгжаЕФЬМЧтМќБШвьЖЁЭщЕФЩй
33. гвЭМЪЧФГСђЫсЪдМСЕФБъЧЉЩЯЕФВПЗжФкШнЁЃОнДЫЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧ
A. ИУСђЫсгыЕШЬхЛ§ЫЎЛьКЯЫљЕУШмвКЕФЮяжЪЕФСПХЈЖШЕШгк9.2 molЁЄL-1
B. 1 molZnгызуСПЕФИУСђЫсЗДгІВњЩњ2 gЧтЦј
C. ИУСђЫсдкГЃЮТЯТПЩбИЫйгыЭЦЌЗДгІЗХГіЖўбѕЛЏСђЦјЬх
D. ХфжЦ200 mL2.30 molЁЄL-1ЕФЯЁСђЫсашСПШЁИУСђЫс25.00 mL
32. ЯТСаа№Ъіе§ШЗЕФЪЧ( ЁЁ )
A. 95 ЁцЪБДПЫЎЕФpHЃМ7ЃЌЫЕУїМгШШПЩЕМжТЫЎГЪЫсад
B. pH = 3ЕФДзЫсШмвКЃЌЯЁЪЭжС10БЖКѓpH = 4
C. 0.2 molЁЄL-1ЕФбЮЫсгыЕШЬхЛ§ЫЎЛьКЯКѓpH = 1
|
31. ХаЖЯЯТСагаЙиЛЏбЇЛљБОИХФюЕФвРОне§ШЗЕФЪЧ( ЁЁ )
A. ЙВМлЛЏКЯЮяЃКЪЧЗёКЌгаЙВМлМќЁЁЁЁЁЁЁЁЁЁЁЁЁЁ B. ЧПШѕЕчНтжЪЃКШмвКЕФЕМЕчФмСІЕФДѓаЁ
C. ЫсадШмвКЃКpHЃМ7ЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁD. бѕЛЏЛЙдЗДгІЃКдЊЫиЛЏКЯМлЪЧЗёБфЛЏ
30ЃЎШчЯТЭМЃЌдквЛЖЈЮТЖШЯТЃЌЂёЮЊКубЙУмБеШнЦї,ЂђЮЊКуШнУмБеШнЦїЁЃдкЂёЁЂЂђжаЗжБ№МгШы2 mol AКЭ2 mol B,Ц№ЪМЪБШнЦїЬхЛ§ОљЮЊV L,ЗЂЩњШчЯТЗДгІВЂДяЕНЛЏбЇЦНКтзДЬЌЃК 2AЪЎB xC(g)ЃЌЦНКтЪБСНШнЦїжаAЁЂBЁЂCЕФЮяжЪЕФСПжЎБШОљЮЊ1ЃК3ЃК6ЁЃЯТСаЫЕЗЈвЛЖЈе§ШЗЕФЪЧ( ЁЁ )
xC(g)ЃЌЦНКтЪБСНШнЦїжаAЁЂBЁЂCЕФЮяжЪЕФСПжЎБШОљЮЊ1ЃК3ЃК6ЁЃЯТСаЫЕЗЈвЛЖЈе§ШЗЕФЪЧ( ЁЁ )
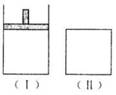
AЃЎxЕФжЕЮЊ2ЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁ
BЃЎBЮяжЪПЩЮЊЙЬЬхЛђвКЬх
CЃЎЂёЁЂЂђШнЦїжаДгЦ№ЪМЕНЦНКтЫљашЪБМфЯрЭЌЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁ
DЃЎЦНКтЪБЃЌЂёШнЦїЕФЬхЛ§аЁгкV L
29ЃЎ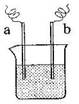 гвЭМжаЃЌСНЕчМЋЩЯЗЂЩњЕФЕчМЋЗДгІЮЊЃК
гвЭМжаЃЌСНЕчМЋЩЯЗЂЩњЕФЕчМЋЗДгІЮЊЃК
aМЋЃКCu2+ + 2 eЃ= CuЁЁЁЁЁЁ bМЋЃКFe - 2 eЃ= Fe2+
ЯТСаЫЕЗЈжаВЛе§ШЗЕФЪЧ(ЁЁ )
AЃЎИУзАжУПЩФмЪЧЕчНтГи
BЃЎaМЋЩЯвЛЖЈЗЂЩњЛЙдЗДгІ
CЃЎaЁЂbПЩФмЪЧЭЌжжЕчМЋВФСЯ
DЃЎИУЙ§ГЬжаФмСПЕФзЊЛЛвЛЖЈЪЧЛЏбЇФмзЊЛЏЮЊЕчФм
28ЃЎЕўЕЊЫс(HN3)гыДзЫсЫсадЯрЫЦЃЌЯТСаа№ЪіжаДэЮѓЕФЪЧ(ЁЁ)
AЃЎHN3ЫЎШмвКжаЮЂСЃХЈЖШДѓаЁЫГађЮЊЃКc(HN3)ЃОc(H+)ЃОc(N3¯)ЃОc(OH¯)
BЃЎHN3гыNH3зїгУЩњГЩЕФЕўЕЊЫсяЇЪЧЙВМлЛЏКЯЮя
CЃЎNaN3ЫЎШмвКжаРызгХЈЖШДѓаЁЫГађЮЊЃКc(Na+)ЃОc(N3¯)ЃОc(OH¯)ЃОc(H+)
DЃЎN3¯гыCO2КЌЯрЕШЕчзгЪ§
27ЃЎгУЖшадЕчМЋЕчНтСђЫсЭКЭбЮЫсЕФЛьКЯШмвКЃЌЕчНтвЛЖЮЪБМфКѓЭЃжЙЭЈЕчЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧ(ЁЁ)
AЃЎвѕМЋжЪСПвЛЖЈдіМг
BЃЎЭЈЕчЪБЕчзгДгвѕМЋОЭтЕчТЗСїШыбєМЋ
CЃЎЯрЭЌЬѕМўЯТЃЌбєМЋВњЩњЕФЦјЬхЕФЬхЛ§вЛЖЈБШвѕМЋДѓ
DЃЎЯрЭЌЬѕМўЯТЃЌбєМЋВњЩњЕФЦјЬхЕФЬхЛ§вЛЖЈБШвѕМЋаЁ
26ЃЎдкЯТСаЪЕбщжаЃЌВЛФмДяЕНФПЕФЕФЪЧ(ЁЁЁЁ )
AЃЎгУН№ЪєФЦЗжБ№гыЫЎКЭввДМЗДгІЃЌШЗЖЈЫЎКЭввДМЗжзгжаєЧЛљЧт(-OH)ЕФЛюЦУадЧПШѕ
BЃЎгУЪЏФЋзіЕчМЋЃЌЕчНтMg(NO3)2ЁЂCu(NO3)2ЕФЛьКЯШмвКЃЌШЗЖЈЭКЭУОЕФН№ЪєЛюЖЏадЧПШѕ
CЃЎНјааH2OКЭH2SЕФШШЗжНтЪЕбщЃЌШЗЖЈСђКЭбѕСНжждЊЫиЕФЗЧН№ЪєадЧПШѕ
DЃЎИљОнNa2CO3КЭNa2SO3ЫЎШмвКЫсМюадЧПШѕЃЌШЗЖЈЬМКЭСђСНдЊЫиЗЧН№ЪєадЕФЧПШѕ
24ЃЎбЧТШЫсФЦ(NaClO2)ПЩзіЦЏАзМСЃЌдкГЃЮТЯТВЛМћЙтЪБПЩБЃДцвЛФъЃЌЕЋдкЫсадШмвКжавђЩњГЩбЧТШЫсЖјЗЂЩњЗжНтЃК5HClO2===4ClO2Ёќ+H++Cl-+2H2OЃЌЗжНтЪБЃЌИеМгШыСђЫсЗДгІЛКТ§ЃЌЫцКѓЭЛШЛЗДгІЪЭЗХГіClO2ЃЌетЪЧвђЮЊ(ЁЁЁЁ )
AЃЎЫсЪЙбЧТШЫсЕФбѕЛЏаддіЧПЁЁЁЁЁЁ BЃЎШмвКжаЕФH+Ц№ДпЛЏзїгУ
CЃЎШмвКжаЕФCl-Ц№ДпЛЏзїгУЁЁ ЁЁЁЁЁЁDЃЎвнГіЕФClO2ЪЙЩњГЩЮяХЈЖШНЕЕЭ
|
AЃЎK+ХЈЖШМѕаЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁ BЃЎKMnO4дкбєМЋЧјЩњГЩ
CЃЎвѕМЋжмЮЇШмвКЕФpHжЕМѕаЁЁЁЁЁ ЁЁЁЁ DЃЎЗДгІЙ§ГЬжаЙВзЊвЦ0.005molЕчзг
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com