
16、氯只有35Cl和37Cl两各稳定同位素,它们在氯气中的原子数之比35Cl︰37Cl为3︰1。则分子量为70、72、74的氯气分子数之比可能是
A、5︰2︰1 B、5︰2︰2 C、9︰3︰1 D、9︰3︰2
15、下列变化规律中正确的是
A、H2S、HCl、PH3热稳定性由弱到强
B、物质的量浓度相等的NaCl、MgCl2、AlCl3三种溶液的pH值由小到大
C、等质量的甲烷、乙稀、乙炔充分燃烧,所耗用氧气的量由多到少
D、CH3CH2OH、?C6H5OH、CH3COOH的酸性由弱到强
14、 对于反应2SO2
+ O2
2SO3,下列判断错误的是
对于反应2SO2
+ O2
2SO3,下列判断错误的是
A、2体积2SO2和足量O2反应,必定生成2体积SO3
B、其他条件不变,增大压强,平衡必定向右移动
C、平衡时,SO2消耗速度必定等于O2生成速度的两倍
D、单位时间内每生成1molSO2,同时消耗1.5molO2,则反应必逆向进行。
13、对下列事实的解释错误的是
A、在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有吸水性
B、浓硝酸在光照下颜色变黄,说明浓硝酸不稳定
C、常温下,浓硝酸可以用铝缸贮存,说明铝与浓硝酸不反应
D、反应CuSO4+H2S = CuS↓+H2SO4能进行,说明硫化铜既不溶于水也不溶于稀硫酸
12、等物质的量浓度的下列溶液中,NH4+离子的浓度最大的是
A、NH4Cl B、NH4HCO3 C、NH4HSO4 D、NH4NO3
11、下列各组离子在溶液中能大量共存的是
A、Ca2+ 、HCO3-、Cl-、K+ B、Al3+、AlO2-、HCO3-、Na+
C、Fe2+、NH4+、SO42-、S2- D、Fe3+、SCN-、Na+、CO32-
10、 水的电离过程为H2O? H++OH-,在不同温度下其离子积为Kw(25℃)=1.0×10-14,Kw(35℃)
水的电离过程为H2O? H++OH-,在不同温度下其离子积为Kw(25℃)=1.0×10-14,Kw(35℃)
=2.25×10-14。则下列叙述正确的是
A、C(H+)随着温度升高而降低 B、在35℃时,C(H+)>C(OH-)
C、35℃时食盐水中[H+]为1.5×10-7mol/L D、水的电离是吸热的
9、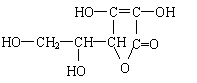 维生素C的结构简式为 ,有关它的叙述错误的是
维生素C的结构简式为 ,有关它的叙述错误的是
A、是一个环状的酯类化合物 B、易起氧化及加成反应
C、可以溶解于水 D、在碱性溶液中能稳定地存在
22、某温度下,甲、乙两个烧杯中各盛有100g相同浓度的KCl溶液,现将甲杯蒸发35g水,析出晶体5g;乙烧杯蒸发45g水,析出晶体10g。则原溶液需蒸发多少克水才恰好达到饱和?
A、10g B、15g C、20g D、25g
21、下列说法中正确的是
A、1mol稀硫酸和1mol稀Ba(OH)2溶液完全中和所放出的热量为中和热。
B、中和反应都是放热反应,盐类水解反应都是吸热反应。
C、在101kPa时,1mol碳燃烧所放出的热量一定是碳的燃烧热。
D、碳与二氧化碳的反应既是吸热反应,也是化合反应。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com