
2.太平天国运动遇到了历史上不曾有过的新情况是指
A.内部变乱导致分裂 B.军队与地方武装的联合围剿
C.中外反动势力的联合绞杀 D.敌人的长期封锁
1.举世闻名的皇家园林圆明园首次被洗劫并焚毁是在
A.第一次鸦片战争期间 B.第二次鸦片战争期间
C.甲午中日战争期间 D.八国联军侵华战争期间
33.将12.4gNa和Na2O2固体混合物加入89.4g水中,充分反应后,把生成的所有气体收集在另外一个密闭容器中,用电火花点燃,恰好完全反应,求:
①原混合物中Na和Na2O2的物质的量各为多少?
②所得NaOH溶液中溶质的质量分数为?
③若将所得NaOH溶液加水稀释至体积为10L后溶液中溶质的物质的量浓度?


32.(10分)实验室用浓盐酸配制250mL0.2 mol/L的盐酸溶液:
(1)配制250mL 0.2 mol/L盐酸溶液,需要浓盐酸(密度为1.18g/mL,质量分数为36.5%)的体积为___________mL(小数点后保留l位)。
(2)配制时,其正确的操作顺序是_________________________________(字母表示,每
个字母只能用一次)。
A、用30mL水洗涤烧杯2-3次,洗涤液均注入窬量瓶,振荡
B、用量筒摄取所需的浓盐酸,沿玻璃棒倒入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其混合均匀
C、将已冷却的盐酸沿玻璃棒注入250mL的容量瓶中
D、将容量瓶盖紧,振荡,摇匀
E、改用胶头滴管加水,使溶液凹面恰好与刻度相切
F、继续往容量瓶内小心加水,直到液面接近刻度2-3cm处
(3)若实验中出现下列情况,对所配溶液浓度有什么影响?(填“偏高”、“偏低”或“无
影响”)
①操作A中,没有将洗涤液都转移入容量瓶,会使溶液的浓度_________。
②操作E中定容时俯视刻度线,会使溶液的浓度________。
③操作D中将容量瓶盖紧,振荡,摇匀、静置后发现凹面低于刻度线又加水至刻度线,会使溶液的浓度_________。
④操作C中,所用容量瓶中已有少量蒸馏水,则结果_________。
31.(12分)某校化学兴趣小组用浓盐酸与二氧化锰加热反应,制取并收集2瓶干燥、纯净的氯气,为防止换集气瓶时生成的氯气污染空气,设计了如下装置:
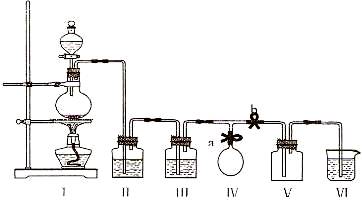
(1)写山装置I烧瓶中发生反应的化学方程式____________________________。
(2)装置II中盛放的药品是饱和氯化钠溶液,其作用是___________________________
___________;装置III的作用是干燥氯气,应盛放_________。装置VI中盛放的药品是氢氧化钠溶液,其作用是______________________________。
(3)实验开始后,先______a_______b(填“关闭”或“打开”,下同):当收集满一瓶氯
气时,为减少换集气瓶时氯气的外溢,再______a_____b),换好集气瓶后,继续收集氯气。
30.(10分)有一包固体粉末,其中可能含有Na2CO3、NaCl、KeSO4、CuCl2、BaCl2、K2CO3、Na2SO4、NaBr。现按下列步骤进行实验,现象如下:
①将固体溶于水得无色溶液和白色沉淀,过滤:
②在①滤出的沉淀中加入足量稀硝酸,有部分沉淀溶解,同时有无色气体放出。。
③取①的滤液做焰色反应,火焰呈黄色,隔着蓝色钴玻璃观察未见紫色,再向①的滤液中通入氯气,溶液由无色变为红棕色。试填写下列空白:
(1)混合物中一定含有______________________________________________,一定不含
有_______________________,可能含有___________________________________。
(2)步骤②发生反应的离子方程式_________________________________________。
29.(8分)现有A、B、C、D、E、F、G、H、M九种物质,其中A、B、C均为氧化物,且A为淡黄色粉末,G、E为气体单质且G为黄绿色,F的水溶液与石灰水混合可制得D的溶液。它们之间相互转化的关系如下图,其他与题无关的生成物均已略去。请同答下列问题:
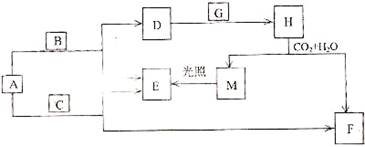
(1)丐出化学式:A________、E________、H________、M________。
(2)写出A+B-→D+E反应的化学方程式:________________________________。
(3)写H-→M+F的离子方程式___________________________________________。
28.(3分)工业上将氯气通入石灰乳 制取漂白粉,写出反应的化学方群式,并用双线桥标出电子转移的方向和数目:
制取漂白粉,写出反应的化学方群式,并用双线桥标出电子转移的方向和数目:
___________________________________________。
27.(3分)电质硫有强碱共热发生如下反应: ,在此反应中,被氧化的元素是_________。被还原的元素是________,氧化剂与还原剂的质量比是________。
,在此反应中,被氧化的元素是_________。被还原的元素是________,氧化剂与还原剂的质量比是________。
26.(2分)在标准状况下, L NH3溶于6mL水中,得到密度为p g/cm3的氨水,则此氨水的物质的量浓度为________________________________mol/L。
L NH3溶于6mL水中,得到密度为p g/cm3的氨水,则此氨水的物质的量浓度为________________________________mol/L。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com