
6.下列各句中,没有语病的一句是
A.作为翻译工作者,一定要学好本民族语言也是很重要的。
B.为了实现现代,我国要有具有世界先进水平的一流的若干所大学。
C.在肇事的两个美国士兵被宣判无罪之后,汉城的一些餐馆拒绝向美国人提供服务。
D.近年来我国在对濒危动物的保护,虽然做了不少工作,但离要求还相差很远。
5.下列各句中,加点的词语使用不恰当的一句是
A.但有朝一日,那里的黑人男孩和女孩将能与白人男孩和女孩相敬如宾,携手并进。
B.由于剩余价值的发现,这里就豁然开朗了,而先前无论资产阶级经济学家或者社会主义批评家所做的一切研究都只是在黑暗中摸索。
C.树缝里也漏着一两点路灯光,没精打采的,是渴睡人的眼。
D.胡同文化是一种封闭的文化。住在胡同里的居民大都安土重迁,不大愿意搬家。
4.下列词语中没有错别字的一组是
A.斑驳 真谛 杀一儆百 丰华正茂
B.漫溯 恪守 光彩夺目 骇人听闻
C.熨帖 袅娜 不可思义 义奋填膺
D. 慰籍 宁谧 相形见拙 安之若诉
3.下列各组词语中,没有错别字的一组是( )
A.卓尔不群 出其不意 兵荒马乱 名副其实
B.毕恭毕敬 垂拱而治 世外桃源 题纲挈领
C.挥洒自如 剽窃成果 耳懦目染 揠苗助长
D.未竟事业 名门旺族 积重难返 座无虚席
2.下列词语中加点的字读音全都正确的一组是( )
A.蜕变(tuì) 粗糙(zào) 琐屑(xiè) 游目骋怀(chěng)
B.佝偻 (lǚ) 长篙(hāo) 踱步(dù) 凝神屏息(bǐng)
C.翌日(yì) 霎时(shà) 气馁(něi) 浅尝辄止(zhé)
D.羞涩(shè) 隽永(juàn) 侥幸(jiǎo) 脉脉含情(mài)
1、下列加点字读音全都正确的一项是( ) A.壬(rén)戌 窈窕(tiǎo) 桂棹(zhào) 冯(féng)虚御风 B.嫠(lí )妇 愀(qiǎo)然 舳(yóu)舻 山川相缪(liáo) C.酾(shī)酒 横槊(shuò) 江渚(zhǔ) 正襟(jīn)危坐 D.匏(páo)樽 枕藉(jí) 蜉(fú)蝣 一叶扁(piān)舟
24、(06年北京)铝和氢氧化钾都是重要的工业产品。请回答:
(1)工业冶炼铝的化学方程式是 。
 (2)铝与氢氧化钾反应的离子方程式是
。
(2)铝与氢氧化钾反应的离子方程式是
。
(3)工业品氢氧化钾的溶液中含有某些含氧酸根杂质,可用离子交换膜法电解提纯。电解槽内装
有阳离子交换膜(只允许阳离子通过),其工作原理如图所示。
①该电解槽的阳极反应式是 。
②通电开始后,阴极附近溶液pH会增大,请简述原因
③除去杂质后氢氧化钾溶液从液体出口 (填写“A”或“B”)导出。
① 4OH?? 4e? = 2H2O + O2↑② H+放电,促进水的电离,OH?浓度增大③ B
23. (09天津)(14分)氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
(09天津)(14分)氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
 (1)氢氧燃料电池的能量转化主要形式是 ,在导线中电子流动方向为
(用a、b表示)。
(1)氢氧燃料电池的能量转化主要形式是 ,在导线中电子流动方向为
(用a、b表示)。

 (2)负极反应式为
。
(2)负极反应式为
。
 (3)电极表面镀铂粉的原因为
。
(3)电极表面镀铂粉的原因为
。
 (4)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能。因此,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
(4)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能。因此,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
 Ⅰ.2Li+H2
Ⅰ.2Li+H2
 2LiH
2LiH Ⅱ.LiH+H2O==LiOH+H2↑
Ⅱ.LiH+H2O==LiOH+H2↑
 ①反应Ⅰ中的还原剂是
,反应Ⅱ中的氧化剂是
。
①反应Ⅰ中的还原剂是
,反应Ⅱ中的氧化剂是
。
 ②已知LiH固体密度为0.82g/cm3。用锂吸收224L(标准状况)H2,生成的LiH体积与被吸收的H2体积比为
。
②已知LiH固体密度为0.82g/cm3。用锂吸收224L(标准状况)H2,生成的LiH体积与被吸收的H2体积比为
。
 ③由②生成的LiH与H2O作用,放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为
mol。
③由②生成的LiH与H2O作用,放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为
mol。
答案:(1)由化学能转化为电能 由a到b(2)2H2+4OH--4e-=4H2O或H2+2OH--2e-=2H2O
(3)增大电极单位面积吸附H2、O2分子数,加快电极反应速率(4)①Li H2O ②或8.71×10-4 ③32
22.(09海南) Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4-SOCl2。电池的总反应可表示为:4Li+2SOCl2 =4LiCl+S +SO2。
Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4-SOCl2。电池的总反应可表示为:4Li+2SOCl2 =4LiCl+S +SO2。 请回答下列问题:
请回答下列问题:
 (1)电池的负极材料为
,发生的电极反应为
;
(1)电池的负极材料为
,发生的电极反应为
;
 (2)电池正极发生的电极反应为
;
(2)电池正极发生的电极反应为
;
 (3)SOCl2易挥发,实验室中常用NaOH溶液吸收SOCl2,有Na2SO3和NaCl生成。 如果把少量水滴到SOCl2中,实验现象是
,反应的化学方程式为
;
(3)SOCl2易挥发,实验室中常用NaOH溶液吸收SOCl2,有Na2SO3和NaCl生成。 如果把少量水滴到SOCl2中,实验现象是
,反应的化学方程式为
;
 (4)组装该电池必须在无水、无氧的条件下进行,原因是
。
(4)组装该电池必须在无水、无氧的条件下进行,原因是
。
答案:: 


 (1)锂 Li-2e-=Li+(2分)
(1)锂 Li-2e-=Li+(2分)
 (2)2SOCl2+4e-=4Cl-+S+SO2(2分)
(2)2SOCl2+4e-=4Cl-+S+SO2(2分)
 (3)出现白雾,有刺激性气体生成 SOCl2+H2O=SO2↑+2HCl↑(3分)
(3)出现白雾,有刺激性气体生成 SOCl2+H2O=SO2↑+2HCl↑(3分)
 (4)锂是活泼金属,易与H2O、O2反应;SOCl2也可与水反应(2分)
(4)锂是活泼金属,易与H2O、O2反应;SOCl2也可与水反应(2分)
解析:分析反应的化合价变化,可得Li为还原剂 ,SOCl2为氧化剂。
(1)负极材料为Li(还原剂),Li – e- = Li+
(2)负极反应式可由总反应减去负极反应式得到:2SOCl2 + 4 e- = 4Cl- + S + SO2
(3)题中给出有碱液吸收时的产物,则没有碱液吸收时的产物应为SO2和HCl,所以现象应该为出现白雾和有刺激性气体生成。
(4)因为构成电池的两个主要成份Li能和氧气水反应,且SOCl2也与水反应
21. (09全国卷Ⅰ)下图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极。
(1) 接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加。据此回答问题:
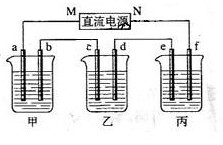 ①电源的N端为 极;
①电源的N端为 极;
②电极b上发生的电极反应为 ;
③列式计算电极b上生成的气体在标准状态下的体积: ;
④电极c的质量变化是 g;
⑤电解前后各溶液的酸、碱性大小是否发生变化,简述其原因:
甲溶液 ;
乙溶液 ;
丙溶液 ;
(2)如果电解过程中铜全部析出,此时电解能否继续进行,为什么?
答案:(1)①正极 ②4OH--4e-=2H2O + O2↑。③2.8L ④16g ⑤甲增大,因为相当于电解水;乙减小,OH-放电, H+增多。丙不变,相当于电解水。(2)可以 因为CuSO4溶液已转变为H2SO4溶液,反应也就变为水的电解反应
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com