
16.(10分)Ⅰ.某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生如下过程:H2O2→O2。
(1)该反应中的还原剂是_______________。
(2)该反应中,发生还原反应的过程是 → 。
(3)该反应中氧化剂与还原剂物质的量之比为 。
(4)如反应转移了0.3mol电子,则产生的气体在标准状况下体积为 。
Ⅱ.已知:Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H=-24.8kJ/mol
3Fe2O3(s)+CO(g)=2Fe3O4(s)+ CO2(g)△H=-47.2kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H=+640.5kJ/mol
请运用盖斯定律写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方
程式:_________________________________________________________________
15.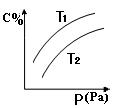 在密闭容器中,对于可逆反应A+3B
在密闭容器中,对于可逆反应A+3B  2C(g),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是
2C(g),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是
A.A一定为气体
B.B一定为气体
C.该反应是放热反应
D.若正反应方向△H <0,则T1>T 2
第Ⅱ卷 (非选择题 共55分)
14.下列实验操作正确的是
|
编号 |
实验 |
操作 |
|
A |
观察钠与水反应 的现象 |
用镊子从煤油中取出金属钠,切下绿豆大小的钠,小心放入装满水的烧杯中 |
|
B |
配制一定物质的量浓度的氯化钾溶液 |
准确称取一定质量的氯化钾固体,放入到1000mL的容量瓶中,加水1000mL溶解,振荡摇匀。 |
|
C |
稀释浓硫酸 |
将蒸馏水沿烧杯内壁慢慢注入盛浓硫酸的烧杯中,并用玻璃棒不断搅拌,使产生的热量不断散失 |
|
D |
取出分液漏斗中 的上层液体 |
下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体从分液漏斗上口倒出 |
13.甲烷燃料电池(电解质是KOH溶液)的总反应为:CH4+2KOH+2O2 = K2CO3 + 3H2O。 下列有关的说法中不正确的是
A.甲烷燃料电池的能量利用率比甲烷燃烧的能量利用率大
B.该燃料电池在使用过程中电解质溶液的浓度和性质均发生变化
C.负极反应式:CH4+3H2O-8e-=CO32-+7H+
D.正极反应式:2O2+4H2O+8e-=8OH-
12.设NA为阿佛加德罗常数,下列叙述中正确的
A.标准状况下,22.4LCO2和O2混合气体中含有的氧原子数为NA
B.0.1mol Fe在0.1mol C12中充分燃烧,转移的电子数为0.3NA
C.2mol SO2和1mol O2在密闭容器中加热(V2O5催化)充分反应后,容器内分子总数为2NA
D.将0.1mol Cl2与足量NaOH溶液在常温下充分反应,转移的电子数为0.1NA
11.关于下列图示的说法中正确的是

A.图①表示CO(g)+H2O(g) CO2(g)+H2(g)是放热反应
CO2(g)+H2(g)是放热反应
B.图②为电解硫酸铜溶液的装置,一定时间内,两电极产生单质的物质的量之比一定
为1︰1
C.图③实验装置可一次而又科学准确的完成比较Cl2、Br2、I2单质氧化性强弱的实验
D.图④两个装置中通过导线的电子数相同时,消耗负极材料的物质的量也相同
10.下列化学反应的离子方程式正确的是
A.往碳酸钡中滴加稀盐酸:CO32-+2H+=CO2↑+H2O
B.用小苏打治疗胃酸过多:HCO3-+H+=CO2↑+H2O
C.往氨水中滴加氯化铝:Al3++4OH-=AlO2-+2H2O
D.氢氧化钡溶液与稀硫酸反应:Ba2++SO42-+H++OH-=BaSO4↓+H2O
9.某元素的一种同位素X的原子质量数为A,含N个中子,它与1 H原子组成HmX分子,在a g HmX中所含质子的物质的量是
A.(A-N+m)mol B.(A-N)mol
C.(A-N)mol D.(A-N+m)mol
8.已知短周期元素的离子。aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是
A.原子半径 A>B>D>C B.原子序数 d>c>b>a
C.离子半径 C>D>B>A D.单质的还原性 A>B>D>C
7.已知:H2(g)+F2(g)=2HF(g) ΔH=-270kJ/mol,下列说法不正确的是
A.44.8L氟化氢气体分解成22.4L的氢气和22.4L的氟气吸收270kJ热量
B.1mol氢气与1mol氟气反应生成2mol液态氟化氢放出的热量大于270kJ
C.相同条件下,1mol氢气与1mol氟气的能量总和高于2mol氟化氢气体的能量
D.2molH-F键的键能比1molH-H键和1molF-F键的键能之和大270kJ
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com