
21. (10分,每空2分)
下图是某药物中间 体的结构示意图:
体的结构示意图:

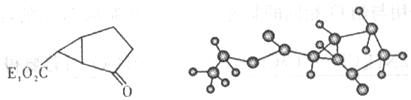
试回答下列问题:
(1)观察上面的结构简式与立体模型,通过对比结构简式,则“E1”表示 ,该药物中间体的分子式为 。
(2)请你根据结构示意图写出该化合物所能发生的反应的化学方程式(除燃烧外)
a. ;
b.  。
。
(3)该药物中间体的异构体X属于芳香族化合物,X的结构中不可能存在的官能团是 。
20. (10分,每空2分)
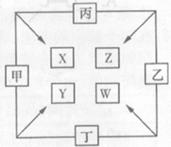 甲、乙、丙、丁四种单质在点燃条件下两两化合生成X、Y、Z、W四种化合物,转化关系如右图所示。
甲、乙、丙、丁四种单质在点燃条件下两两化合生成X、Y、Z、W四种化合物,转化关系如右图所示。
已知:
①甲、乙、丙均为前三周期元素的单质,常温下均为气体,丁是日常生活中的一种常见金属。
②常温下,X是无色液体,Y是黑色固体。
 ③丙在乙中燃烧发出苍白色的
③丙在乙中燃烧发出苍白色的 火焰,丁在乙中燃烧生成棕黄色的烟,W是水溶液呈黄色。
火焰,丁在乙中燃烧生成棕黄色的烟,W是水溶液呈黄色。
请回答:
(1)丁在元素周期表中位于第
族。丁与X在高温下也能得到Y,请写出该反应的化学方程式
 。
。
(2)将少量W的溶液滴入几滴KSCN,迅速变为红色,再加入少量KCl固体,溶液的红色 。
(3)甲与丙两单质的元素可形成原子个数比1:1的化合物H,将H滴入品红后,溶液的颜色褪去,加热后溶液为 (填颜色)。
(4)将Y恰好溶于Z后,检验其中低价金属离子的方法是滴入酸性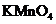 ,紫色褪去,说明有该离子,仔细分析后发现该结论存在漏洞,此“漏洞”是
,紫色褪去,说明有该离子,仔细分析后发现该结论存在漏洞,此“漏洞”是
。
19. (10分,每空2分)
(I)下图甲和乙是某学校王老师制备NH3并进行性质实验时的改进装置。按图甲把仪器安装好,称取2g固体氯化铵装入试管底部,再快速称取2g氢氧化钠覆盖在氯化铵上方;立即用带有滴管的塞子塞紧(滴管预先吸入约2mL浓氨水);烧杯内盛滴有酚酞试液的水;浓氨水滴入试管里,可立即观察到试管内发生剧烈反应,有大量气泡。
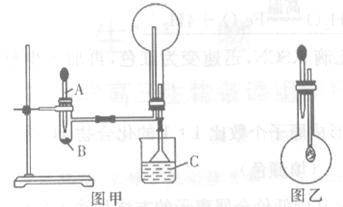
A:浓氨水; B:氢氧化钠和氯化铵混合物;C:滴有酚酞的水
(II)将I中收满NH3的圆底烧瓶取下,改装成图乙所示的装置,胶头滴管内事先预吸入2mLH2O,此时小气球系在玻璃棒上呈自然松弛状态;将滴管内的水慢慢滴入少瓶中,轻轻晃动烧瓶,通过观察实验现象便可以验证NH3的某个性质。按要求回答下列问题:
(1)中学化学教材中是用与制O2相同的制备装置来加热制取NH3的,该方法制NH3的化学方程式为 ;若要得到干燥的氨气可用 进行干燥。
(2)下面是某同学关于王老师能用图甲制取NH3的原因分析,合理的解释是 。
①在NH3·H2O中有平衡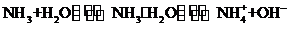 ,
,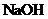 使平衡向左移动
使平衡向左移动
②在NH3·H2O中有平衡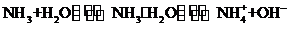 ,
,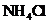 使平衡向左移动
使平衡向左移动
③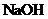 固体溶于水时放热,使体系的温度升高,NH3的溶解度减小,会有部分NH3逸出。
固体溶于水时放热,使体系的温度升高,NH3的溶解度减小,会有部分NH3逸出。
④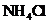 与
与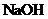 在此情况下可反应生成NH3,及
在此情况下可反应生成NH3,及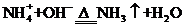
(3)图甲中的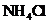 与
与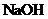 固体混合物能否用
固体混合物能否用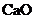 固体代替?
(填“能”或“不能”)
固体代替?
(填“能”或“不能”)
(4)图乙中胶头滴管中的水挤入烧瓶中,观察到的现象及合理解释是 。
18. (12分,每空2分)
甲、乙、丙、丁是4种短周期元素,它们的原子序数依次增大;其中甲和丙、乙和丁分别是同主族元素,又知乙、丁两元素的原子核中质子数之和是甲、丙梁语速原子核中质子数之和的2倍,甲元素的一种同位素核内无中子。
(1)过量的乙与丁组成的一种化合物通入紫色石蕊试液中的现象是 。写出均含甲、乙、丙、丁四种元素的两种化合物相互间发生反应,且生成气体的离子方程式
。
(2)甲与乙组成的化合物与乙和丙组成的化合物反应能产生乙单质,写出该反应的化学方程式 。
(3)用甲元素的单质与乙元素的单质可以制成电池,电池中装有KOH浓溶液,用多孔的金属惰性电极浸入KOH溶液,在A极通入甲的单质,B极通入乙的单质,则A极是该电池的 极;B极的电极反应式是 。
(4)将丁与乙元素以原子个数比1:2组成的化合物6.4g与80mL2mol/L的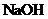 溶液恰好反应,则所生成溶质总质量为
g。
溶液恰好反应,则所生成溶质总质量为
g。
17. (10分,每空2分)
已知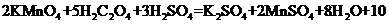 ( ),
( ),
在高锰酸钾酸性溶液和草酸(H2C2O4)溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。
(1)请写出括号内物质的电子式: ,该反应中氧化剂是(填名称) ,
写出草酸与足量NaOH溶液反应的离子方程式 。
(2)针对上述实验现象,某同学认为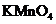 与
与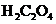 反应是放热反应,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你的猜想还可能是
的影响。
反应是放热反应,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你的猜想还可能是
的影响。
(3)若用已知浓度的酸性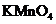 溶液滴定未知浓度的H2C2O4溶液,则
溶液滴定未知浓度的H2C2O4溶液,则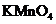 溶液应装在
(填仪器名称)中。
溶液应装在
(填仪器名称)中。
16. 元素X、Y 和Z可结合形成化合物XYZ3;
X、Y和Z的原子序数之和为26;Y和Z在同一周期。下列有关推测正确的是
和Z可结合形成化合物XYZ3;
X、Y和Z的原子序数之和为26;Y和Z在同一周期。下列有关推测正确的是
A、XYZ3可能是一种微溶于水的盐,且X与Z可形成离子化合物XZ
B、XYZ3可能是一种可溶于水的酸,且X与Y可形成共价化合物XY
C、XYZ3可能是一种易溶于水的盐,且Y与Z可形成离子化合物YZ
D、XYZ3可能是一种离子化合物,且Y与Z可形成离子化合物YZ3
第II卷 非选择 题(共52分)
题(共52分)
15. 下列离子在溶液中能大量共存,加入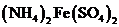 ·
·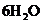 晶体后,仍能大量共存的是
晶体后,仍能大量共存的是
A、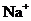
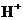
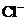
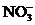 B、
B、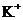
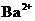
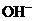
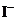
C、
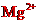

 D、
D、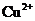
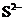
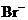
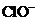
14. 若用下图所示的实验装置里制备纯净、干燥的氯气,并试验它与金属的反应,每个虚线框表示一个氮源装置,其中错误的是
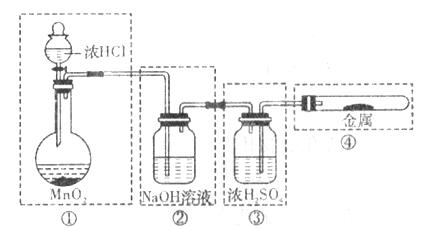
A、只有①和③处 B、只有②④处
C、只有②③④处 D、全部
13. 足量金属M与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与1.68LO2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中 加入2mol/L NaOH溶液至
加入2mol/L NaOH溶液至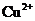 恰好完全沉淀,则消耗
恰好完全沉淀,则消耗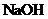 溶液的体积是
溶液的体积是
A、200mL B、150 mL C、100 mL D、50 mL
12. 将一定量的锌与100mL18.5mol/L的浓硫酸充分反应后,锌完全溶解,同时生成气体A33.6L(标准状况)。将反应后的溶液稀释至1L,测得溶液中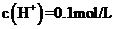 ,则下列叙述中错误的是
,则下列叙述中错误的是
A、反应中消耗的Zn的质量为9 7.5g
7.5g
B、气体A中的SO2和H2的体积比为1:4
C、反应中被还原的元素只有一种
 D、反应中共转移电子3mol
D、反应中共转移电子3mol
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com