
32.7.68gCu与200mL2.0mol/L稀HNO3溶液充分反应。假设反应后的溶液仍为 200mL,求此时溶液中NO3-的物质的量浓度 。
个旧一中2009-2010学年第一学期期中检测
31.在密闭容器中将NO2加热到某温度时,进行如下的反应:2NO2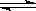 2NO+O2,反应5分钟后达平衡,测得平衡时各组分的浓度分别为:c(NO2)=0.06 mol/L,c(NO)=0.24 mol/L。试求:(1)NO2的转化率为多少?(2)反应开始时与平衡时的压强比为多少?(3)用O2来表示的反应速率是多少mol·L-1·min-1。
2NO+O2,反应5分钟后达平衡,测得平衡时各组分的浓度分别为:c(NO2)=0.06 mol/L,c(NO)=0.24 mol/L。试求:(1)NO2的转化率为多少?(2)反应开始时与平衡时的压强比为多少?(3)用O2来表示的反应速率是多少mol·L-1·min-1。
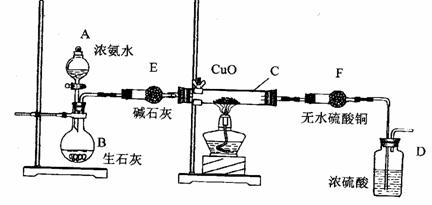
30.(9分)某课外活动小组在实验室用下图的一些装置组合后,快速制取氨并验证氨的某些性质,同时收集少量纯净氮气,请回答:
(1)写出用熟石灰和氯化铵反应制氨气的化学方程式:
。
(2)本实验进行一断时间后,观察到加热的硬质玻璃试管内黑色氧化铜粉末转为红色,盛无色硫酸铜的干燥管内出现蓝色,并且在最后的出气导管处收集到纯净、干燥的氮气。根据这些现象,写出在硬质玻璃试管内发生反应的化学方程式:_______ _,这个反应说明氨气具有________ (填编号)
A.碱性 B.还原性 C.氧化性能 D.不稳定性
(3)洗气瓶中盛浓硫酸的主要作用是_____________ ___。
(4)在最后的出气的导管口收集干燥、纯净的氮气,收集方法是: ______。(填编号) A.排气法 B.排水法 C.用气囊收集
(5)装置E的作用是___________ __。装置F的作用是 _________________。
29.(6分)已知A、B、C、D为气体,E、F为固体,G是氯化钙,它们之间的转换关系如下图所示:
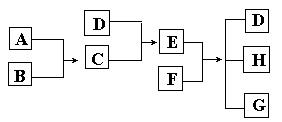
(1) D的化学式(分子式)是_____________,E的化学式(分子式)是_____________。
(2) A和B反应生成C的化学方程式是______________________________。
(3) E和F反应生成D、H和G的化学方程式是:
________ _____________________ _____。 三.实验题(9分)
28.(10分)将一定量的SO2和含0.7mol氧气的空气(忽略CO2)放入一定体积的密闭容器中,550℃时,在催化剂作用下发生反应:2SO2+O2  2SO3(正反应放热)。反应达到平衡后,将容器中的混合气体通过过量NaOH溶液,气体体积减少了21.28L;再将剩余气体通过焦性没食子酸的碱性溶液吸收O2,气体的体积又减少了5.6L(以上气体体积均为标准状况下的体积)。(计算结果保留一位小数)请回答下列问题:
2SO3(正反应放热)。反应达到平衡后,将容器中的混合气体通过过量NaOH溶液,气体体积减少了21.28L;再将剩余气体通过焦性没食子酸的碱性溶液吸收O2,气体的体积又减少了5.6L(以上气体体积均为标准状况下的体积)。(计算结果保留一位小数)请回答下列问题:
(1)判断该反应达到平衡状态的标志是 。(填字母)
a.SO2和SO3浓度相等 b.SO2百分含量保持不变
c.容器中气体的压强不变 d.SO3的生成速率与SO2的消耗速率相等
e.容器中混合气体的密度保持不变
(2)欲提高SO2的转化率,下列措施可行的是 。(填字母)
a.向装置中再充入N2 b.向装置中再充入O2
c.改变反应的催化剂 d.升高温度
(3)该反应达到平衡时SO2的转化率为(用百分数表示) ;
(4)若将平衡混合气体的5%通入过量的BaCl2溶液,生成沉淀 克。
27. (8分)在一密闭容器中进行可逆反应mA(g)+nB(g)
(8分)在一密闭容器中进行可逆反应mA(g)+nB(g) 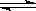 pC(g)+qD(g),符合下图,试用“>”或“<”填(1)-(3)题.
pC(g)+qD(g),符合下图,试用“>”或“<”填(1)-(3)题.
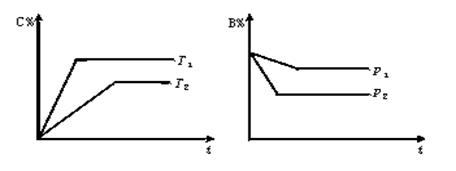
(1)温度T1 T2;(2)压强p1 p2;
(3)m+n p+q;(4)正反应为 反应(填“放热”或“吸热”)。
26.(4分)配平下列化学(或离子)方程式: (1) Cu2S + HNO3 -- Cu(NO3)2+ NO↑ + H2SO4+ H2O (2) SO32- + MnO4- + H+ -- Mn2+ + SO42- + H2O
25.对已达化学平衡的下列反应:2X(g)+Y(g)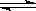 2Z(g),减小压强时,对反应产生的影响是
2Z(g),减小压强时,对反应产生的影响是
A.逆反应速率增大,正反应速率减小,平衡向逆反应方向移动
B.逆反应速率减小,正反应速率增大,平衡向正反应方向移动
C.正、逆反应速率都减小,平衡向逆反应方向移动
D.正、逆反应速率都增大,平衡向正反应方向移动
第Ⅱ卷 非选择题
24.在一个固定体积的密闭容器中,一定温度下,加入2molBr2、1molH2,发生反应:Br2(g)+H2(g) 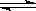 2HBr(g),达到平衡时,HBr的质量分数为w%,在相同条件下,按下列情况充入物质,达到平衡时,HBr的质量分数仍为w%的是
2HBr(g),达到平衡时,HBr的质量分数为w%,在相同条件下,按下列情况充入物质,达到平衡时,HBr的质量分数仍为w%的是
A.2molHBr B.3molHBr
C.2molBr2 + 1molHBr D.3molBr2 +1molH 2+2molHBr
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com