
33.(15分)下图是某家族的两种遗传病的系谱图。据图回答下列问题:
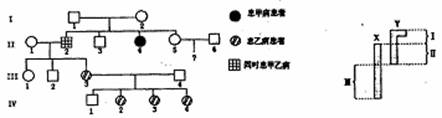
 (1)已知控制乙病的基因位于性染色体上,但不知是位于X、Y的同源区还是非同源区(如图所示),请你完成如下的判断。(甲病用A、a表示、乙病用B、b表示,若位于X、Y同源区,则基因型写法是:XBYB、XBYb、XbYb)
(1)已知控制乙病的基因位于性染色体上,但不知是位于X、Y的同源区还是非同源区(如图所示),请你完成如下的判断。(甲病用A、a表示、乙病用B、b表示,若位于X、Y同源区,则基因型写法是:XBYB、XBYb、XbYb)
据图所知,Ⅰ1、Ⅰ2正常,生了一个患病的
孩子(Ⅱ2),故乙病为① 性遗传病,
如果只考乙病基因,则Ⅲ3的基因型可能是
② ,Ⅲ4的基因型可能是
③ ;只有基因型为④
的婚配后代才会出现男性都正常,女性都患
病;所以该基因位于X、Y的⑤ 。
(2)假设Ⅱ6是甲、乙病的携带者,根据上推断,
若Ⅱ5和Ⅱ6婚配,后代中同时患甲、乙两种
病的几率是 。
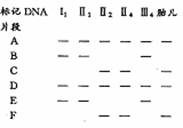
(3)若Ⅱ5再次怀孕后到医院进行遗传咨询,虽乙鉴定胎儿为女性,但医生仍建议对胎儿进行基因检测,原因是① 。用② 将有关DNA分子处理成多个DNA片段后,电泳分离得如右图所示结果。由结果分析可知,该胎儿是否患甲病③ ,理由是④ 。
32.(11分)如图1表示植物光合作用强度与光照强度的关系,图2表示A、B、C三类植物在夏季晴朗的一天中的水分蒸腾情况,图3是一个利用淀粉植物进行光合作用实验的装置示意图。请据图回答:
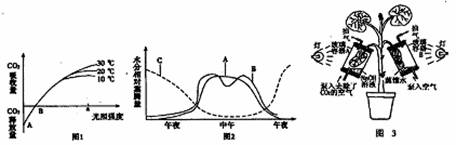
(1)图1中光照强度为a时,不同温度条件下CO2的吸收量不同,导致光合作用强度不同,原因主要 。
(2)图2中若A类植物与B类植物中午之前的光合速率相同,则中午时分的A比B的光合速率(填“大”或“相同”或“小”) ,原因是 。
(3)若取图3中装置若干,植物经“脱淀粉”处理后A、B装置用相同的光照强度照射5小时,对叶片光合作用强度进行测定,取A、B容器内叶片的对应部位截取同等面积的叶片,烘干称重,分别记为WA、WB,分析处理数据,若△W=WB-WA,则△W表示
。
(4)再提供如图装置一套和红、绿玻璃纸各一张,若要探究光质对光合作用的影响,应对装置作怎样的改动?
① 、 ;
② ,并保证其它条件不变且相同。
31.(6分)分子从常态转变为容易发生化学反应的活跃状态所需要的能量称为活化能。可以通过加热使分子得到能量从而转变成活跃状态发生化学反应;也可以加催化剂,降低活化能,发生化学反应。下表是H2O2在不同条件下的分解实验,请分析回答下列问题:
|
处理 试管编号 |
H2O2 |
3.5%FeCl3 |
20%肝脏研磨液 |
温度 |
实验现象 |
|
1 |
2mL |
/ |
/ |
室温 |
无气泡产生 |
|
2 |
2mL |
/ |
/ |
90℃ |
少量气泡 |
|
3 |
2mL |
2滴 |
/ |
室温 |
较多气泡 |
|
4 |
2mL |
/ |
2滴 |
室温 |
大量气泡 |
本实验可得出的结论有:
(1)化学催化剂和酶都能通过降低活化能而具有加速化学反应的功能。说明酶具有 的功能,根据本试验反映出酶具有 的特点。
(2)改变温度,对第 号试管影响最大。该实验还表明,正是由于酶的作用,细胞代谢才能在 条件下快速进行。
30.(15分)A、B、C、D、E、F都是链状有机物,它们一的转化关系如图所示。A中只含有一种官能团,D中含有两种官能团,D分子中不含甲基,且与碳原子相连的氢原子取代所得的一氯代物只有1种。请回答下列问题:
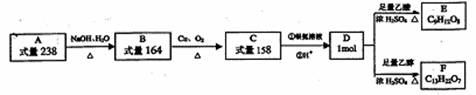
(1)D中含有官能团 ,D的分子式 。
(2)写出D的结构简式 ,A的结构简式 。
(3)写出B生成C的化学方程式 。
(4)写出C与银氨溶液反应的化学方程式
29.(15分)I.某硫酸厂进行硫铁矿(主要成分是FeS2)含量的测定。取样品0.1000g在空气中充分灼烧,将生成的SO2气体与足量的Fe2(SO4)3溶液反应,用度为0.02000mol/L的KMnO4溶液滴定至终点,消耗KMnO4 溶液30.00mL。
已知:SO2+2Fe++2H2O
SO42-+2Fe2++4H+
5Fe2++MnO4-+8H+
5Fe3++Mn2++4H2O
(1)滴定前是否要滴加指示剂? (填:“是”“否”)其理由是 。
(2)样品中FeS2的质量分数是 。(假定杂质不参加反应)
(3)若灼烧6g纯FeS2产生的SO2全部转化为SO3气体放出9.83KJ热量,产生的SO3与水全部化合生成硫酸,放出13.03KJ热量,写出SO3气体转化为硫酸的热化学方程式
。
Ⅱ.二氧化硫和氨的氧化物是大气的主要污染物,防止和治理环境污染是当前环保工作的重要研究内容之一。
(1)用CH4催化还原NOx为N2可以消除氮氧化物的污染。试写出总反应方程式:
,现有1L NO、NO2混合气体,将其还原成N2,需同温同压下CH4的体积0.4L,则混和气体中NO、NO2的物质量之比为 。
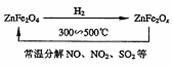 (2)新型纳米材料氧缺位铁酸锌(ZnFe2Ox),常温下它能使工业废气中的氮的氧化物、SO2分解,减小工业废气对环境的影响,它可由铁酸锌(ZnFe2Ox)经高温还原制得。转化流程如图所示:
(2)新型纳米材料氧缺位铁酸锌(ZnFe2Ox),常温下它能使工业废气中的氮的氧化物、SO2分解,减小工业废气对环境的影响,它可由铁酸锌(ZnFe2Ox)经高温还原制得。转化流程如图所示:
若2mol ZnFe2Ox与SO2可生成0.75mol S, x= 。写出由铁酸锌高温被H2还原生成氧缺位铁酸锌的化学方程式 。
28.(15分)已知元素周期表中六种元素,X、Y、Z、W、Q、R原子序数依次减小。回答下列问题:
(1)X元素与Y元素相邻,与X元素处于同一纵行的元素形成的单质的熔点、沸点随元素的原子序数的增大而增大,Y元素的含氧酸有多种,它的单质和氧化物都是强氧化剂,都可用作自来水的消毒剂,X位于周期表的 族,写出实验室制备Y的单质的化学方程式 。
(2)Y、Z、W三个原子的最外层共有11个电子,且三种元素形成的最高价氧化物的水化物之间,两两皆能反应且均生成盐和水,写出Y、Z、W三种元素的最高价氧化物对应水化物反应的离子方程式。
(3)Q、R两元素单原子形成的离子在水中不存,与水作用使水溶液呈碱性,R形成单质的电子式为 ,W与R形成的化合物的化学式为 。它们的晶体属于 晶体。
(4)在一定温度下,R、Q形成的化合物在密闭容器中可发生下列反应:
 2R2O3(g)
4RQ(g)+O2(g);反应到达平衡后,若恒容条件下通入一定量的氨气,则R2O3的转化率
,若在恒压条件下通入一定量的氨气,则R2O3的转化率
。(填“增大”“减小”“不变”)
2R2O3(g)
4RQ(g)+O2(g);反应到达平衡后,若恒容条件下通入一定量的氨气,则R2O3的转化率
,若在恒压条件下通入一定量的氨气,则R2O3的转化率
。(填“增大”“减小”“不变”)
27.(15分)实验室制乙烯通常采用95%的乙醇与浓硫酸(体积比为1:3)混合加热到170℃方法制得,其制备原理可表示如下:
|
 CH3CH2OH+H2SO4(浓) CH3CH2OSO2OH+H2O ①
CH3CH2OH+H2SO4(浓) CH3CH2OSO2OH+H2O ①
|
 CH3CH2OSO2OH(浓)
CH2=CH2↑+H2SO4 ②
CH3CH2OSO2OH(浓)
CH2=CH2↑+H2SO4 ②
(1)浓硫酸在乙烯生成中作用为 ,反①属于 反应,反应②属于 反应。
(2)此法在实际操作中由于浓H2SO4的用量大、比热容高,加热至170℃所需时间长,有人将乙醇和浓H2SO4的混合液加热到80℃时,一次性投入一些小块的生石灰,大大缩短了反应所需时间,提高了乙烯的产率,试用速度和平衡理论解释之。
(3)反应过程中乙醇常被炭化,溶液中有黑色物质出现,随着反应进行炭化现象越来越严重,同时制得的乙烯气体中含有CO2、SO2等气体,为了减少反应过程中炭化现象又不影响乙烯的生成,下列措施合理的是 。
A.调速乙醇和浓硫酸的体积比为1:4
B.调整乙醇和浓硫酸的体积比为1:2
C.用大理石代替碎瓷片
D.降低反应体系温度至140℃
E.用其他脱水剂(如P2O5)代替浓硫酸
(4)为确认混合气体中含有乙烯和二氧化硫,有人设计下图实验装置。(可供选择的试剂:
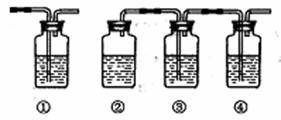 品红溶液、氢氧化钠溶液、溴水、酸性高锰酸钾溶液)
品红溶液、氢氧化钠溶液、溴水、酸性高锰酸钾溶液)
A.①②③④中可盛放的试剂分别为① ;② ;
③ ;④ ;
B.能说明二氧化硫气体存在的现象是 。
C.能确认含有乙烯的现象是 。
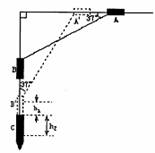
26.(20分)某机械打桩机原理可简化为如图所示,直角固定杆光滑,杆上套有mA=55kg和mB=80kg两滑块,两滑块用无弹性的轻绳相连,绳长为5m,开始在外力作用下将A滑块向右拉到与水平夹角为37°时静止释放,B滑块随即向下运动带动A滑块向左运动,当运动到绳与竖直方向夹角为37°,B滑块(重锤)撞击正下方的桩头C,桩头C的质量mC=200kg。碰撞时间极短,碰后A滑块由缓冲减速装置让其立即静止,B滑块反弹上升0.05m,C桩头朝地下运动0.2m静止。求(1)滑块B磁前的速度;(2)泥土对桩头C的平均阻力。(g=10/ms2)
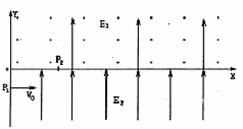
25.(18分)如图所示。坐标系中第一象限有垂直纸面向外的匀强磁场,磁感应强度B=102T,同时有竖直向上与Y轴用方向的匀强电场,均强大小E1=102V/m,第四象限有竖直向上与Y轴同方向的匀强电场,均强大小E2=2E1=2×102V/m。若有一个带正电的微粒,质量m=10-12kg,电量q=10-13C,以水平与x轴同方向的初速度从坐标轴的P1点射入第四象限,OP1=0.2m,然后从x轴上的P2点穿入第一象限,OP2=0.4m,接着继续运动。求:(1)微粒射入的初速度;(2)微粒第三次过x轴的位置;(3)从P1开始到第三次过x轴的总时间。(g=10m/s2)
24.(16分)如上右图所示,某货物仓库,需将生产成品用传递带从底端传递到高度为H的高处存放,货物从静止开始轻放到传送带的最下端,已知货物与传送带间的动摩擦因数为 ,传送带始终保持恒定速度运动。若想用最短时间将货物匀加速运送至顶端,则传送带与水平面夹角θ应设计为多大?最短时间为多少?(传送带长度可随设计需要而变化,g=10m/s2)
,传送带始终保持恒定速度运动。若想用最短时间将货物匀加速运送至顶端,则传送带与水平面夹角θ应设计为多大?最短时间为多少?(传送带长度可随设计需要而变化,g=10m/s2)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com