
5.已知 则
则 的值是
(
)。
的值是
(
)。
A。 (B)
(B) (C)
(C) (D)
(D)
4、已知P是三角形ABC所在平面内的一点,若 其中
其中 ,则点P一定在( )
,则点P一定在( )
A。AC边所在的直线上 B。BC边所在的直线上
C。AB边所在的直线上 D。三角形ABC的内部
3、 设等比数列 的公比
的公比 ,前n项和为
,前n项和为 ,则
,则 ( )
( )
A.  B.
B. C.
C. D.
D.
2.复数 ,则复数
,则复数 对应的点在
(
)。
对应的点在
(
)。
(A)第一象限 (B)第二象限 (C)第三象限 (D)第四象限
1.已知集合M= ,N=
,N= ,则
,则 (
)。
(
)。
A。R B。 C。
C。 D。
D。
28.(14分)已知下列信息:

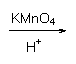
(CH3)2C=CHCH3 + CH3COOH

|
 CH2=CH-CH=CH2+CH2=CH2
CH2=CH-CH=CH2+CH2=CH2
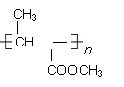 一种用途较广泛的有机玻璃树脂--聚丁烯酸甲酯结构简式为:
一种用途较广泛的有机玻璃树脂--聚丁烯酸甲酯结构简式为:
有一种合成这种高聚物的途径副产物污染少或无污染,原子利用率较高,符合“绿色化学挑战计划”的要求,其合成路线如下:
 |
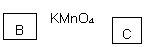 |
||||||
|
|||||||
|
|||||||

|
|

|


试回答下列问题:
(1)写出A、B、D所代表的有机物的结构简式:
A B D
(2)反应④属于 反应(填反应类型)。
(3)在上述合成过程中,原子利用率最高的化学反应有 (填编号)。
27. (9分)在2 L容积不变的密闭容器内,800 ℃时反应2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
|
时间/s |
0 |
1 |
2 |
3 |
4 |
5 |
|
n(NO)/mol |
0.020 |
0.010 |
0.008 |
0.007 |
0.007 |
0.007 |
(1)若上述反应在850℃进行,反应2秒时n(NO)=0.009mol,并且不再随时间而改变,则该反应是________热反应。用O2表示从0-2 s内该反应的平均速率v=_____
(2)下图中表示NO2的变化的曲线是________。
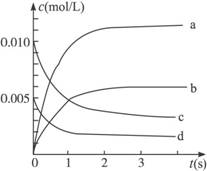
(3)能说明该反应已达到平衡状态的是_________。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
(4)为使该反应的反应速率增大,且平衡向正反
应方向移动的是_________。
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
26.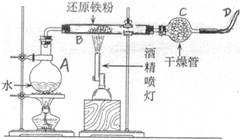 (9分)右图是铁粉和水蒸气反应的
(9分)右图是铁粉和水蒸气反应的
实验装置示意图
(1)写出该反应的化学方程式
(2)实验中,D处排出的气体几乎点不着,
已知该装置不漏气,使用的各种药品没有质量问题,你认为气体点不着的可能原因是:
改正的措施是:
(3)有人建议将烧瓶中的水改用纯碱晶体(Na2CO3•10H2O),你认为是否可行?
理由是
25.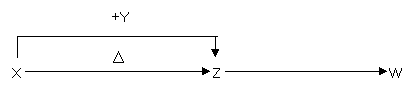 (12分)X、Y、Z、W四种化合物均由短周期元素组成,其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无味气体。这四种化合物具有下列转化关系(部分反应物、产物及反应条件已略去)。
(12分)X、Y、Z、W四种化合物均由短周期元素组成,其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无味气体。这四种化合物具有下列转化关系(部分反应物、产物及反应条件已略去)。
请回答
(1)W是由 键构成的 分子(极性或非极性)
(2)X与Y在溶液中反应的离子方程式是 。
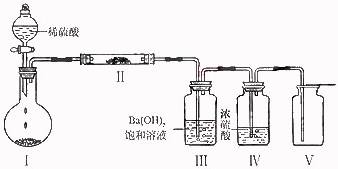 (3)利用下图装置(夹持固定装置已略去)进行实验,在装置I中加入X,装置II中加入一种淡黄色固体物质进行反应,装置III中生成白色沉淀,装置V中可收集到一种无色气体。
(3)利用下图装置(夹持固定装置已略去)进行实验,在装置I中加入X,装置II中加入一种淡黄色固体物质进行反应,装置III中生成白色沉淀,装置V中可收集到一种无色气体。
①装置II中反应的化学方程式是 。
检验装置V中物质的方法是 。
②用X含有的四种元素中的两种组成的某化合物,在催化剂存在下制备并收集纯净干燥的位置V中气体,所需仪器装置是 (从上图选择必要装置,填写编号)。反应的化学方程式是 。
24.近年来,加“碘”食盐较多使用了碘酸钾,KIO3在工业上可用电解法制取,以石墨和铁为电极,以KI溶液为电解液在一定条件下电解,反应式为KI+H2O→KIO3+H2↑。下列有关说法中,正确的是
A、电解时,石墨做阳极,铁作阴极
B、电解时,在阳极上产生氢气
C、电解后得到KIO3产品的步骤有:过滤→浓缩→结晶→灼烧
D、电解中,每转移0.6mol电子,理论上可得到0.1mol无水KIO3晶体
第Ⅱ卷(非选择题:共44分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com