
12、关于某无色溶液中所含离子的鉴别,下列判断正确的是
A.加AgNO3溶液,生成白色沉淀,加稀盐酸沉淀不消失,确定原溶液有Cl-
B.加Ba(NO3)2溶液,生成白色沉淀,加稀盐酸沉淀不消失,确定原溶液有SO42-
C.通入Cl2后,溶液变为黄色,加入淀粉溶液后溶液变蓝,确定原溶液有I-
D.加入盐酸,生成的气体能使澄清石灰水变浑浊,则原溶液中一定有大量CO32-
11、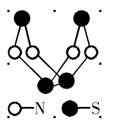 现代无机化学对硫-氮化合物的研究是最为活跃的领域之一。其中下图是已经合成的最著名的硫-氮化合物的分子结构。下列说法正确的是
现代无机化学对硫-氮化合物的研究是最为活跃的领域之一。其中下图是已经合成的最著名的硫-氮化合物的分子结构。下列说法正确的是
A.该物质的分子式为SN
B.该物质的分子中既有极性键又有非极性键
C.该物质具有很高的熔、沸点
D.该物质与化合物S2N2互为同素异形体
10、等物质的量的镁和铝相混合,均分为四份,分别加到足量的下列溶液中,充分反应后,放出氢气最多的是
A.3mol·L-1 HCl溶液 B.4mol·L-1 HNO3溶液
C.8mol·L-1 NaOH溶液 D.18mol·L-1 H2SO4溶液
9、下列说法正确的是
A、H与D,16O与18O互为同位素;甲醇、乙二醇和丙三醇互为同系物
B、最外层有5个电子的原子都是非金属原子
C、周期表中所有元素都是从自然界中发现的
D、由ⅠA族和ⅥA族元素形成的原子个数比为1∶1、电子总数为38的化合物,是含有共价键的离子型化合物
8、下列有关因果关系的描述正确的是
A、因为盐酸的酸性强于氢硫酸,所以氯元素比硫元素非金属性强
B、因为元素最高价态化合物有氧化性,所以磷酸具有强氧化性
C、因为O2转化为O3是吸热反应,所以O3比O2稳定
D、金刚石转变为石墨时结构发生了改变,因而是一个化学反应
7、下列元素的最高价氧化物溶于水,形成的含氧酸的酸性最强的是
A、原子最外层电子数是次外层的2倍的元素
B、原子M层电子数等于另两层电子数之差的元素
C、第三周期ⅦA族的元素
D、其单质有多种同素异形体,其中一种着火点很低、能自燃的元素
6、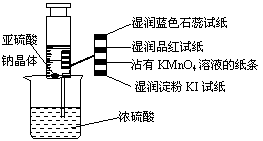 如图所示,在注射器中加入少量Na2SO3晶体,并吸收少量浓硫酸(以不接触纸条为准),则下列有关说法正确的是
如图所示,在注射器中加入少量Na2SO3晶体,并吸收少量浓硫酸(以不接触纸条为准),则下列有关说法正确的是
A.蓝色石蕊试纸先变红后褪色
B.沾有KMnO4溶液的滤纸褪色,
证明了SO2的漂白性
C.湿润淀粉KI试纸变蓝
D.品红试纸褪色证明了SO2的漂白性
5、在一定的温度下,向饱和的烧碱溶液中放入一定量的过氧化钠,充分反应后恢复到原来的温度,下列说法正确的是
A.溶液中Na+浓度增大,有O2放出 B.溶液中OH-总数不变,有O2放出
C.溶液的pH增大,有O2放出 D.溶液中Na+总数减少,有O2放出
4、下列的比较顺序中,不正确的是
A.热稳定性:HF>HCl>HBr>HI B.微粒半径:K+>Na+>Mg2+>Al3+
C.碱性:CsOH>RbOH>KOH>NaOH D.熔点:Li<Na<K<Rb
3、 下列有关0.1 mol·L-1 NaOH 溶液的叙述正确的是
A.1L该溶液中含有NaOH 40g
B.100mL该溶液中含有OH- 0.01mol
C.从1L该溶液中取出100mL,所取出的NaOH溶液的浓度为0.01 mol·L-1
D.在1L水中溶解4g NaOH即可配制得0.1 mol·L-1NaOH 溶液
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com