
119.某温度下,反应2NO2(g)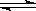 N2O4;ΔH<0在密闭容器中达到平衡,下列叙述中不正确的是( )
N2O4;ΔH<0在密闭容器中达到平衡,下列叙述中不正确的是( )
A.保持体积不变,加入少许N2O4,再达平衡时NO2的体积分数变小
B.保持体积不变,加入少许NO2,将使逆反应速率减小
C.加压使体积变小,将使逆反应速率增大,平衡时颜色变浅
D.保持体积不变,升高温度,再达到平衡时颜色加深
118.下列有关热化学方程式的叙述中,正确的是 ( )
A.含20.0gNaOH的稀溶液与稀盐酸完全中和,放出 28.7 kJ的热量,则表示该反应中和热的热化学方程式为NaOH(aq)+HCl(aq)=NaC1(aq)+H2O(l);△H=-57.4 kJ·mol-1
B.已知C(石墨,s)=C(金刚石,s);△H > 0,则金刚石比石墨稳定
C.已知2H2(g)十O2(g)=2H2O(g)△H=-483.6 kJ·mol-1,则H2的燃烧热为241.8kJ·mol-1
D.已知2C(S)+2O2(g)=2CO2(g); △H1 2C(s)+O2(g)=2CO(g) △H2 则△H1<△H2
117.一定温度和压强下,下列各可逆反应达到化学平衡状态,各反应有如图所示的对应关系:
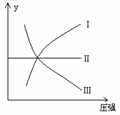 (1)N2(g)+3H2(g)
(1)N2(g)+3H2(g) 2NH3(g);ΔH<0(曲线Ⅰ)
2NH3(g);ΔH<0(曲线Ⅰ)
(2)H2(g)+I2(g) 2HI(g);ΔH>0(曲线Ⅱ)
2HI(g);ΔH>0(曲线Ⅱ)
(3)2SO3(g)  2SO2(g)
+O2(g);ΔH>0(曲线Ⅲ)
2SO2(g)
+O2(g);ΔH>0(曲线Ⅲ)
则下列y轴的表达意义均符合上述三个平衡状态的是( )
A.平衡混合气中一种生成物的体积分数 B.平衡混合气中一种反应物的体积分数;
C.平衡混合气的平均相对分子质量 D.平衡混合气中一种反应物的转化率
116.铜板上铁铆钉处的吸氧腐蚀原理如图所示,下列有关说法中,不正确的是( )
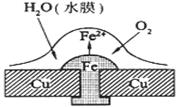 A.正极电极反应式为:2H++2e-=H2↑
A.正极电极反应式为:2H++2e-=H2↑
B.此过程中还涉及到反应:4Fe(OH)2+2H2O+O2=4Fe(OH)3
C.此过程中铜并不被腐蚀
D.此过程中电子从Fe移向Cu
115.下列说法不正确的是( )
A.配制FeCl2溶液时,可将FeCl2晶体先溶于浓盐酸,再加水稀释和少量铁屑保存
B.输油管道,为防止其表面被腐蚀应涂上隔水材料并与外电源负极相连
C.pH值均为9的NaOH溶液和Na2CO3溶液,两溶液中水的电离程度相同
D.0.1mol/L 弱酸HA溶液与0.05mol/L NaOH溶液等体积混合所得溶液有 2c(H+)+c(HA) = c(A-)+2 c(OH-)
114.一定温度下的难溶电解质AmBn在水溶液中达到沉淀溶解平衡时,其平衡常数Ksp=cm(An+)×cn(Bm-),称为难溶电解质的离子积。在25℃时,AgCl的白色悬浊液中,依次加入等浓度的KI溶液和Na2S溶液,观察到的现象是先出现黄色沉淀,最后生成黑色沉淀。已知有关物质的颜色和溶度积如下:
|
物质 |
AgCl |
AgI |
Ag2S |
|
颜色 |
白 |
黄 |
黑 |
|
KSP(25℃) |
1.8×10-10 |
1.5×10-16 |
1.8×10-50 |
下列叙述不正确的是( )
A.溶度积小的沉淀可以转化为溶度积更小的沉淀
B.若先加入Na2S溶液,再加入KI溶液,则无黄色沉淀产生
C.25℃时,饱和AgCl、AgI、Ag2S溶液中所含Ag+的浓度相同
D.25℃时,AgCl固体在等物质的量浓度的NaCl、CaCl2 溶液中的溶度积相同
113.在298K、1.01×105 Pa下,12 g石墨在24 g氧气中燃烧至反应物完全消耗,测得放出x kJ(x>0)的热量。已知在该条件下,1 mol石墨完全燃烧放出y kJ(y>0)的热量。则石墨与氧气反应生成CO的热化学方程式表达正确的是
A、C(石墨,s)+ O2(g)=CO(g) △H(298K)= -y kJ·mol-1
O2(g)=CO(g) △H(298K)= -y kJ·mol-1
B、C(石墨,s)+ O2(g)=CO(g) △H(298K)= -x kJ·mol-1
O2(g)=CO(g) △H(298K)= -x kJ·mol-1
C、C(石墨,s)+ O2(g)=CO(g) △H(298K)= -(2x-y)kJ·mol-1
O2(g)=CO(g) △H(298K)= -(2x-y)kJ·mol-1
D、2C(石墨,s)+O2(g)=2CO(g) △H(298K)= -(2x-y)kJ·mol-1
112.常温下,下列各溶液的叙述中正确的是 ( )
A.0.1mol/L的醋酸钠溶液20mL与0.1mol/L盐酸10mL混合后溶液显酸性
c (Ac-)>c (Cl-)>c (H+)>c (HAc)
B.pH=7的醋酸钠和醋酸混合液中:c(Na+)= c(CH3COO-)
C.0.1mol/L的醋酸的pH=a,0.01mol/L的醋酸的pH=b,则a+1>b
D.已知酸性HF>CH3COOH,pH相等的NaF与CH3COOK溶液中,
[c(Na+)-c(F-)]< [c(K+)-c(CH3COO-)]
111.下列有关二元弱酸H2A的盐溶液的说法中,正确的是( )
A.在溶质物质的量相等的Na2A、NaHA两溶液中,阴离子总数相等
B.在等物质的量浓度的Na2A、NaHA两溶液中,前者pH大于后者
C.在NaHA溶液中一定有:c(Na+)>c(HA-)>c(OH-)>c(H+)
D.在Na2A溶液中一定有:c(Na+)+c(H+)=c(HA-)+c(OH-)+2c(A2-)
110.已知下列反应的热化学方程式为:( )
⑴C(s)+O2(g)=CO2(g) ΔH 1=-393.5kJ/mol
⑵CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH 2=-870.3kJ/mol
⑶H2(g)+ O2(g)=H2O(l) ΔH 3=-285.8kJ/mol
O2(g)=H2O(l) ΔH 3=-285.8kJ/mol
2C(s)+2H2(g)+O2(g)=CH3COOH(l) 的反应热(焓变)为( )
A.488.3 kJ/mol B.-488.3 kJ/mol C.-244.15 kJ/mol D.244.15 kJ/mol
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com