
2、(2009·海南)三聚氰胺化学式为C3H6N6)是一种化工原料,有轻微毒性,计算:
(1) 三聚氰胺相对分子质量:
(2)三聚氰胺中碳、氢、氮元素的质量比:
(3)三聚氰胺中氮元素的质量分数(精确到0.1%)。
1、(2009·青岛模拟)酚酞是常用的酸碱指示剂,化学式为C20H14O4。
(1)酚酞是由
种元素组成的;
(2)酚酞分子中碳原子和氧原子的个数比是 ;
(3)酚酞中碳、氢元素的质量比为
(最简整数比)。
5、混合物中
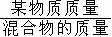
某物质的质量分数(纯度)=
×100%

或==
×100%
[例1](2009·烟台)2008年下半年发生的毒奶粉事件,是不法分子在牛奶或奶粉中添加了有毒的三聚氰胺造成的。三聚氰胺化学式为C3H6N6,是一种重要的化工原料。
(1)三聚氰胺的相对分子质量为 ,碳、氢、氮三种元素的质量比为 ,氮元素的质量分数为 。
(2)检测食品中蛋白质含量的传统方法是:通过检测食品中氮元素的含量,推算其蛋白质含量。例如,若检测到牛奶中的氮元素质量分数≥0.46%,即为蛋白质含量检测合格。某种不合格牛奶中氮元素的质量分数为0.36%,若向1000g该牛奶中加入2g三聚氰胺,请计算此时牛奶中氮元素的质量分数,并根据计算结果说明不法分子在牛奶中添加三聚氰胺的目的。
[答案](1)126 6∶1∶14 66.7% (2)0.49% 目的是提高牛奶中含氮量,造成牛奶中蛋白质含量高或合格的假象
[解析](1)C3H6N6的相对分子质量==12×3+1×6+14×6==126
碳、氢、氮三种元素的质量比为(12×3):(1×6):(14×6)==6:1:14
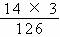
氮元素的质量分数 ==×100%=66.7

(2)加入三聚氰胺后牛奶中氮元素的质量为
1000g×0.36%+2g×66.7%≈4.9g
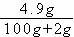
×100%≈0.49%
[规律小结]化学式的计算要看清元素符合右下角的数字,这些数字是解题的关键。
变式训练一
4、A元素的质量
==化合物(AmBn)的质量×A的质量分数
3、AB元素的质量比:



= 
注:计算时一定要写清楚各元素质量比顺序,因顺序不同,比值也不同。
2、A的质量分数=
×100%
注、利用上述公式计算时,某元素的原子个数应写在该元素符号前面,不能写在右下角。
常用的计算公式(以化合物AmBn为例)
1、相对分子质量=A的相对原子质量×m+B的相对原子质量×n
 注:计算结晶水合物的相对分子质量时,化学式中的“·”表示相加,而不表示相乘。
注:计算结晶水合物的相对分子质量时,化学式中的“·”表示相加,而不表示相乘。
122.一种新燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-。下列对该燃料说法正确的是( )
A、在熔融电解质中,O2-由负极移向正极
B、电池的总反应是:2C4H10 + 13O2 → 8CO2 + 10H2O
C、通入空气的一极是负极,电极反应为:O2 + 4e- = 2 O2-
D、通入丁烷的一极是负极,电极反应为:C4H10 - 26e- + 13 O2-= 4CO2 + 5H2O
121.在反应容器中充入lmolA气体和nmolB气体,在一定条件下发生反应:A(g)+nB(g)  mD
(g),达平衡时,测得A的转化率为50%,在相同温度和相同压强下,平衡时混合气体的体积是反应前的
mD
(g),达平衡时,测得A的转化率为50%,在相同温度和相同压强下,平衡时混合气体的体积是反应前的 ,则n和m的数值可能是
( )
,则n和m的数值可能是
( )
A.n=l m=l B.n=2 m=2 C.n=3 m=3 D.n=2 m=3
120.将两个铂电极插入氢氧化钾溶液中,向两极分别通入甲烷和氧气,即构成甲烷燃料电池,已知通入甲烷的一极,其电极反应为:CH4+10OH--8e-=CO32-+7H2O;通入氧气的另一极,其电极反应式是
2O2+4H2O+8e-=8OH-,下列叙述正确的是 ( )
A.通入甲烷的电极为负极
B.正极发生氧化反应
C.该电池使用一段时间后应补充氢氧化钾
D.燃料电池工作时,溶液中的阴离子向正极移动
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com