
11. 在一定温度下,对于反应2A(g)+B(g)
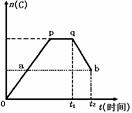
在一定温度下,对于反应2A(g)+B(g)  2C(g)在反应过程中C的物质的量n(C)随着时间变化关系如图所示,现从t1时间开始对反应体系升高温度,n(C)的变化如图qb所示。试回答下列问题:
2C(g)在反应过程中C的物质的量n(C)随着时间变化关系如图所示,现从t1时间开始对反应体系升高温度,n(C)的变化如图qb所示。试回答下列问题:
(1)p点反应的v正
v逆(填“>”、“<”或“=”)
(2)此反应的正反应为 热反应(填“放”或“吸”);
(3)a、b两点的正反应速率;va vb(填“>”、“<”或“=”)。
$
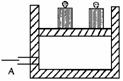
10.如图所示为一恒压容器。在恒定温度下,将1molN2和3molH2混合后由A口快速充入容器,封闭A,反应N2+3H2 2NH3在t1时刻达到平衡,t2时刻再从A口快速充入一定量NH3,封闭A,t3重新达平衡至t4。请在图中画出0→t4时间内混合气中NH3的体积分数(y坐标)随时间(x坐标)变化的曲线。
2NH3在t1时刻达到平衡,t2时刻再从A口快速充入一定量NH3,封闭A,t3重新达平衡至t4。请在图中画出0→t4时间内混合气中NH3的体积分数(y坐标)随时间(x坐标)变化的曲线。

9.将2mol H2O和2mol CO置于1L容器中,在一定条件下,加热至高温,发生如下可逆反应:
2H2O(g)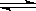 2H2+O2
2H2+O2
2CO+
O2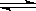 2CO2
2CO2
(1)当上述系统达到平衡时,欲求其混合气体的平衡组成,则至少还需要知道两种气体的平衡浓度,但这两种气体不能同时是 和 ,或 和 。(填它们的分子式)
(2)若平衡时O2和CO2的物质的量分别为 n(O2)平=a mol, n(CO2)平=b mol。试求n(H2O)平= 。(用含a、b的代数式表示)
8.在一恒定的容器中充入2 mol A和1
mol B发生反应:2A(g)+B(g)  x C(g),达到平衡后,C的体积分数为W%;若维持容器的容积和温度不变,按起始物质的量A:0.6 mol、B:0.3 mol、C:1.4 mol充入容器,达到平衡后,C的体积分数仍为W%,则x值为
x C(g),达到平衡后,C的体积分数为W%;若维持容器的容积和温度不变,按起始物质的量A:0.6 mol、B:0.3 mol、C:1.4 mol充入容器,达到平衡后,C的体积分数仍为W%,则x值为
A.只能为2 B.只能为3
C.可能是2,也可能是3 D.无法确定
7.可逆反应3A(g) 3B(?)+C(?);ΔH>0。随着温度升高,气体平均相对分子质量有变小趋势,则下列判断中正确的是( )
3B(?)+C(?);ΔH>0。随着温度升高,气体平均相对分子质量有变小趋势,则下列判断中正确的是( )
A.B和C可能都是固体 B.B和C一定都是气体
C.若C为固体,则B一定是气体
D.B和C可能都是气体
6.在密闭容器中,对于反应:2SO2(g)+O2(g)  2SO3(g),SO2和O2起始时分别为20 mol和10
mol;达平衡时,SO2的转化率为80%。若从SO3开始进行反应,在相同的温度下,欲使平衡时各成分的百分含量与前者相同,则起始时SO3的物质的量及其转化率为( )
2SO3(g),SO2和O2起始时分别为20 mol和10
mol;达平衡时,SO2的转化率为80%。若从SO3开始进行反应,在相同的温度下,欲使平衡时各成分的百分含量与前者相同,则起始时SO3的物质的量及其转化率为( )
A.10 mol和10% B.20 mol和20%
C.20 mol和40% D.20 mol和80%
5.一定温度下,将amolPCl5通入一个容积不变的密闭容器中,发生反应:PCl5(g)  PCl3(g)+Cl2(g)反应达平衡时,测得混合气体的压强为P1,此时再向容器中通入amolPCl5,同样温度下再度达到平衡时,测得压强为P2。下列判断正确的是(
)
PCl3(g)+Cl2(g)反应达平衡时,测得混合气体的压强为P1,此时再向容器中通入amolPCl5,同样温度下再度达到平衡时,测得压强为P2。下列判断正确的是(
)
A.2P1>P2 B.PCl5的分解率增大
C.2P1<P2 D.Cl2的体积分数增大
4.放热反应CO(g)+H2O(g)
 CO2(g)+H2(g)在温度t1时达到平衡,c1(CO)=c1(H2O)=1.0
mol/L,其平衡常数为K1。升高反应体系的温度至t2时,反应物的平衡浓度分别为c2(CO)和c2(H2O),平衡常数为K2,则(
)
CO2(g)+H2(g)在温度t1时达到平衡,c1(CO)=c1(H2O)=1.0
mol/L,其平衡常数为K1。升高反应体系的温度至t2时,反应物的平衡浓度分别为c2(CO)和c2(H2O),平衡常数为K2,则(
)
A.K2 和K1的单位均为mol/L B.K2 <K1
C.c2(CO)=c2(H2O) D.c1(CO)>c2(CO)
3.某温度下,反应H2(g)+I2(g)  2HI(g);ΔH<0。在一带有活塞的密闭容器中达到平衡,下列说法中不正确的是( )
2HI(g);ΔH<0。在一带有活塞的密闭容器中达到平衡,下列说法中不正确的是( )
A.恒温,压缩体积,平衡不移动,混合气体颜色加深
B.恒压,充入HI(g),开始时正反应速率减小
C.恒容,升高温度,正反应速率减小
D.恒容,充入H2, I2(g)的体积分数降低
2.在固定容积的密闭容器中,A和B发生下列反应,A(s)+2B(g)  2C(g);ΔH>0。在一定条件下达到平衡,若升高温度则达平衡后混合气体的( )
2C(g);ΔH>0。在一定条件下达到平衡,若升高温度则达平衡后混合气体的( )
A.平均相对分子质量增大
B.平均相对分子质量减小
C.密度增大
D.密度减小
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com