
通过作习题后,反思所涉及到的知识点,每解答完一个题目,思考此题所涉及到的化学基础知识,使知识点和题目挂钩,达到夯实基础,又可优化知识式结构的目,便于知识的消化、贮存、提取和应用。反思解题的思路和方法,一道试题,做完以后,思考,还有其他解法吗,那一种最好,若更换某一条件,此题又如何解答呢?解题思路是否正确、严谨,能否引出一类题的解法,强化解题能力提高解题效率。反思解题过程中的失误。解题时,走过哪些弯路,犯过哪些错误,又是如何解决的,克服自己在解题中不足之处。
学习方法的交流,并不是简单地学生提前打好底稿,到台前一念。这样做的效果并没有多大,重点并不突出。为此,定期举办学习计划、优秀笔记展览,试卷自批记录展览;学习经验简介:把易混易错的问题整理成小册子,随身携带,一有空闲,便翻阅察看,强化记忆。
自由复习,并不是学生随便,它需要在复习之前,要求学生制定出切实可行的复习计划,一定要根据自己的实际水平和能力,并且保持均衡发展,不要偏科。复习的方法多种多样,但一定要有效。比如;把一年来的试卷进行分类整理,装订成卷,同时,还要把试卷中的错误及时进行纠正,找出原因所在,及时进行查漏补缺,突出重点,梳理知识头绪,把握思路。自由复习的整个过程,重点突出学生是在整理理解、消化、提高的过程。千万不能又重新进行大量练习题的开始。
化学是一门以实验为主的自然学科,知识的理解和掌握都通过实验来实现的。因此,高三复习阶段,可以把一些代表物质的性质,设计成一整套的实验,学生通过自己亲自动手实验,达到了掌握知识,培养能力的目的。在头脑中形成一个清醒的认识思路,找到了解决问题的方法。同时又培养学生主动学习的意识,研究探索的意识,相互合作的意识。
为了避免好生吃不饱,差生消化不了,安排好时间同时考同一学科,一定要全批全改,一定要严肃认真,一定做好试题的分析准备工作。然后根据学生成绩不同,分不同层次,把学生集中在一起,由教师进行专门的试卷讲评。对于层次高一些的学生,重点分析完试卷后,针对存在的问题,要进行高层次的深化,进行一题多解,一题多变,多题一解…,好学生吃饱吃好。对于中等学生,讲主干知识,使之成块、成网,成系统。对于差生,重点放在基础知识的巩固上,同时,还要对学生进行针对性的辅导,补课。
针对所学知识中重点、难点、疑点问题,可进行专题化训练,要练到火候:练速度、练准确率、练答题技巧,练语言表达能力,练分析问题的能力,特别是在有限的时间内,让学生具有实战能力。
高三复习,做题避免不了,但易陷入题海中,整天做题、讲题,然后再做,学生没有理解深化的过程,很难把知识掌握到位。物理学家卢瑟福带弟子,问之:上午干什么?答:实验室;又问之:下午干什么?答:实验室;复又问之:晚上干什么?答:实验室;卢瑟福追问了一句:你整天都在做实验,那你什么时间进行思考呢?没有思考,也就不可能有深化的过程,更谈不上提高。为了达到精讲,教师必须要钻研大纲,熟悉教材,把握知识的重难点,删去偏、难、怪题。让学生把精力都放在基础知识的掌握上,能力的提高上。教师在组题时,可挑选一些比较好的试题,但尽量不要用成题,原题,及使用,也要在原有基础上加以变动,要有创意,内容上要尽量涵盖所有的知识点,一则使学生不会感到枯燥,二则也提高了教师对知识的把握精度,编题的水平,虽然教师要付出相当大的工作量,可会节省下学生的更多宝贵时间,同时,大大地提高了复习的效率。这样也就避免了各学科间相互抢课,挤占时间的现象的出现。
学期初,任课教师通过集体商讨,制定出本学科的复习计划,并选定好一本复习资料;然后据本学科的学科特点和内容,确定好每位教师应具体负责的内容,章节内容要落实到人,目的、要求要具体明确。所有计划做出后,印发到各班,分发到学生手中,使学生做到心中有数。
2、由于,高中教材中不再涉及化学平衡常数的概念,所以,不好从浓度商和平衡常数的角度给出平衡移动的判断标准,但从化学反应速率的角度给出平衡移动的标准学生是可以接受的。笔者建议,新的教材中不妨从化学反应速率角度明确给出平衡移动的标准。
在恒温恒容下,对于反应:2NO2=N2O4 ,若增加N2O4的浓度时,浓度和压强都增大,最终平衡究竟往哪个方向移动,NO2的转化率该如何变化.遇到此类问题,应以物理变化(加入物质,浓度增大)的影响为主(主要矛盾),化学变化(即平衡移动)为辅(次要矛盾)。
平衡转移看浓度转化率看压强我们老师是这么教的~那此题NO2的转化率应该变大吧
3.反应向右进行,平衡向左移动。理由:增大反应物的浓度,正反应速率增大,此时逆反应速率不变,所以,反应向正反应方向进行。由于,新加入的PCl5的转化率比原来容器中的低(原理分析同1),所以,平衡向左移动了。
下面说明一下,以上观点的错误原因:
观点一:把平衡后再充入1mol PCl5的过程,同开始就充入2 mol PCl5等价,本身犯了“偷换概念”的错误。即使等价于开始充入2 mol PCl5,也不能称之为平衡的移动,平衡的移动是指对于同一容器中的达到平衡的可逆反应,因条件改变而引起的变化。
观点二:不能把平衡移动的方向和物质的百分含量联系在一起。如:在一定温度下,某密闭容器中进行合成氨的反应N2+3H2 2NH3达到平衡,再充入n
mol H2平衡向右移动,达新平衡后NH3的百分含量增大吗?很明显,不一定,这取决于n与原来平衡混合气的总物质的量的大小对比(主要)和反应进行的程度;如:n远大于原平衡混合气的总物质的量时,氨气的百分含量一定减小了。所以,化学平衡移动的方向与物质的百分含量无关。
2NH3达到平衡,再充入n
mol H2平衡向右移动,达新平衡后NH3的百分含量增大吗?很明显,不一定,这取决于n与原来平衡混合气的总物质的量的大小对比(主要)和反应进行的程度;如:n远大于原平衡混合气的总物质的量时,氨气的百分含量一定减小了。所以,化学平衡移动的方向与物质的百分含量无关。
观点三:好象很圆滑,但也犯了将平衡移动方向和反应物的转化率混为一谈的错误。认为转化率提高平衡就向右移动,反之向左移动,本身就是错误的。举例说明:一定温度下,在一体积固定的密闭容器中,加入1 mol H2和1 mol I2(g),达到平衡后,充入1 mol H2则平衡向右移动,再充入1 mol I2(g)平衡又向右移动,但根据转化率的关系,因为首次平衡和最终平衡态的转化率相等,就会得出两次右移等于平衡不移动的谬论。
产生以上错误的根本原因在于没有弄清楚,平衡移动的判断标准,化学平衡的移动是旧的平衡被破坏,建立新平衡的过程,旧的平衡被破坏的原因是v(正)=v(逆)的条件被打破,从而产生两种平衡移动的方向,v(正)′> v(逆)′平衡右移,v(正)′< v(逆)′平衡左移。
综上所述,化学平衡移动的标准是:改变外界条件后v(正)′和v(逆)′的大小关系,若v(正)′> v(逆)′则平衡右移,若v(正)′< v(逆)′则平衡左移,或者说是和反应进行的方向一致。
对教材的建议:
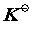
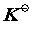
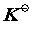 1、大学教材中,化学平衡移动的判断依据是:反应商(Q)与标准平衡常数( )的相对大小的变化,平衡时Q= ,改变条件使Q< ,平衡被破坏,反应向正向(或逆向)进行,之后重新建立平衡,我们说平衡右移(左移)
1、大学教材中,化学平衡移动的判断依据是:反应商(Q)与标准平衡常数( )的相对大小的变化,平衡时Q= ,改变条件使Q< ,平衡被破坏,反应向正向(或逆向)进行,之后重新建立平衡,我们说平衡右移(左移)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com