
11、 答案C
答案C
 [解析]根据化学方程式可得,生成的氢气的物质的量等于参加反应的碱的物质的量的一半,所以A项正确;B项中p为生成的氧化物的质量,1molMg可结合1molO,2molAl结合3molO,因此生成沉淀的物质的质量等于镁和铝的质量之和加氧元素的质量,而结合氧元素的物质的量等于生成氢气的物质的量,也等于消耗氢氧根离子的物质的量的一半,所以B项正确,而得到的氢氧化镁和氢氧化铝的质量等于镁铝的质量和与氢氧根离子的质量之和,C项中忽略了体积的单位。
[解析]根据化学方程式可得,生成的氢气的物质的量等于参加反应的碱的物质的量的一半,所以A项正确;B项中p为生成的氧化物的质量,1molMg可结合1molO,2molAl结合3molO,因此生成沉淀的物质的质量等于镁和铝的质量之和加氧元素的质量,而结合氧元素的物质的量等于生成氢气的物质的量,也等于消耗氢氧根离子的物质的量的一半,所以B项正确,而得到的氢氧化镁和氢氧化铝的质量等于镁铝的质量和与氢氧根离子的质量之和,C项中忽略了体积的单位。
 [考点分析]化学计算
[考点分析]化学计算
10、答案B
[解析]A项可能受到Ag+影响生成AgCl沉淀;C能够使品红溶液褪色的气体不一定就是 还可能是其他气体比如氯气;D、能发生银镜反应的官能团为醛基,而醛基还可能存在与甲酸或甲酸某酯、甲酸盐中。
还可能是其他气体比如氯气;D、能发生银镜反应的官能团为醛基,而醛基还可能存在与甲酸或甲酸某酯、甲酸盐中。
[考点分析]常见离子检验、物质鉴别综合运用
9、 答案B
答案B
 [解析]A项不符合中和热的定义;C项中生成物水为气态,D项中辛烷的物质的量不是1mol,所以ACD错误。
[解析]A项不符合中和热的定义;C项中生成物水为气态,D项中辛烷的物质的量不是1mol,所以ACD错误。
 [考点分析]燃烧热、中和热概念的理解及热化学方程式书写正误判断
[考点分析]燃烧热、中和热概念的理解及热化学方程式书写正误判断
 [考点分析]元素周期律和元素周期表的综合应用
[考点分析]元素周期律和元素周期表的综合应用
8、 答案D
答案D
 [解析]X、Y、Z相邻且X的原子序数为Y的一半,推测X为氧元素,则Y为硫元素,Z为氯元素。其最高价氧化物的水化物为HClO4。三种元素中S元素的非金属性最弱,因此其氢化物的还原性最强。根据M2Y又因为X、Y、Z、M是元素周期表中前20号元素,其原子序数依次增大判断M为钾元素,SO2为极性分子,而K2S属于离子化合物。
[解析]X、Y、Z相邻且X的原子序数为Y的一半,推测X为氧元素,则Y为硫元素,Z为氯元素。其最高价氧化物的水化物为HClO4。三种元素中S元素的非金属性最弱,因此其氢化物的还原性最强。根据M2Y又因为X、Y、Z、M是元素周期表中前20号元素,其原子序数依次增大判断M为钾元素,SO2为极性分子,而K2S属于离子化合物。
7、答案D
 [解析]A项中H+与HSO3-不能大量共存;B项隐含条件是酸性溶液NO3-在酸性条件下具有强氧化性,可氧化I-,C项中Fe2+和AlO2-可发生双水解而不能大量共存。 D项为碱性条件,可大量存在。
[解析]A项中H+与HSO3-不能大量共存;B项隐含条件是酸性溶液NO3-在酸性条件下具有强氧化性,可氧化I-,C项中Fe2+和AlO2-可发生双水解而不能大量共存。 D项为碱性条件,可大量存在。
 [考点分析]离子共存
[考点分析]离子共存
6、 答案A
答案A
[解析]B、C60为分子晶体;B、纤维素为天然高分子化合物,而纤维素硝酸酯是人工合成的、D、二氧化硅是制造光导纤维的主要材料。
[考点分析]本题主要考查化学与生活、化学基本概念.
13. 在一体积可变的密闭容器中,加入一定量的X、Y,发生反应
在一体积可变的密闭容器中,加入一定量的X、Y,发生反应

 kJ/mol。反应达到平衡时,Y的物质的量浓度与温度、气
kJ/mol。反应达到平衡时,Y的物质的量浓度与温度、气
 体体积的关系如下表所示:
体体积的关系如下表所示:
 气体体积 气体体积 C(Y)/mol·L-1 C(Y)/mol·L-1   温度℃ 温度℃ |
1 |
2 |
3 |
|
100 |
1.00 |
0.75 |
0.53 |
|
200 |
1.20 |
0.9 |
0.63 |
|
300 |
1.30 |
1.00 |
0.70 |
下列说法正确的是
 A.m>n
A.m>n
 B.Q<0
B.Q<0
 C.温度不变,压强增大,Y的质量分数减少
C.温度不变,压强增大,Y的质量分数减少  D.体积不变,温度升高,平衡向逆反应方向移动
D.体积不变,温度升高,平衡向逆反应方向移动

12. 关于浓度均为0.1
mol/L的三种溶液:①氨水、②盐酸、③氯化铵溶液,下列说法不正确的是
关于浓度均为0.1
mol/L的三种溶液:①氨水、②盐酸、③氯化铵溶液,下列说法不正确的是
 H+4):③>①
H+4):③>①
 B. ①和③等体积混合后的溶液:c(NH+4)>c(Cl
B. ①和③等体积混合后的溶液:c(NH+4)>c(Cl )>c(OH
)>c(OH )>c(H+)
)>c(H+)
 C.①和②等体积混合后的溶液:c(H+)=c(OH
C.①和②等体积混合后的溶液:c(H+)=c(OH )+c(NH3·H2O)
)+c(NH3·H2O)  D.水电离出的c(H+):②>①
D.水电离出的c(H+):②>①
11. 向m g镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体b L。
向m g镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体b L。
 向反应后的溶液中加入c mol/L氢氧化钾溶液V mL,使金属离子刚好沉淀完全,得到的
向反应后的溶液中加入c mol/L氢氧化钾溶液V mL,使金属离子刚好沉淀完全,得到的
 沉淀质量为n g。再将得到的沉淀灼烧至质量不再改变为止,得到固体p g。则下列关系不正确的是
沉淀质量为n g。再将得到的沉淀灼烧至质量不再改变为止,得到固体p g。则下列关系不正确的是
 A.
A. B.
B. C.n=m+17Vc D.
5m/3<
C.n=m+17Vc D.
5m/3<
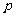 <17m/9
<17m/9
10.下列有关物质检验的实验结论正确的是
|
选项 |
实
验 操 作 及 现 象 |
实
验 结 论 |
|
A |
向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成 |
该溶液中一定含有 |
|
B |
向某溶液中加入2滴KSCN溶液,溶液不显红色。再向溶液中加入几滴新制的氯水,溶液变为红色 |
该溶液中一定含有 |
|
C |
将某气体通入品红溶液中,品红溶液褪色 |
该气体一定是 |
|
D |
将少量某物质的溶液滴加到新制的银氨溶液中,水浴加热后有银镜生成 |
该物质一定属于醛类 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com