
8.设起始时通入的一定量A气体为n mol
2A(g)  B(g) + xC(g)
B(g) + xC(g)
起始(mol) n 0 0
变化(mol) na% 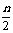 a%
a% 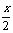 na%
na%
平衡(mol)n(1-a%) 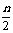 a%
a% 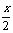 na%
na%
据气体定律有:n/[n(1-a%)+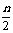 a% +
a% +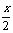 na%]=1/[1+p%]
na%]=1/[1+p%]
解得:(x-1)a=2p 对照选项可知BC符合。
1.B 2.C 3.B 4.B 5.A 6.A 7.BC 8.BC
讲析:2.由于NO2气体中总是存在2NO2(g)  N2O4(g);△H<0
这一反应,故通常测得的“NO2的相对分子质量”,往往是NO2与N2O4的平均相对分子质量,故测量值总是偏高。为了尽可能准确地测定NO2的相对分子质量,应使可逆反应尽量向逆反应方向移动。根据化学平衡移动原理,升高温度,减小压强都使平衡向逆反应方向移动。4.增大压强正逆反应速率都增大,则反应物和生成物中一定都有气体。且
N2O4(g);△H<0
这一反应,故通常测得的“NO2的相对分子质量”,往往是NO2与N2O4的平均相对分子质量,故测量值总是偏高。为了尽可能准确地测定NO2的相对分子质量,应使可逆反应尽量向逆反应方向移动。根据化学平衡移动原理,升高温度,减小压强都使平衡向逆反应方向移动。4.增大压强正逆反应速率都增大,则反应物和生成物中一定都有气体。且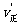 >
>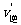 ,说明正反应是气体体积缩小的反应。 6.运用差量法求解。 7.化学平衡的计算模式: mA2(g)+nB2(g)
,说明正反应是气体体积缩小的反应。 6.运用差量法求解。 7.化学平衡的计算模式: mA2(g)+nB2(g) pC(g)
pC(g)
起始浓度(mol/L) a a 0
变化浓度(mol/L) mx nx px
平衡浓度(mol/L) a-mx a-nx px
据题意:a-mx=0.9 a-nx=0.1 px=0.8
联立解得:n-m=p 对照选项,运用原子守恒,满足关系的是BC。
4.(1)减小,通入适量SO2或给体系升温 (2)任意值 (3)3.6<c≤4
讲析:(2)a:b=1.2:0.6=2:1,与反应达到平衡状态A时的起始比例相同,为恒温恒压下的等效平衡,生成物只有一种物质,则c取任意值。
(3)
2SO2(g)+O2(g)  2SO3(g)
2SO3(g)
起始量 a b c
据题意有: a+b+c<4.2……①
假设c molSO3完全转化为SO2、O2,则
(a+c)+(b+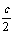 )=6……②
联立①②得:c>3.6
)=6……②
联立①②得:c>3.6
若起始时只有SO3,则c≤4。
c的取值范围:3.6<c≤4
检测提高
3.(1)770℃ 890℃
(2)降低压强或移去钾蒸气 适当升高温度
(3)K=C(K)/C(Na)
讲析:此题要求学生能够分析图表数据,并结合化学平衡移动原理加以运用。要知道常压为101.3Kpa,且对平衡常数数学表达式的要求要熟悉。
1.B 2.A
9.(1)在等温等容条件下,达平衡时容器内气体压强都为P。两者为等效平衡,换算为同一半边的物质的物质的量相同。设通人1/3molNH3,需加入N2和H2的物质的量分别为x和y,则有:x+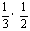 =1
x=5/6 y+
=1
x=5/6 y+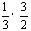 =1 y=1/2
=1 y=1/2
(2)假设1molH2完全反应,可生成NH3 2/3mol,
消耗N21/3mol,则2/3<n(N2)<1; 0<n(NH3)<2/3。
(3)不可能,若按题中给出的N2和H2物质的量
n(H)=0.5×2+0.5×3=2.5>2,不符合守恒原理。
第13课时 (B卷)
纠错训练
8.关于合成氨反应压强条件的选择,从理论上看:由于增大压强有利于增大化学反应速率,而该反应又是一个很难进行的反应,因此,应尽量采用高压;又因该反应正方向是一个气体分子数减小的反应,增大压强,平衡将向气体分子数减小的方向即正反应方向移动,故高压有利于提高N2、H2的转化率。由此可知,无论从反应速率,还是从化学平衡考虑,增大压强总是有利的,因而从理论上讲,压强越高越好。
但是,基于以下两个原因:(1)实验表明,当压强增大到一定程度时,继续增大压强,NH3在平衡混合物中含量增加的幅度越来越不显著;(2)压强增大,对动力、材料及设备的要求越来越高,而这些要求又受到现实条件的种种限制,因此,压强的无限增大既无必要,也不现实。
综上所述,从提高综合经济效益考虑,应采取适当高压,就目前理论和实践发展水平来看,根据生产厂家的规模和条件,宜采用的压强是20MPa--50MPa。
关于SO2转化为SO3的反应:2SO2(g)+O2 (g)  2SO3(g);△H<0,虽然增大压强对提高反应速率和转化率都有利,但由于在V2O5催化下,此反应已有很快的速率,且常压下SO2转化率已高达97.5%(450℃),故不必采取加压的措施。
2SO3(g);△H<0,虽然增大压强对提高反应速率和转化率都有利,但由于在V2O5催化下,此反应已有很快的速率,且常压下SO2转化率已高达97.5%(450℃),故不必采取加压的措施。
可见,反应条件的选择应从理论与实际两个方面综合考虑。
7.(1)除CO的原因是防止合成塔中的催化剂中毒;
(2)吸收CO的适宜条件应选择:低温、高压;
(3)醋酸铜氨再生的适宜条件是:高温、低压。
讲析:分析吸收CO反应的特点:正反应是气体体积缩小的放热反应,对于这样一个可逆反应,用化学平衡原理及有关知识可做出解答。
6.解建立计算模式: X + 2Y  2Z
2Z
n始(mol) a b 0
Δn(mol) x 2x 2x
n平(mol) a-x b-2x 2x
据题意:(a-x)mol+(b-2x)mol=2xmol 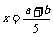 mol
mol
气体Y的转化率=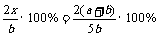 故B项正确。
故B项正确。
1.D 2.BD 3.BD 4.D 5.D 6.B
讲析:1.第一步反应:C(s)+H2O(g)
 CO(g)+H2(g) ;△H>0,是吸热反应,降低温度平衡左移;生成的CO量少,不利于提高CO的转化率,故①不对。增大CO 浓度,其转化率也不可能提高。此题选D。 2.应注意化学平衡移动原理和化学反应速率理论的应用范围。B中加催化剂只能提高反应速率。D中合成氨的反应是放热反应,升高温度反应速率加快,平衡左移。 3.寒冷季节易诱发关节疼痛,说明降低温度易形成尿酸钠晶体,则反应②是放热反应,故选BD。 4.平衡气体平均相对分子质量为2×4.25=8.5,而向右反应结果,物质的量增加,平均相对分子减小。根据平衡中可逆反应的不完全转化特征n(A)>
CO(g)+H2(g) ;△H>0,是吸热反应,降低温度平衡左移;生成的CO量少,不利于提高CO的转化率,故①不对。增大CO 浓度,其转化率也不可能提高。此题选D。 2.应注意化学平衡移动原理和化学反应速率理论的应用范围。B中加催化剂只能提高反应速率。D中合成氨的反应是放热反应,升高温度反应速率加快,平衡左移。 3.寒冷季节易诱发关节疼痛,说明降低温度易形成尿酸钠晶体,则反应②是放热反应,故选BD。 4.平衡气体平均相对分子质量为2×4.25=8.5,而向右反应结果,物质的量增加,平均相对分子减小。根据平衡中可逆反应的不完全转化特征n(A)>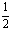 n(平),故M(A)<2M(平)=17。 5.根据固定体积的密闭容器内温度不变,混合气体的压强增大和“X”浓度减小,可知化学平衡向正反应方向移动,得4+3<2+n,n>5,据选项可知n=6。
n(平),故M(A)<2M(平)=17。 5.根据固定体积的密闭容器内温度不变,混合气体的压强增大和“X”浓度减小,可知化学平衡向正反应方向移动,得4+3<2+n,n>5,据选项可知n=6。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com