
13、[答案]B
[解析]醋酸在稀释时会继续电离,则在稀释相同体积的过程中醋酸中的H+大、pH小,A项错误;随着稀释体积的增大,醋酸电离程度虽增大,但离子浓度在减小,B项正确;温度一定,任何稀的水溶液中的Kw都是一定值, C项错误;由于醋酸是弱酸,要使盐酸和醋酸溶液pH值相同,醋酸的浓度比盐酸大得多,D项错误。
[考点分析]本题考查了弱电解质溶液稀释时有关量的变化与分析。
12、[答案]D
[解析]加入催化剂同时改变正、逆反应速率,A项错误;若是恒容条件,增加不参与反应的气体而使反应体系的压强增大,由于浓度不变,反应速度就不变,B项错误;降低温度使反应速率降低,将增大反应达到平衡的时间,C项错误;根据计算平均速率的定义公式可得D项正确。
[考点分析]本题主要是对影响化学反应速率的因素进行了考查。
11、 [答案]A
[答案]A
 [解析] KAl(SO4)2·12H2O电离出的Al3+能水解,生成Al(OH)3胶体,可用作净水剂,A正确;金刚石能够与氧气发生反应,生成二氧化碳,B错误;浓H2SO4有强氧化性,在加热条件下与Cu可剧烈反应,C错误;SO2使品红溶液褪色,加热颜色能复原;SO2和溴水发生氧化还原反应,加热不能恢复原来颜色,D错误。
[解析] KAl(SO4)2·12H2O电离出的Al3+能水解,生成Al(OH)3胶体,可用作净水剂,A正确;金刚石能够与氧气发生反应,生成二氧化碳,B错误;浓H2SO4有强氧化性,在加热条件下与Cu可剧烈反应,C错误;SO2使品红溶液褪色,加热颜色能复原;SO2和溴水发生氧化还原反应,加热不能恢复原来颜色,D错误。
 [考点分析]盐类水解、氧化还原反应综合考查
[考点分析]盐类水解、氧化还原反应综合考查
10、 [答案]D
[答案]D
 [解析]CCl4可由CH4和氯气光照取代制得,可萃取碘水中的碘,A正确;石油和天然气的主要成分都是烃,B正确;向乙醇、乙酸和乙酸乙酯分别加入饱和Na2CO3溶液分别现象为:互溶;有气泡产生;溶液分层,可以鉴别,C正确;苯虽不能使KMnO4溶液褪色,但可以燃烧,能发生氧化反应,D错误。
[解析]CCl4可由CH4和氯气光照取代制得,可萃取碘水中的碘,A正确;石油和天然气的主要成分都是烃,B正确;向乙醇、乙酸和乙酸乙酯分别加入饱和Na2CO3溶液分别现象为:互溶;有气泡产生;溶液分层,可以鉴别,C正确;苯虽不能使KMnO4溶液褪色,但可以燃烧,能发生氧化反应,D错误。
 [考点分析]有机物的性质、基本反应类型、有机物鉴别的综合考查
[考点分析]有机物的性质、基本反应类型、有机物鉴别的综合考查
9、 [答案]B
[答案]B
 [解析]处于元素周期表金属与非金属分界线附近的元素,既表现金属性,又表现非金属性,A错误;主族元素的最高正化合价等于它所处的主族序数,也等于其最外层电子数,B正确;H+的最外层电子分别是0,C项错误;同一主族的元素的原子最外层电子数虽相同,但是核电荷数、原子半径不同,化学性质不完全相同学,D错误。
[解析]处于元素周期表金属与非金属分界线附近的元素,既表现金属性,又表现非金属性,A错误;主族元素的最高正化合价等于它所处的主族序数,也等于其最外层电子数,B正确;H+的最外层电子分别是0,C项错误;同一主族的元素的原子最外层电子数虽相同,但是核电荷数、原子半径不同,化学性质不完全相同学,D错误。
 [考点分析]物质结构、元素周期律的综合考查。
[考点分析]物质结构、元素周期律的综合考查。
8、[答案]C
[解析]Cl2中的氯元素化合价为0处于中间价态,既有氧化性又有还原性,A错误;同位素原子的质子数和电子数分别相等,所以化学性质几乎完全相同,B错误;通过实验室制得的Cl2中含有少量HCl, Cl2在饱和食盐水中溶解度很小,而HCl,易溶,C正确;没有指明气体所处状态, D错误。
[考点分析]考查基本概念、基本理论、实验室制法等
7、 答案D
答案D
 [解析]A项,NO与O2混合后会发生反应,分子数将减少,故错;B项,乙烷中含有7根共价键,可以作出乙烷的结构式数,错;C项,氯化钠为离子晶体,不存在小分子,错。D项,CO32 -水解,1mol可以水解生成2molOH-,故阴离子总数变大,正确。
[解析]A项,NO与O2混合后会发生反应,分子数将减少,故错;B项,乙烷中含有7根共价键,可以作出乙烷的结构式数,错;C项,氯化钠为离子晶体,不存在小分子,错。D项,CO32 -水解,1mol可以水解生成2molOH-,故阴离子总数变大,正确。
6、[答案]B
[解析]合金是两种或两种以上的金属或金属与非金属熔合而成的,A正确;光导纤维主要成分是SiO2 ,属于无机物,B错误;加热会使蛋白质发生变性,C正确;在车排气管上加装“催化转化器”能将有毒的CO和NO转化为无毒的CO2和N2,D正确。
[考点分析]化学基本概念、化学与生活、化学与社会的综合考查。
13.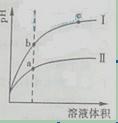
 某温度下,相同pH值的盐酸和醋酸溶液分别加水稀释,平衡pH值随溶液体积
某温度下,相同pH值的盐酸和醋酸溶液分别加水稀释,平衡pH值随溶液体积 变化的曲线如右图所示。据图判断正确的是
变化的曲线如右图所示。据图判断正确的是
 A.Ⅱ为盐酸稀释时pH值变化曲线
A.Ⅱ为盐酸稀释时pH值变化曲线
 B.b点溶液的导电性比c点溶液的导电性强
B.b点溶液的导电性比c点溶液的导电性强
 C.a点Ka的数值比c点Ku的数值大
C.a点Ka的数值比c点Ku的数值大
 D.b点酸的总浓度大于a点酸的总浓度
D.b点酸的总浓度大于a点酸的总浓度
12. 2SO2(g)+O2(g)
2SO2(g)+O2(g)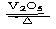 2SO3(g)是制备硫酸的重要反应。下列叙述正确的是
2SO3(g)是制备硫酸的重要反应。下列叙述正确的是
 A.催化剂V2O5不改变该反应的逆反应速率
A.催化剂V2O5不改变该反应的逆反应速率
 B.增大反应体系的压强,反应速率一定增大
B.增大反应体系的压强,反应速率一定增大
 C.该反应是放热反应,降低温度将缩短反应达到平衡的时间
C.该反应是放热反应,降低温度将缩短反应达到平衡的时间
 D.在t1、l2时刻,SO3(g)的浓度分别是c1,c2,则时间间隔t1-t2内,SO3(g)生成的平均速率为
D.在t1、l2时刻,SO3(g)的浓度分别是c1,c2,则时间间隔t1-t2内,SO3(g)生成的平均速率为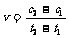
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com