
28、(4分)电解原理在化学工业中有广泛的应用。如图
如果用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
①X电极的材料是___________,电极反应是_________________________。
②Y电极的材料是____________,电极反应是_________________________。
四 计算题(9分)
26.(6分)氯化铁水解的离子方程式为 ___________________________________________
向氯化铁溶液中加入碳酸钙粉末,发现碳酸钙逐渐溶解,并产生无色气体,其离子方程式为 ____________________________________________________________________-
 同时有红褐色沉淀生成,其原因是____________________________________27、(6分)两套如图所示装置,各盛有2g锌粒(颗粒大小相同)分别加入40ml 1mol/L和40ml 4mol/L的硫酸,比较二者收集10ml H2时所用的时间。
同时有红褐色沉淀生成,其原因是____________________________________27、(6分)两套如图所示装置,各盛有2g锌粒(颗粒大小相同)分别加入40ml 1mol/L和40ml 4mol/L的硫酸,比较二者收集10ml H2时所用的时间。
(1)当收集到10mlH2时,哪个实验所耗时间较长?为什么?
_________________________。
(2)活塞外移的情况是
A、均匀外移 B、先快后慢
C、先慢后快 D、先慢后快然后又逐渐减慢
 你选择的理由是__________________________________________________
你选择的理由是__________________________________________________
 __________________________________________________。
__________________________________________________。
25. (6分)可逆反应:aA(g)+
bB(g)
(6分)可逆反应:aA(g)+
bB(g)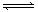 cC(g)+ d D(g);根据图回答:
cC(g)+ d D(g);根据图回答:
(1)压强 P1比P2 (填大或小);(2)(a +b)比(c +d) (填大或小);
(3)温度t1℃比t2℃ (填高或低);(4)正反应为_____________反应。(填放热或吸热)
24.(2分)将足量BaCO3分别加入:① 30mL 水 ②10mL 0.2mol/LNa2CO3溶液 ③50mL 0.01mol/L 氯化钡溶液 ④100mL 0.01mol/L盐酸中溶解至溶液饱和。请确定各溶液中Ba2+的浓度由大到小的顺序为:(用序号表示)
_____
23.已知化学反应A(g)+2B(s) 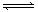 C(g)+3D(g)在25C0 时的平衡常数为40,在该温度下向1升密闭容器中加入1 molA、0.2
molB、1 molC、2 molD.则反应开始时V(正)_________V(逆)(填大于,小于或等于)
C(g)+3D(g)在25C0 时的平衡常数为40,在该温度下向1升密闭容器中加入1 molA、0.2
molB、1 molC、2 molD.则反应开始时V(正)_________V(逆)(填大于,小于或等于)

22.(2分)阿司匹林的结构式为 ,可溶性阿司匹林疗效比阿司匹林更佳,写出制备可溶性阿司匹林的化学反应方程式.
,可溶性阿司匹林疗效比阿司匹林更佳,写出制备可溶性阿司匹林的化学反应方程式.
______________________________________________________________________________
21.用已知浓度的盐酸滴定未知浓度的NaOH溶液会导致测得的NaOH溶液浓度偏高的是( )
A.滴定前滴定管中有气泡,滴定后消失
B.碱式滴定管量取NaOH溶液时,未进行润洗操作
C.滴定时达到滴定终点时仰视读数
D.锥形瓶取用NaOH待测液前加少量水洗涤
第Ⅱ卷(非选择题,共37分)
20.用物质的量均是0.1 mol的CH3COOH和CH3COONa配成1L混合溶液,已知其中c(CH3COO-)大于c(Na+),对该混合溶液的下列判断正确的是( )
A.c(H+)>c(OH-)
B.c(CH3COO-)+c(CH3COOH)=0.1 mol·L-1
C.c(CH3COOH)>c(CH3COO-)
D.c(CH3COO-)+c(OH-)=0.1 mol·L-1
19.在下列各微粒中,能使水的电离平衡向正方向移动,而且溶液的pH大于7是( )

18、燃料电池是利用燃料(如H2、CO、CH4等)跟氧气或空气反应,将化学能转化成电能的装置,电解质溶液是强碱。下面关于甲烷燃料电池的说法正确的是
 A、负极反应为:O2+2H2O+4e- =4OH-;
A、负极反应为:O2+2H2O+4e- =4OH-;
B、负极反应为:CH4+10OH- - 8 e-=CO32-+7H2O
C、放电时溶液中的阴离子向负极移动;
D、随放电的进行,溶液的pH值不变
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com