
3、斜抛运动的速度
在任意时刻两个方向的速度分别为vx=v0cosθ
vy= v0sinθ-gt 物体的实际速度(即合速度)为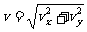 方向根据两个分速度决定。
方向根据两个分速度决定。
2、斜抛运动的位置
我们以斜向上抛为例,与平抛类似建坐标系,如图。
因为vx=vcosθ,vy=vsinθ。所以x=vcosθ·t

1、两个分运动
我们可以把斜向初速度分解为水平方向和竖直方向,水平方向由于不受力,仍然做匀变速直线运动,竖直方向由于受到重力作用,做的是加速度为g的竖直上抛或竖直下抛运动。
2、竖直分速度vy=gt
 3、
3、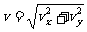 与水平方向的夹角为
与水平方向的夹角为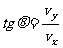 。
。
根据平抛运动在水平方向和竖直方向的规律,可以求出物体在任意时刻水平方向和竖直方向的速度为vx=v vy=gt。物体在任意时刻的速度(即合速度)可以按照勾股定理求得,由图可得
1、水平分速度vx=v0
2、平抛运动的位移
(1)水平位移x=vt
(2)竖直位移 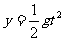
(3)合位移S= ,与水平方向的夹角
,与水平方向的夹角 tanθ=
tanθ=
做平抛运动的物体由于水平方向不受力的作用,根据牛顿第一定律,物体在水平方向做的是匀速运动;在竖直方向,物体没有初速度,但受到重力作用,所以物体在竖直方向做的是自由落体运动。
 如果以水平方向为x轴,以竖直向下为y轴,以抛出点为坐标原点建立坐标系,并从这一时刻开始计时,则物体在任意时刻的坐标为:x=vt (1)
如果以水平方向为x轴,以竖直向下为y轴,以抛出点为坐标原点建立坐标系,并从这一时刻开始计时,则物体在任意时刻的坐标为:x=vt (1) 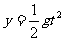 (2)
(2)
由(1)(2)两式消去t可以得到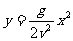 ,对于一个具体的平抛运动,v和g是常数,所以这是初中学过的抛物线方程,即:
,对于一个具体的平抛运动,v和g是常数,所以这是初中学过的抛物线方程,即:
1、平抛运动的轨迹是一段抛物线。
23.有三种不同质量比的氧化铜与炭粉的混合物样品①、②、③。甲、乙、丙三同学各取一种样品,加强热充分反应,测定各样品中氧化铜的量。
(1)甲取样品①强热,若所得固体为金属铜,将其置于足量的稀硝酸中微热。产生1.12L气体(标准状况),则样品①中氧化铜的质量为 g。
(2)乙取样品② a g强热,生成的气体不能使澄清的石灰水变浑浊。再将反应后固体与足量的稀硝酸微热,充分反应后,有b g固体剩余,该剩余固体的化学式为 。样品②中氧化铜质量为 g(以含a、b的代数式表示)。
(3)丙称量样品③强热后剩余的固体,质量比原样品减小了c g,若该固体为金属铜,
则样品③中氧化铜物质的量(n)的取值范围为 。
22.(1)下列有关实验的叙述中,正确的是 。
A.用碱式滴定管量取25.00 mL 溴水
B.不宜用瓷坩埚灼烧氢氧化钠或碳酸钠
C.测定溶液的pH时用干燥.洁净的玻璃棒蘸取溶液,点在用蒸馏水润湿过的pH试纸上,再与标准比色卡比较
D.圆底烧瓶、锥形瓶、烧杯加热时都应垫上石棉网
E.使用容量瓶配制溶液时,俯视刻度线定容后所得溶液浓度偏高
F.滴定用的锥形瓶和滴定管都要用所盛溶液润洗
(2)为测定Na2SO3与Na2CO3的混合物中Na2CO3的含量,取23.2g样品按下图装置(铁架台、铁夹等仪器在图中未画出)进行实验。已知C中装有品红溶液。
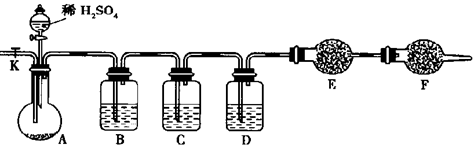
实验室备有的常见试剂:a.浓硫酸 b.品红溶液 c.酸性高锰酸钾溶液
d.饱和碳酸氢钠溶液 e.氢氧化钠溶液 f.无水硫酸铜 g.碱石灰
① C的作用是 ,
F的作用是 ;
② 请将下列容器中应盛放的试剂序号填入相应的空格:
B ,D ,F ;
③实验过程中,当A中的固体反应完全后,需打开活塞K,向A中通入大量的空气,这样做的目的是 。所通入的空气应先经过装有 试剂(从上述试剂中选,填序号)的洗气瓶处理,否则可能引起Na2CO3的含量比实际值 。(填“偏高”、“偏低”或“无影响”)
④若仪器E在实验完成时增重4.4g,则混合物中Na2CO3的质量分数为 。
21.在一定条件下,在一个容积固定的反应器中,有一可左右滑动的密封隔板,两侧进行如图所示的反应(均加有适量的新型固体催化剂,其体积可忽略不计)
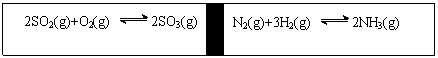
(1)若起始时两边分别投入2 mol SO2、1 mol O2;1 mol N2、3 mol H2,达到平衡后,隔板是否能处于正中间 (填“可能”或“不可能”)。
(2)若起始时投入2 mol SO2、1 mol O2;1 mol N2、2 mol H2,达到平衡后,隔板仍处于正中间,则SO2的转化率和N2的转化率之比为 (填数字);
(3)若起始时投入2 mol SO2、1 mol O2;1 mol N2、a mol H2、0.1 mol NH3,起始时右侧体积小于左侧体积,当a值在一定范围内变化时,均可通过调节反应器温度,使左右两侧反应都达到平衡,且平衡时隔板处于正中间,此时SO2的转化率与N2的转化率之比为5:1,求a的取值范围 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com