
16. 如图所示的电路,水平放置的平行板电容器中有一个带电液滴正好处于静止状态,现将滑动变阻器的滑片
如图所示的电路,水平放置的平行板电容器中有一个带电液滴正好处于静止状态,现将滑动变阻器的滑片 向左移动,则
向左移动,则
A.电容器中的电场强度将增大
B.电容器上的电荷量将减少
C.电容器的电容将减少
D.液滴将向上运动
15. 如图所示,电阻R和电动机M串联接到电路中。巳知电阻R跟电动机线圈电阻相等,开关闭合后,电动机正常工作。设电阻R和电动机两端的电压分别为U1和U2,经过时间t后,电源通过电阻R做功W1,产生的电热为Q1;电流通过电动机M做功W2,产生的电热为Q2。则有
如图所示,电阻R和电动机M串联接到电路中。巳知电阻R跟电动机线圈电阻相等,开关闭合后,电动机正常工作。设电阻R和电动机两端的电压分别为U1和U2,经过时间t后,电源通过电阻R做功W1,产生的电热为Q1;电流通过电动机M做功W2,产生的电热为Q2。则有
A.U1<U2,Q1>Q2
B. W1=W2,Q1=Q2
C.W1<W2,Q1<Q2
D. U1<U2,Q1=Q2
14. 如图所示,实线是电磁场,虚线是等势面,相邻两等势面之
如图所示,实线是电磁场,虚线是等势面,相邻两等势面之
间的电势差相等,一个正电荷在等势面P处时的动能为20J,当
运动到等势面N时动能为零。现取O面为零电势参考平面,则
当此电荷的电势能为4J,它的动能为(不计重力)
A.4J B.6J C.16J D.24J
13. A、B两个点电荷在真空中所产生电场的电场线(方向未标出)如图所示.图中C点为两点电荷连线的中点,MN为两点电荷连线的中垂线,D为中垂线上的一点,电场线的分布关于MN左右对称.则下列说法中不正确的是
A、B两个点电荷在真空中所产生电场的电场线(方向未标出)如图所示.图中C点为两点电荷连线的中点,MN为两点电荷连线的中垂线,D为中垂线上的一点,电场线的分布关于MN左右对称.则下列说法中不正确的是
A.这两个点电荷一定是等量异种电荷
B.这两个点电荷一定是等量同种电荷
C.C、D两点的电势一定相等
D.C点的电场强度比D点的电场强度大
12.汽车的启动电源常用铅蓄电池,放电时的电池反应如下:
PbO2 + Pb + 2H2SO4 = 2PbSO4↓+ 2H2O,根据此反应判断下列叙述中正确的是:
A.PbO2是电池的负极
B.负极的电极反应式为:Pb + SO – 2e – = PbSO4↓
– 2e – = PbSO4↓
C.PbO2得电子,被氧化
D.电池放电时,溶液酸性增强
11.下列是某同学对相应反应的离子方程式所作的评价,其中评价合理的是:
|
编号 |
化学反应 |
离子方程式 |
评价 |
|
A |
碳酸钙与醋酸反应 |
CO32-+2CH3COOH = CO2↑+ H2O+2CH3COO- |
错误,碳酸钙是弱电解质,不应写成离子形式 |
|
B |
苯酚钠溶液中通入少量CO2 |
C6H5O-+ CO2
+ H2O → C6H5OH + HCO3- |
错误,通入少量CO2应生成CO32- |
|
C |
NaHCO3的水解 |
HCO3-+H2O CO32-+H3O+ CO32-+H3O+ |
正确 |
|
D |
等物质的量的FeBr2和Cl2反应 |
2Fe2+ + 2Br-+ 2Cl2 = 2Fe3+ + Br2
+ 4Cl- |
正确 |
285.8 kJ·mol-1
B.已知C(石墨,s)=C(金刚石,s) △H>0,则金刚石比石墨稳定
C.含20.0g NaOH的稀溶液与稀醋酸完全中和,放出28.7kJ的热量,则稀醋酸和稀NaOH溶液反应的热化学方程式为:
NaOH(aq)+CH3COOH(aq)=CH3COONa(aq)+H2O(l) △H=-57.4 kJ·mol-1
D.己知2C(s)+2O2(g)=2CO2(g) △H1;2C(s)+O2(g)=2CO(g) △H2,则△H1>△H2
10.下列有关热化学方程式的叙述正确的是:
A.已知2H2(g)+O2(g)=2H2O(l) △H=-571.6 kJ·mol-1,则氢气的燃烧热为
9.进行化学实验,观察实验现象,通过分析推理得出正确的结论是化学学习方法之一。下列对有关实验事实的解释正确的是
A.溴水中通入SO2后,颜色褪去,说明SO2表现了漂白性
B.用惰性电极电解相同浓度的Cu(NO3)2和AgNO3混合溶液,阴极首先析出的是Ag,说明Ag+ 的还原性比Cu2+ 强
C.常温下,将铝片放入浓硫酸中无明显现象,说明铝不和冷的浓硫酸反应
D.浓硝酸在光照条件下变黄,说明浓硝酸易分解生成有色产物且溶于浓硝酸
8.阿伏加德罗常数约为NA,下列说法中正确的是:
 A.2g重水(D2O,D为
A.2g重水(D2O,D为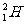 )中含有的中子数0.1NA
)中含有的中子数0.1NA
B.2.24L Cl2(标准状况)跟足量NaOH溶液反应,转移的电子数为0.2 NA
C.32 g S8单质中含有的S-S键个数为NA(S8分子模型如图)
D.1L 1mol·L-1 H2SO3溶液中的离子总数为3NA
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com