
2、下列词语中没有错别字的一组是 ( )
A.渡假 甘拜下风 不假思索 名门旺族
B.厮打 箭拔弩张 凭心而论 鞭辟入里
C.妨碍 永保青春 两全齐美 琳琅满目
D.靓妆 蜂拥而至 文恬武嬉 顾名思义
1、下列各组词语中加点的读音,完全相同的一组是 ( )
A.煎熬 翩跹 信笺 歼击机 草菅人命
B.渎职 赎罪 案牍 小牛犊 穷兵黩武
C.对峙 窒息 挚友 滞纳金 栉风沐雨
D.偏僻 裨益 辅弼 庇护权 刚愎自用
36.(18分) 如图所示,A、B为两块平行金属板,A板带正电、B板带负电。两板之间存在着匀强电场,两板间距为d、电势差为U,在B板上开有两个间距为L的小孔。C、D为两块同心半圆形金属板,圆心都在贴近B板的O’处,C带正电、D带负电。两板间的距离很近,两板末端的中心线正对着B板上的小孔,两板间的电场强度可认为大小处处相等,方向都指向O’。半圆形金属板两端与B板的间隙可忽略不计。现从正对B板小孔紧靠A板的O处由静止释放一个质量为m、电量为q的带正电微粒(微粒的重力不计),问:
如图所示,A、B为两块平行金属板,A板带正电、B板带负电。两板之间存在着匀强电场,两板间距为d、电势差为U,在B板上开有两个间距为L的小孔。C、D为两块同心半圆形金属板,圆心都在贴近B板的O’处,C带正电、D带负电。两板间的距离很近,两板末端的中心线正对着B板上的小孔,两板间的电场强度可认为大小处处相等,方向都指向O’。半圆形金属板两端与B板的间隙可忽略不计。现从正对B板小孔紧靠A板的O处由静止释放一个质量为m、电量为q的带正电微粒(微粒的重力不计),问:
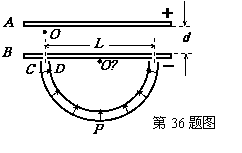 ⑴微粒穿过B板小孔时的速度多大;
⑴微粒穿过B板小孔时的速度多大;
⑵为了使微粒能在CD板间运动而不碰板,CD板间的电场强度大小应满足什么条件;
⑶从释放微粒开始,经过多长时间微粒会通过半圆形金属板间的最低点P点?
35. (18分)如图所示,一质量为m、带电量为q的小球,用绝缘细线悬挂在水平向右的匀强电场中,静止时悬线向左与竖直方向成θ角,重力加速度为g。
(18分)如图所示,一质量为m、带电量为q的小球,用绝缘细线悬挂在水平向右的匀强电场中,静止时悬线向左与竖直方向成θ角,重力加速度为g。
⑴判断小球带何种电荷
⑵求电场强度E
⑶若在某时刻将细线突然剪断,剪断细线后小球做什么运动?
并求经过t时间小球的速度v。
34.(共18分)
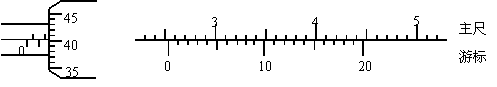
(1)(6分)如图所示,螺旋测微器的读数为 mm;游标卡尺的读数为 cm。
(2)(12分)测量额定电压为2.5V的小灯泡在0-2.5V电压下的实际功率和电阻值,备有下列器材:
A.待测小灯泡:额定电压为2.5V,额定电流约为0.3A
B.电压表:0-3-15V;0-3V量程的内电阻为3kΩ,0-15V量程的内电阻为15kΩ
C.电流表:0-0.6-3A;0-0.6A量程的内电阻为0.13Ω,0-3A量程的内电阻为0.025Ω
D.电池组:电动势约3V,内电阻不详;
E.滑动变阻器:最大阻值为20Ω, 额定电流2A;
F.电键,导线若干.
①根据本实验的需要,电流表应当选用 量程.
②按照实验要求,用笔连线代替导线,将图中的器件连接成完整实验电路.
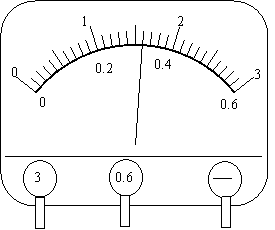 ③当电压表示数为2.50V时,电流表示数如图所示,则这个小灯泡在额定电压下的实际功率为 W,灯丝电阻为 Ω(保留两位有效数字)
③当电压表示数为2.50V时,电流表示数如图所示,则这个小灯泡在额定电压下的实际功率为 W,灯丝电阻为 Ω(保留两位有效数字)

31.(17分)利用废铁丝、硫酸铜废液(含硫酸亚铁)和被有机物污染的废铜粉制备硫酸铜晶体。生产过程如下:

试回答下列问题:
(1)铁丝在投入硫酸铜废液前需用稀H2SO4进行处理,可能发生反应的离子方程式有
。
(2)废铜粉与还原所得铜粉混合灼烧,检验发现灼烧后得到的是CuO和少量Cu的混合物。原因是:①灼烧不充分Cu未被完全氧化。
②CuO被还原。该还原反应的化学方程式是 。
(3)为了使灼烧后的氧化铜混合物充分酸溶,在加入稀H2SO4的同时,还通入O2。通入O2的目的是(用化学反应方程式表示)
(4)直接向氧化铜混合物中加入浓硫酸并加热进行酸溶,也可达到充分酸溶的目的,但实际操作中较少使用,原因可能是
 32(16分)磷酸(H3PO4)在溶液中能够以H3PO4、H2PO4-、HPO42-、和PO43-四种粒子形式存在,当溶液的pH发生变化时,其中任一种粒子的物质的量占四种粒子总物质的量的分数δ也可能发生变化。下图是H3PO4溶液中,各种粒子的物质的量分数δ随pH的变化曲线: 1表示H3PO4;2表示H2PO4-;3表示HPO42-;4表示PO43-
32(16分)磷酸(H3PO4)在溶液中能够以H3PO4、H2PO4-、HPO42-、和PO43-四种粒子形式存在,当溶液的pH发生变化时,其中任一种粒子的物质的量占四种粒子总物质的量的分数δ也可能发生变化。下图是H3PO4溶液中,各种粒子的物质的量分数δ随pH的变化曲线: 1表示H3PO4;2表示H2PO4-;3表示HPO42-;4表示PO43-
(1)设磷酸总浓度为c(总),写出c(总)与各含磷粒子浓度间的关系式
。
(2)向Na3PO4溶液中逐滴滴入稀盐酸,当pH从9降到6的过程中发生的主要反应的离子方程式为 。当pH=7时,溶液中主要存在的阴离子(OH-离子除外)是 。
(3)从图中推断NaH2PO4溶液呈 性(填“酸”、“碱”、或“中”),其原因是
。
(4)在Na3PO4溶液中,c(Na+)/ c(PO43-) 3(填“>”、“==”、或“<”);向该溶液中滴入几滴浓KOH溶液后,c(Na+)/ c(PO43-)的值减小,原因是 。
33(14分)在一固定容积的密闭容器中进行着如下反应:
CO2(g) + H2(g) 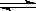 CO(g) + H2O(g)
CO(g) + H2O(g)
其平衡常数K和温度t的关系如下:
|
t℃ |
700 |
800 |
850 |
1000 |
1200 |
|
K |
2.6 |
1.7 |
1.0 |
0.9 |
0.6 |
(1)K的表达式为: ;(2)该反应的正反应为 反应(“吸热”或“放热”);
(3)能判断该反应是否已经达到化学平衡状态的是:
A.容器中压强不变 B.混合气体中CO浓度不变
C.v(H2)正 = v(H2O)逆 D.c(CO2) = c(CO)
(4)在850℃时,可逆反应:CO2(g) +
H2(g) 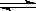 CO(g) + H2O(g),在该容器内各物质的浓度变化如下:
CO(g) + H2O(g),在该容器内各物质的浓度变化如下:
|
时间/min |
CO2 (mol/L) |
H2 (mol/L) |
CO (mol/L) |
H2 O (mol/L) |
|
0 |
0.200 |
0.300 |
0 |
0 |
|
2 |
0.138 |
0.238 |
0.062 |
0.062 |
|
3 |
c1 |
c2 |
c3 |
c3 |
|
4 |
c1 |
c2 |
c3 |
c3 |
计算:3min-4min达到平衡时CO的平衡浓度c3和CO2 (g)的转化率,要求写出简单的计算过程(c3精确到小数点后面三位数)。
30.(17分)(1)化学实验必须注意安全,下列做法存在安全隐患的是 (选填序号)。
A.氢气还原氧化铜实验中,先加热氧化铜后通氢气
B.蒸馏石油时,加热一段时间后发现未加碎瓷片,立刻拨开橡皮塞并投入碎瓷片
C.实验室做钠的实验时,余下的钠屑投入到废液缸中
D.配制浓硫酸与酒精混合液时,将1体积的酒精倒入3体积的浓硫酸中
E.皮肤上沾有少量浓硝酸时,立刻用大量水冲洗,再涂上稀碳酸氢钠溶液
F.制乙烯时,用量程为300℃的温度计代替量程为200℃的温度计,测反应液的温度
(2)工业制备高锰酸钾是锰的重要化合物和常用的氧化剂。以下是工业上用软锰矿制备高锰酸钾的一种工艺流程。
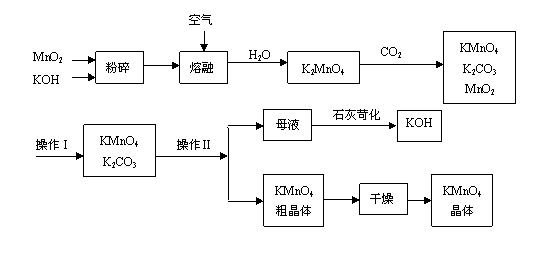

①KMnO4稀溶液是一种常用的消毒剂。其消毒原理与下列物质相同的是______(填代号)。
a、84消毒液(NaClO溶液) b、双氧水 c、苯酚 d、75%酒精
②高锰酸钾保存在棕色试剂瓶,下列试剂保存不需要棕色试剂瓶的是_______(填代号)。
a、浓硝酸 b、 硝酸银 c、氯水 d、烧碱
③上述流程中可以循环使用的物质有 、 (写化学式)。
④若不考虑物质循环与制备过程中的损失,则1 mol MnO2可制得 mol KMnO4。
⑤该生产中需要纯净的CO2气体。若实验室要制备纯净的CO2,所需试剂最好选择(选填代号) 。a、石灰石 b、稀HCl c、稀H2SO4 d、纯碱
⑥操作Ⅰ的名称是 ;操作Ⅱ根据KMnO4和K2CO3两物质在 (填性质)上的差异,采用 (填操作步骤)、趁热过滤得到KMnO4粗晶体。
29.(14分) 某自花传粉植物的紫苗(A)对绿苗(a)为显性,紧穗(B)对松穗(b)为显性,黄种皮(D)对白种皮(d)为显性,各由一对等位基因控制。假设这三对基因是自由组合的。现以绿苗紧穗白种皮的纯合品种作母本,以紫苗松穗黄种皮的纯合品种作父本进行杂交实验,结果F1表现为紫苗紧穗黄种皮。
请回答:
(1)如果生产上要求长出的植株一致表现为紫苗紧穗黄种皮,那么播种F1植株所结的全部种子后,长出的全部植株是否都表现为紫茵紧穗黄种皮?为什么?
(2)如果需要选育绿苗松穗白种皮的品种,那么能否从播种F1植株所结种子长出的植株中选到?为什么?
(3)如果只考虑穗型和种皮色这两对性状,请写出F2代的表现型及其比例。
(4)杂交失败,导致自花受粉,则子代植株的表现型为 ,基因型为 ;
28.(18分)鸭蛋蛋壳的颜色主要有青色和白色两种。金定鸭产青色蛋,康贝尔鸭产白色蛋。为研究蛋壳颜色的遗传规律,研究者利用这两个鸭群做了五组实验,结果如下表所示。
|
杂交组合 |
第1组 |
第2组 |
第3组 |
第4组 |
第5组 |
|
|
康贝尔鸭♀×金定鸭♂ |
金定鸭♀×康贝尔鸭♂ |
第1组的F1自交 |
第2组的F1自交 |
第2组的F1♀×康贝尔鸭♂ |
||
|
后代所产蛋(颜色及数目) |
青色(枚) |
26178 |
7628 |
2940 |
2730 |
1754 |
|
白色(枚) |
109 |
58 |
1050 |
918 |
1648 |
请回答问题:
(1)根据第1、2、3、4组的实验结果可判断鸭蛋壳的 色是显性性状。
(2)第3、4组的后代均表现出 现象,比例都接近 。
(3)第5组实验结果显示后代产青色蛋的概率接近 ,该杂交称为 ,用于检验 。
(4)第1、2组的少数后代产白色蛋,说明双亲中的 鸭群混有杂合子。
(5)运用 方法对上述遗传现象进行分析,可判断鸭蛋壳颜色的遗传符合孟德尔的 定律。
27.(16分)智能温室无土栽培作物,易于管理,优质高产。该项技术广泛应用于现代农业。
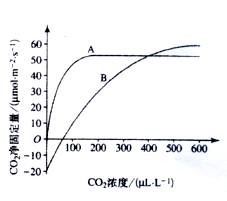
(1)下图表示A、B两种植物的光照等其他条件适宜的情况下,光合作用强度对环境中CO2浓度变化的响应特性。据图判断在CO2浓度为300μL·L-1 (接近大气CO2浓度)时,光合作用强度较高的植物是_______________。
(2)若将上述两种植物幼苗置于同一密闭的玻璃罩中,在光照等其他条件适宜的情况下,一段时间内,生长首先受影响的植物是____________,原因是____________。
(3)当植物净固定CO2量为0时,表明植物____________________。
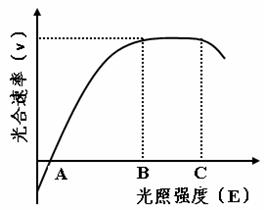
(4)下图表示温室内光照强度(E)与作物光合速率(v)的关系。在温度、水分和无机盐均适宜的条件下,当E<B时,增大光合速率的主要措施是____________;当B<E<C时,限制作物增产的主要因素是____________;当E>C时,可采取____________措施,保证作物的最大光合速率。如遇连阴天,温室需补光,选用____________光最有效。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com