
10.下列溶液中,微粒的物质的量浓度关系正确的是
A.1.0 mol·L-1的Na2CO3溶液:c(OH-)= c(HCO3-) +c(H+)+2 c(H2CO3)
B.1.0 mol·L-1的NH4Cl溶液:c(NH4+)= c(Cl-)
C.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:
c(Na+) > c(CH3COO-)> c(H+)> c(OH-)
D.向硝酸钠溶液中滴加稀盐酸,得到pH=1的混合溶液:c(Na+) = c(NO3-)
9.
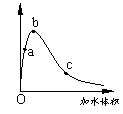 一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如右图所示,下列说法正确的是
一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如右图所示,下列说法正确的是
A.a、b、c三点溶液的pH:c<a<b
B.a、b、c三点醋酸的电离程度:a<b<c
C.用湿润的pH试纸测量a处溶液的pH,测量结果偏小
D.a、b、c三点溶液用1mol/L氢氧化钠溶液中和,消耗氢氧化
钠溶液体积:c<a<b
8.下列离子方程式书写正确的是
A.NaHCO3的水解:HCO3-+H2O CO32-+H3O+
CO32-+H3O+
B.向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至恰好沉淀完全:
Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3·H2O+ H2O
C.向Ca(ClO)2溶液中通入适量SO2 : Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO
D.Fe(OH)3溶于氢碘酸:Fe(OH)3 + 3 H+ = Fe3+ + 3 H2O
7.下列实验操作会导致实验结果偏高的是
A.配制100 g 10%的CuSO4溶液,称取10 g 硫酸铜晶体溶于90 g水中
B.配制100mL 0.1 mol·L-1 NaCl溶液,用托盘天平称量时药品与砝码位置放颠倒了,游码读数为0.2 g
C.配制100mL 2 mol·L-1的稀硫酸,用酸式滴定管量取98%的浓H2SO4时先平视后仰视
D.测定碳酸钠晶体中结晶水的百分含量时,所用的晶体已经受潮
6.短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为13。X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍或者是Y原子最外层电子数的3倍。则下列有关说法中正确的是
A.X的氢化物溶于水显酸性 B.Y的氧化物是离子化合物
C.Z的氧化物的水化物一定是强酸
D.X和Z的最高价氧化物对应的水化物都是弱酸
不定项选择题:包括6小题,每小题4分共计24分。每小题有一个或两个选项符合题意。
5.正在载入...
55
55555
下列有关实验操作正确的是
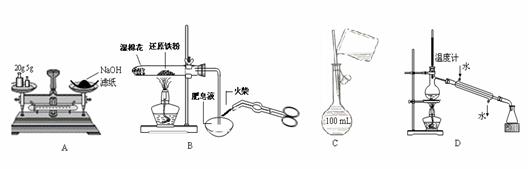
A.称量氢氧化钠固体 B.检验铁粉与水蒸气反应产生的氢气
C.配制150 mL 0.10 mol·L-1盐酸 D.分离两种沸点相差较大的液体互溶混合物
4.下列各组离子在指定溶液中一定能大量共存的是
A.酸性溶液中:Fe2+、Al3+、NO3-、I-、Cl-
B.pH=13的溶液中:CO32-、Na+、AlO2-、NO3-
C.加入Al能放出H2的溶液中:Cl-、HCO3-、NO3-、NH4+
D.在由水电离出的c(OH-)=10-13mol·L-1的溶液中:Na+、Ba2+、ClO-、NO3-
3.已知2-丁烯有顺、反两种异构体,在某条件下两种气体处于平衡:
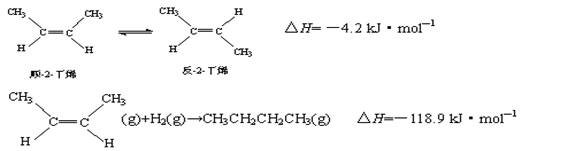
下列说法正确的是
A.顺-2-丁烯比反-2-丁烯稳定
B.顺-2-丁烯的燃烧热比反-2-丁烯大
C.加压和降温有利于平衡向生成顺-2-丁烯反应方向移动
D.反-2-丁烯氢化的热化学方程式为: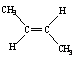 (g)+H2(g)→CH3CH2CH2CH3(g)
△H=-123.1 kJ·mol
(g)+H2(g)→CH3CH2CH2CH3(g)
△H=-123.1 kJ·mol
2.用NA表示阿伏加德罗常数的值,下列叙述中正确的是
A.常温常压下,1 mol甲基(-CH3)所含的电子数为10NA
B. 500 mL 0.2 mol/L的K2S溶液中含有的离子总数为0.3 NA
C.1 mol C10H22分子中共价键总数为32 NA
D.标准状况下,2.24L氯气与氢氧化钠溶液完全反应转移的电子数为0.1 NA
1.目前有研究表明,过氧乙酸对甲型H1N1流感病毒有较好的杀灭作用,这主要是利用了过氧乙酸的
A.酸性 B.强氧化性 C.还原性 D.挥发性
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com