
20.(8分)三氧化二铁和氧化亚铜都是红色粉末,常用作颜料。某校化学实验小组通过实验来探究一红色粉末是Fe2O3、Cu2O或二者混合物。探究过程如下:
查阅资料:(1)Cu2O是一种碱性氧化物,, 溶于稀硫酸生成Cu和CuSO4 (2)Cu2O在空气中加热生成CuO (3)2 Fe3+ + Cu = 2 Fe2+ + Cu2+
提出假设
假设1:红色粉末是Fe2O3 假设2:红色粉末是Cu2O
假设3:红色粉末是Fe2O3和Cu2O的混合物
设计探究实验:
取少量粉末放入足量稀硫酸中,在所得溶液中再滴加 KSCN 试剂。
⑴若假设1成立,则实验现象是 。
⑵若滴加 KSCN 试剂后溶液不变红色,能否能证明固体粉末中不含Fe2O3?
⑶若溶液中还有固体存在 , 滴加 KSCN 试剂时溶液不变红色 , 继续滴加几滴新制的氯水后溶液也不变红色,则证明原固体粉末是 。
探究延伸:经实验分析,确定红色粉末为Fe2O3和Cu2O的混合物。
⑷实验小组欲用加热法测定Cu2O的质量分数。取a g固体粉末在空气中充分加热,待质量不再变化时,称其质量为bg(b > a),则混合物中Cu2O的质量分数为 。
19. (6分)将含有Ag+、Mg2+、Al3+、Na+等离子的100 mL稀溶液,按下列实验步骤逐一进行分离。填写下列空白(各步可使用的试剂限于在NaOH、CO2、NaCl中选择)
(6分)将含有Ag+、Mg2+、Al3+、Na+等离子的100 mL稀溶液,按下列实验步骤逐一进行分离。填写下列空白(各步可使用的试剂限于在NaOH、CO2、NaCl中选择)
(1)沉淀A是 ,沉淀C是
(2)加入试剂①是 ,②是
(3)滤液D中通入过量的③,发生的有关反应的化学方程式为_____________________________
18.在FeO、Fe2O3和CaCO3的混合物中,已知铁元素的质量分数为56%,则CaCO3的质量分数可能是
A.10% B.25% C.30% D.35
第II卷(非选择题,共54分)
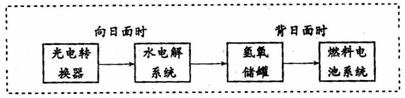
17.下图是某空间站能量转化系统的局部示意图,其中燃料电池采用KOH为电解液,
 下列有关说法不正确的是
下列有关说法不正确的是
A.该能量转化系统中的水可以循环利用
B.燃料电池系统产生的能量实际上来自于水
C.燃料电池工作一段时间后,溶液的pH下降
D.燃料电池放电时的正极反应:O2 + 4e- + 2H2O=4OH-
16.对于两三种有机物形成的混合物,要确定其组成或体积比常用平均式量法或平均化学式法。下面是高中阶段某同学归纳的例题,其中推理不严谨的是( )
A.两种气态烃形成的混合气体0.1mol ,完全燃烧生成0.16mol CO2和3.6g水,则一定有甲烷,可能有乙烯或丙炔。
B.常温下两种气态烃混合气体0.1mol ,完全燃烧生成0.2mol CO2和2.7g水,则一定有乙炔,可能有乙烯或乙烷。
C.常温下一种烯烃和炔烃形成的混合气体相对氢气的密度为13.5,则一定是由乙炔和乙烯组成
D.一定条件下三种炔烃组成的混合气体相对氢气的密度为20, 则一定有乙炔,而丙炔则不能确定。
15.醋酸溶液中存在电离平衡CH3COOH
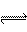 H++CH3COOˉ,下列叙述不正确的是
H++CH3COOˉ,下列叙述不正确的是 
A.醋酸溶液中离子浓度的关系满足:c(H+)=c(OHˉ)+c(CH3COOˉ)
B. 0.10mol/L的CH3COOH溶液中加水稀释,溶液中所有离子浓度都减小
C. CH3COOH溶液中加少量的CH3COONa固体,平衡向左移动
D.常温下pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合后,溶液的pH<7
14. 六苯乙烷为白色固体,其结构表示如图:
六苯乙烷为白色固体,其结构表示如图:
下列有关说法中不正确的是( )
A.它是一种芳香烃,易溶于一般的有机溶剂
B.它的分子式为C38H30,是非极性分子
C.它的一氯代物只有4种
D.所有碳原子一定不在同一平面上
13.要鉴别己烯中是否混有少量甲苯,正确的实验方法是 ( )
A.先加足量的酸性高锰酸钾溶液,然后再加入溴水
B.先加适量溴水,然后再加入酸性高锰酸钾溶液
C.点燃这种液体,然后再观察火焰的颜色
D.加入浓硫酸与浓硝酸后加热
12.下列操作中,能证明溴乙烷中含溴原子的是
A.取少量溴乙烷,加足量AgNO3溶液
B.取少量溴乙烷,加足量HNO3和AgNO3混合溶液
C.取少量溴乙烷,加NaOH溶液加热后,再加AgNO3溶液
D.取少量溴乙烷,加NaOH溶液加热后,再加过量HNO3和AgNO3混合溶液
11.下列说法正确的是( )
A.标准状态下,22.4L已烷所含分子的物质的量约为1mol
B.烷烃、烯烃、炔烃、芳香烃在一定条件下均可与Cl2反应
C.C20H42一定属于烷烃,其密度可能比水大
D.聚四氟乙烯能使酸性高锰酸钾溶液褪色
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com