
22.4L·mol-1是标准状况下的气体摩尔体积。在不同的温度和压强下,气体摩尔体积的数值也会发生变化。例如,在273℃、101kPa条件下,Vm约为44.8L·mol-1。①请判断101kPa、50℃时的Vm比22.4 L·mol-1______________(填“大”或“小”)②标准状况下,67.2L气体的物质的量为_______________mol。③已知KClO3在MnO2催化、101kPa、210℃时即可分解得到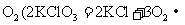 );现将
);现将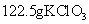 在
在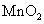 催化、101kPa条件下加热至273℃。若完全分解,则可以得到标准状况下的O2_________________L。
催化、101kPa条件下加热至273℃。若完全分解,则可以得到标准状况下的O2_________________L。
(2)反应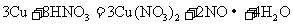 的离子方程式为:
的离子方程式为:
_______________________________________________________________________。
每生成11.2L标准状况下的气体,转移电子的物质的量为__________________mol。
23.(1)气体摩尔体积是指在一定温度和压强下,单位物质的量的气体所占的体积。
22.有5瓶白色固体试剂,分别是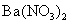 、
、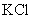 、
、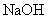 、
、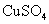 、
、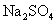 ,现只提供蒸馏水通过下面的实验步骤可鉴别它们。请填写下列空白:
,现只提供蒸馏水通过下面的实验步骤可鉴别它们。请填写下列空白:
(1)各取适量固体试剂分别加入5支试管中,加入适量蒸馏水,振荡试管,观察到的现象是_______________________________________。
被检出的物质的化学式(分子式)是________________________
(2)分别取未检出液,往其中加入上述已检出的溶液,观察到的现象和相应的离子方程式
①现象:试管中有白色沉淀生成,离子方程式为:________________________。
②现象:试管中有蓝色沉淀生成,离子方程式为:________________________。
(3)最后可利用试剂_________________(填化学式)鉴别余下未检出的物质
21.某气体,它由三原子分子构成,该气体的体积为VL(标准状况下),它的摩尔质量为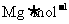 ,若阿伏加德罗常数用
,若阿伏加德罗常数用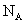 表示,则:
表示,则:
(1)该气体的物质的量为_____________mol。
(2)该气体的质量为_________________g。
(3)该气体所含原子总数为______________个。
(4)该气体在标准状况下的密度为_______________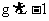 。
。
(5)该气体溶于水后形成aL溶液(该气体和不水反应),其溶液的物质的量浓度为_______________mol/L。
20.为除去粗盐中的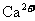 、
、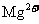 、
、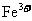 、
、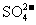 以及泥沙等杂质,某同学设计了一种纸杯精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
以及泥沙等杂质,某同学设计了一种纸杯精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
称取粗盐 滤液
滤液 精盐
精盐
(1)判断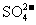 已除尽的方法是_________________。
已除尽的方法是_________________。
(2)操作②为什么不用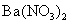 溶液?
溶液?
其理由是_____________________________________________________。
(3)第④步中,相关的离子方程式是________________________________________。
第⑥步中,相关的离子方程式是___________________________________________。
(4)实验室进行⑦步NaCl溶液蒸发时,一般有以下操作过程①放置酒精灯;②固定铁圈位置;③放上蒸发皿(蒸发皿中盛有NaCl溶液);④加热搅拌;⑤停止加热。其正确的操作顺序为________________________。
(5)为检验精盐纯度,需配制250mL0.2mol/L NaCl(精盐)溶液,如图是该同学转移溶液的示意图,图中的错误是__________________________。
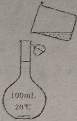
(6)配制NaCl溶液时,若出现下列操作,其结果偏高还是偏低?
A.称量NaCl时已潮解
B.天平的砝码已锈蚀
C.定容摇匀时,液面下降又加水
D.定容时俯视刻度线
19.下列A、B、C、D是中学常见的混合物分离或提纯的基本装置。

根据混合物分离或提纯的原理,回答下列实验中需要使用哪种装置。将A、B、C、D填入适当的空格中。
(1)除去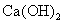 溶液中悬浮的
溶液中悬浮的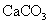 _____________;
_____________;
(2)从碘水中提取碘___________________;
(3)分离植物油和水____________________;
(4)与海水晒盐原理相符的是________________;
(5)分离乙醇和氯化钠溶液__________________,
18.已知浓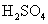 和
和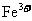 都可以将Cu氧化成
都可以将Cu氧化成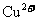 ,浓
,浓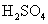 也可以将
也可以将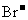 氧化成
氧化成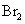 ,Fe与
,Fe与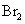 反应生成
反应生成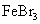 。由此可以确定上述有关物质氧化性由强到弱的顺序为
。由此可以确定上述有关物质氧化性由强到弱的顺序为
A.浓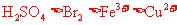 B.浓
B.浓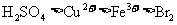
C.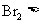 浓
浓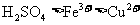 D.
D.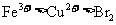
 浓
浓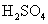
第II卷 非选择题(共46分)
17.被称为万能还原剂的NaBH4(NaBH4中H为-1价)能溶于水并和水反应,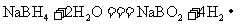 ,下列有关该反应的说法中,正确的是
,下列有关该反应的说法中,正确的是
A.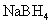 既是氧化剂又是还原剂
既是氧化剂又是还原剂
B.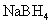 是氧化剂,
是氧化剂,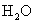 是还原剂
是还原剂
C.硼元素被氧化,氢元素被还原
D.被氧化的元素与被还原的元素质量比为1:1
16.铁和水蒸气在加热条件下发生反应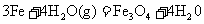 ,在此反应中水是
,在此反应中水是
A.氧化剂 B.还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
15.能用 来表示的化学反应
来表示的化学反应
A.氢氧化镁和稀盐酸反应
B.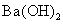 溶液滴入稀硫酸中
溶液滴入稀硫酸中
C.澄清石灰水和稀硝酸反应 D.二氧化碳通入澄清石灰水中
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com