
7、2003年,美国在未经联合国安理会授权的情况下,攻打主权国家伊拉克,遭到包括俄、德、法等国在内的许多国家的反对,这一事件主要反映了
A.“一超多强”的局面被打破 B.多极化趋势不断加强
C.联合国维护和平的作用加强 D.世界总趋势走向缓和
6、“从世界史的观点来看,美国革命之所以重要,并不是因为它创造了一个独立的国家,而是因为它创造了一个新的、不同类型的国家。”对“新的、不同类型”的正确理解是
A.开创政党政治的先河 B.最早建立责任制内阁政府
C.确立了总统共和制 D.开创了政府首脑选举制度
5、“雄关漫道真如铁,而今迈步从头越。”这是毛泽东在1935年2月写下的《忆秦娥·娄山关》中的一句,其中“从头越”反映了
A.南昌起义,武装反抗国民党反动派 B.进军井冈山,“农村包围城市”
C.遵义会议,红军获得新生 D.长征胜利,红军开始抗战
4、1982年,全国人大通过了修订的《中华人民共和国宪法》。规定“国家在必要时得设立特别行政区,在特别行政区内实行的制度按照具体情况由全国人民代表大会以法律规定。”这一规定说明了“一国两制”
A.构想正式提出 B.是改革开放的指导方针
C.有了法律依据 D.构想得到了成功实践
3、鸦片战争后,李鸿章对中国时局的看法是:“我朝处数千年未有之奇局”“此三千年一大变局也”。这里的“奇局”、“大变局”应指
A.资本主义征服世界的历史潮流 B.列强侵略中国,导致中国社会巨变
C.太平天国波澜壮阔的革命形势 D.中国近代经济结构的变化
2、魏源在19世纪50年代写到,“西方人讲礼貌、正直、有知识,根本不应该称之为 ‘夷’”。四五十年代的许多著作把西方人称为“夷”,但在七八十年代这些著作再版时都改作“洋”了。该变化反映了
A.中国人对西方认识的逐步深入 B.中国人由仇视西方到崇拜西方
C.由中国中心到西方中心的变化 D.对西方外交政策由对抗到和解
1、西周统治者确立嫡长子继承制的出发点是
A.保证王权平稳过渡 B.巩固中央集权
C.维护国家的统一 D.确立等级制度
21.(《物质结构与性质》)
(1)金属镁有许多重要的用途,法国化学家维多克·格利雅因发明了在有机合成方面用途广泛的格利雅试剂而荣获诺贝尔化学奖,格利雅试剂的结构简式可表示为RMgX,它是金属镁和卤代烃反应的产物,简称格氏试剂,它在醚的稀溶液中以单体形式存在,并与二分子醚络合,在浓溶液中以二聚体存在,结构如下图:

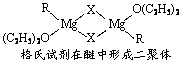
①上述2种结构中均存在配位键,把你认为是配位键的用“→”标出。
②由原子间的成键特点,可以预测中心原子Mg的杂化类型可能为_________;Mg
原子的核外电子排布式可表示为________________________。
③下列比较中正确的是_________________________________
A.金属键的强弱:Mg>Al B.基态原子第一电离能:Mg>Al
C.金属性:Mg>Al D.晶格能:NaCl>MgCl2
|
TiCl4+2Mg=======Ti+2MgCl2
①Ti元素在元素周期表中的位置是 ,钛原子的外围电子排布式为 。
②TiCl4在常温下是无色液体,在水或潮湿空气中易水解而冒白烟。则TiCl4属于 (填“原子”、“分子”或“离子”)晶体。
③二氧化钛作光催化剂能将居室污染物甲醛、苯等有害气体可转化为二氧化碳和水,达到无害化。有关甲醛、苯、二氧化碳及水说法正确的是 。
A. 苯与B3N3H6互为等电子体
B.甲醛、苯分子中碳原子均采用sp2杂化
C.苯、二氧化碳是非极性分子,水和甲醛是极性分子
D.水的沸点比甲醛高得多,是因为水分子间能形成氢键
 (3)2001年报导的硼和镁形成的化合物刷新了金属化合物超导温度的最高纪录。下图中示意的该化合物的晶体结构单元:镁原子间形成正六棱柱,则棱柱的上下底面还各有一个镁原子,六个硼原子位于棱柱内,则该化合物的化学式可表示为
(3)2001年报导的硼和镁形成的化合物刷新了金属化合物超导温度的最高纪录。下图中示意的该化合物的晶体结构单元:镁原子间形成正六棱柱,则棱柱的上下底面还各有一个镁原子,六个硼原子位于棱柱内,则该化合物的化学式可表示为
A.MgB B.MgB2 C.Mg2B D.Mg3B2
20.某自来水中含有Ca2+、Mg2+、Na+、K+、HCO3-、SO42-、Cl-,长期烧煮上述自来水会在锅炉内形成水垢。锅炉水垢不仅耗费燃料,而且有烧坏锅炉的危险,因此要定期清除锅炉水垢。已知部分物质20℃时的溶解度数据为
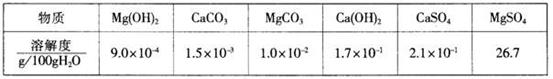
(1)请用化学方程式表示锅炉中的水垢含有Mg(OH)2的原因 。
(2)锅炉中的水垢所含有的CaSO4不能直接用酸除去,需要加入试剂X,使其转化为易溶于盐酸的物质Y而除去。试剂X是 (填序号)。
A.NaCl B. NaOH C.Na2CO3 D.Na2S
CaSO4能转化为物质Y 的原因是(用文字叙述) 。
(3)除含CaSO4、Mg(OH)2外,锅炉水垢中还可能含有的物质是(写化学式) 。
(4)水中的Ca2+、Mg2+可以用一定浓度的M溶液进行测定,M与Ca2+、Mg2+都以等物质的量进行反应。现取含Ca2+浓度为0.40g/L的自来水样10mL,至锥形瓶中进行滴定,达到终点时,用去了浓度为0.01mol/L的M溶液20.00mL,则该自来水样中Mg2+的物质的量浓度是 。
19.相对分子质量为92的某芳香烃X是一种重要的有机化工原料,研究部门以它为初始原料设计出如下转化关系图(部分产物、合成路线、反应条件略去)。其中A是一氯代物,H是一种功能高分子,链节组成为C7H5NO。

已知:
Ⅰ 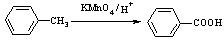
Ⅱ 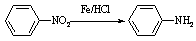 (苯胺,易被氧化)
(苯胺,易被氧化)
请根据所学知识与本题所给信息回答下列问题:
⑴H的结构简式是_______________________________________________;
⑵反应②的类型是 ;
⑶反应⑤的化学方程式是____________________________________________;
⑷ 有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有_____种;
有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有_____种;
⑸请用合成反应流程图表示出由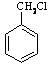 和其他无机物合成
和其他无机物合成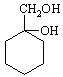 最合理的方案(不超过4步)。
最合理的方案(不超过4步)。
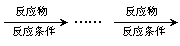 例:
例: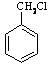

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com