
16. 在物理学的发展过程中,许多物理学家的科学发现推动了人类历史的进步。在对以下几位科学家所作科学贡献的叙述中,下列说法正确的是( )
A. 笛卡尔通过实验测出了引力常量
B. 牛顿提出的万有引力定律奠定了天体力学的基础
C.伽利略发现了行星运动的规律
D.密立根进行了多次实验,比较准确地测定了电子的电量
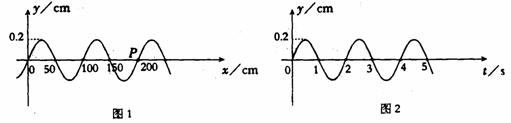
15.图1为一列简谐横波在t=20s时的波形图,图2是这列波中P点的振动图线,那么该波的传播速度和传播方向是 ( )
A.v=25cm/s,向左传播
B.v=50cm/s,向左传播
C.v=25cm/s,向右传播
D.v=50cm/s,向右传播

14、下列说法中正确的是( )
A.1克0℃水的内能比1克0℃冰的内能小
B.热现象过程中不可避免地出现能量耗散现象,能量耗散不符合热力学第二定律
C.随分子间距离增大先只有斥力后只有引力
D.布朗运动的无规则性,反映了液体分子运动的无规则性
13.下列选项中,微粒的物质的量浓度关系正确的是( )
A.0.1mol/L的Na2CO3溶液中:c(OH-)=c(HCO3-)+c(H+)+c(H2CO3)
B.0.1mol/L NH4Cl的溶液与0.05 mol/L的NaOH溶液等体积混合后,得到的pH>7的溶
液中:c(Cl-)>c(Na+)>c(NH4+)>c(OH-)>c(H+)
C.向硝酸钾溶液中滴加稀盐酸得到pH=4的混合溶液:c(K+)=c(NO3-)
D.浓度分别为0.1mol/L和0.01mol/L的CH3COOH溶液中:CH3COO-离子浓度前者是后
者的10倍
12.将一定量的A、B装入容积为1L的恒温密闭容器中,发生反应2A(g) + bB(g) cC(g),1min时达到平衡,C的浓度为x mol/L.若保持温度不变,将密闭容器的容积压缩为原来的一半,重新达到平衡后,C的浓度为1.5x mol/L,下列说法正确的是 ( )
cC(g),1min时达到平衡,C的浓度为x mol/L.若保持温度不变,将密闭容器的容积压缩为原来的一半,重新达到平衡后,C的浓度为1.5x mol/L,下列说法正确的是 ( )
A.化学计量数的关系:b>c
B.容器的容积减小后,该反应的逆反应速率减小
C.原容器中用B的浓度的变化表示该反应在1min内的速率为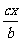 mol·L-1·min-1
mol·L-1·min-1
D.若保持温度和容器不变,充入氦气(不参与反应),平衡不发生移动
11. 向某NaOH溶液中通入CO2气体后得到溶液M,因CO2通入的量的 不同,
向某NaOH溶液中通入CO2气体后得到溶液M,因CO2通入的量的 不同,
溶液M的组成也不同,若向M中加入盐酸,产生的气体体积V(CO2)与加入
盐酸的体积V(HCl) 的关系如图所示.则下列分析与判断不正确的是(不计
CO2的溶解) ( )
A.若OB=0 ,则形成溶液M所发生的离子方程式为OH- + CO2 ===HCO3-
B.若OB=BC,则溶液M为Na2CO3 溶液
C.若OB>BC,则溶液M中大量存在的阴离子为CO32-和HCO3-
D.若3OB=BC,则溶液M中c(NaHCO3)=2c(Na2CO3)
10.下列实验操作或对实验事实的叙述中存在错误的是( ) 
①.用50mL酸式滴定管准确量取25.00mL酸性 KMnO4
溶液,放入锥形瓶中待用
②.在测定硫酸铜晶体的结晶水时,将灼烧硫酸铜晶体的坩埚放在空气 中冷却,然后称量
③.中和热的测定所需的玻璃仪器有烧杯、温度计、量筒
④.配制1 mol/L 的NaOH溶液时,下列操作会造成所配浓度偏低: 溶解后烧杯未多次洗涤; 定容时仰视刻度线; 容量瓶中原有少许蒸馏水
⑤.实验室配制氯化亚铁溶液时,将氯化亚铁先溶解在盐酸中,然后用蒸馏水稀释并加入少量铁粉
A.②③④
B.①②③④

C.②③④⑤
D.①②④
9.NA表示阿伏加德罗常数,下列说法正确的是( )
A.4 g 重水(D2O)中的中子数为1.6 NA
B.标准状况下,2.24L N2和C2H2的混合气体,所含电子总数为1.4NA
C.60g SiO2中Si-O键的个数为2NA
D.0.1mol Fe粉与足量水蒸气反应生成H2的分子数为0.15NA
8.下列离子方程式书写正确的是( )
A.用醋酸除水垢 CaCO3+2H+===Ca2++CO2 +H2O
B.漂白粉在空气中失效 ClO- + CO2 +H20 ===HClO + HCO3-
C.AgNO3溶液中加入过量氨水 Ag+ +NH3·H2O===AgOH +NH4+
D.Na2CO3溶液中通入少量CO2 CO32- +CO2 +H2O===2HCO3-
7.A、B、C、D、E为原子序数依次递增的同一短周期主族元素,下列说法一定正确的是(m为正整数)( )
A.若A、B的最高价氧化物水化物均为碱,则A(OH)m的碱性一定比B(OH)m+1的碱性强
B.若D、E的气态氢化物均溶于水,则E的最高正化合价为+6
C.若C的最低化合价为-3,则E的最高正化合价为+6
D.若B的最高正化合价为+4,则五种元素的单质所形成的晶体都是分子晶体
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com