
1.关于物体的运动,下面说法可能的是 ( )
A.加速度在减小,速度在增加
B.加速度方向始终变而速度不变
C.加速度和速度大小都在变化,加速度最大时速度最小,速度最大时加速度最小
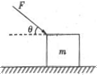 D.加速度方向不变而速度方向变化
D.加速度方向不变而速度方向变化
21.(10分)为了测定某铜银合金的成分,将30.0g该合金溶于80.0mL浓度为13.5mol/L的浓HNO3中,待合金完全溶解后,收集到气体6.72L(标准状况),并测得溶液的c(H+)=1.0mol/L。假设反应后溶液的体积仍为80.0mL,试计算:
(1)被还原的硝酸的物质的量。
(2)合金中铜的质量分数。
(3)6.72L(标准状况)气体的组成。
20.(10分)已知稀溴水和氯化铁溶液都呈黄色,某化学活动小组进行实验探究。
李强、王刚两同学分别在足量的稀氯化亚铁溶液中,加入1-2滴液溴,振荡后溶液呈黄色。
(1)李强同学认为这不是发生化学反应所致,则使溶液呈黄色的微粒是: ▲ (填粒子的化学式);王刚同学则认为这是发生化学反应所致,试写出对应的离子方程式: ▲ 。
(2)如果要验证王刚同学判断的正确性,请根据下面所提供的可用试剂,用两种方法加以验证,请将选用的试剂代号及实验中观察到的现象填入下表。
实验可供选用试剂: A.碘化钾淀粉溶液 B.氢氧化钠溶液 C.硝酸银溶液
D.硫氰化钾溶液 E.四氯化碳 F.酸性高锰酸钾溶液
|
实验方案 |
所选用试剂(填代号) |
实验现象 |
|
方案一 |
▲ |
▲ |
|
方案二 |
▲ |
▲ |
(3)根据上述实验推测,若在稀溴化亚铁溶液中通入少量氯气,则首先被氧化的离子是
▲ (填粒子的化学式);若在稀溴化亚铁溶液中通入过量氯气,则相应的离子方程式为 ▲ 。
19.(10分)海洋是一个远未完全开发的巨大化学资源宝库,海洋资源的综合利用具有非常广阔的前景。工业上从海水中可提取许多种物质,广泛应用于生活、生产、科技等方面。
试回答下列问题:
(1)蒸馏法是人类最早使用的淡化海水的方法。
你认为蒸馏法海水淡化最理想的能源是 ▲ 。
(2)从海水中可得到多种化工原料和产品。下列是海水资源利用的流程图。
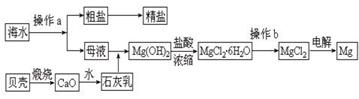
①流程图中操作a的名称为 ▲ 。
②工业上从海水中提取的NaCl,可用来制取纯缄,其简要过程如下:向饱和食盐水中先通入气体A,后通入气体B,充分反应后过滤得到晶体C和滤液D,将晶体C灼烧即可制得纯碱。气体A、B是CO2或NH3,则气体B应是 ▲ 。(填化学式)
③镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。
a.若要验证所得无水MgCl2中不含NaCl,最简单的操作方法是: ▲ 。
b.操作b是在 ▲ 气氛中进行,若在空气中加热,则会生成Mg(OH)Cl,写出有关反应的化学方程式 ▲ 。
c.在母液苦卤中含有较多的NaCl、MgCl2、KCl、MgSO4等物质。用沉淀法测定苦卤中Mg元素的含量(g/L),实验过程中应测定的数据有 ▲ 。
18.(12分)硅和氮均是自然界含量丰富的元素,其单质及其化合物在环境、能源及材料科学中有着重要影响和广泛应用。
试回答下列问题:
⑴向大气中排放NOx可能导致的环境问题有 ▲ (答两点)。已知,足量NaOH溶液能完全吸收NO2生成氮的含氧酸盐,试写出该反应的离子方程式:
▲ 。
⑵光导纤维的使用,让人们的生活更加丰富精彩。 ▲ 是制备光导纤维的基本原料。
⑶氮化硅陶瓷是一种新型无机非金属材料,其化学式为 ▲ ,可由硅粉(用Al2O3和Y2O3作助剂)在氮气中高温烧结而成。由于使用的硅粉表面含二氧化硅,在反应中需加入碳粉。在烧结过程中,二氧化硅、碳、氮气以物质的量之比3:6:2反应生成两种化合物,该反应的化学方程式为 ▲ 。
⑷硅燃烧放出大量热量,“硅能源”有望成为二十一世纪的新能源。与“氢能源”比较,“硅能源”具有 ▲ 等更加优越的特点,从而得到全球的关注和期待。
(5)三硅酸镁(2MgO·3SiO2·nH2O)被用来治疗胃溃疡,是因为该物质不溶于水,服用后能中和胃酸,作用持久。写出三硅酸镁与胃酸(盐酸)反应的化学方程式: ▲ 。
17.(12分)甲、乙、丙、X均为中学常见的纯净物,它们之间有如下转化关系(副产物已略去)
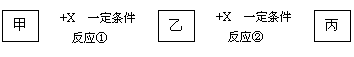
试回答下列问题:
(1)若X是强氧化性单质,则甲可能是 ▲ 。
a.S b.N2 c.Na d.Mg e.Al
(2)若X是金属单质,向丙的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀。则乙的化学式为 ▲ ;丙溶液在贮存时应加入少量X,理由是(用必要的文字和离子方程式表示) ▲ 。
检验此丙溶液中金属元素价态的操作方法是 ▲ 。
(3)若甲、乙、丙为含有金属元素的无机化合物,X为强电解质,甲溶液与丙溶液反应生成乙;反应①的离子方程式为 ▲ ,
或 ▲ 。
16.(8分)2008年5月12日四川汶川发生特大地震,为防止在大灾之后疫病流行,当时,全国各地向灾区紧急运送了大量的各种消毒剂、漂白剂等。
(1)84消毒液因其杀菌率高、杀菌种类多、适用范围广,被普遍使用。其主要成分是次氯酸钠,该物质可与硫化钠溶液作用生成硫酸钠,试写出对应的化学反应方程式:
▲ 。
(2)二氧化氯是目前国际上公认的第四代高效、无毒的广谱消毒剂,它可由KClO3在H2SO4存在下与SO2反应制得。请写出反应的离子方程式:
▲ 。
(3)漂白剂亚氯酸钠(NaClO2)在常温与黑暗处可保存一年,亚氯酸不稳定可分解,反应的离子方程式为:5HClO2 =4ClO2↑+ H+ +Cl-+2H2O。则该反应中氧化剂与还原剂的质量之比为: ▲ 。
(4)过碳酸钠是一种多用途的新型氧系固态漂白剂,化学式可表示为Na2CO3·3H2O2,它具有Na2CO3和H2O2的双重性质。过碳酸钠与下列物质均会发生化学反应而失效,其中过碳酸钠只发生了氧化反应的是 ▲ 。
A.MnO2 B.稀盐酸 C.KMnO4溶液 D.Na2SO3溶液
15.(10分)
资料1.据《重庆晚报》2009.8.12报道:在全民补碘政策实施15年之后的今天,来自民间和医学界自主补碘的呼声越来越高。加碘食盐是“防病”还是“致病”?甲状腺疾病频发是否与碘营养过量有关?中国食盐加碘“一刀切”政策或将面临深层次的调整。
资料2.下表是某食用碘盐包装袋上的部分说明:
|
配 料 |
食盐、碘酸钾、抗结剂 |
|
碘含量 |
35±15mg/kg |
|
储藏方法 |
密封、避光、防潮 |
|
食用方法 |
烹饪时,待食品熟后加入碘盐 |
请回答下列问题:
(1)下列说法正确的是 ▲ 。
A.碘酸钾易挥发 B.高温会导致碘的损失
C.用淀粉就能直接检验碘盐中的碘酸钾 D.碘酸钾可氧化氯化钠
(2)碘酸钾与碘化钾在酸性条件下发生如下反应:KIO3+KI+H2SO4→K2SO4+I2+H2O(未配平)该化学方程式配平后系数依次为 ▲ 。该反应的还原剂为 ▲ ;1mol KIO3完全反应转移的电子总数为 ▲ 。
(3)碘不能多也不能少。已知:I2+2S2O32-=2I-+S4O62-,我校化学兴趣小组测定某食用碘盐中碘的含量。其步骤为:
①准确称取w g食盐,加适量蒸馏水使其完全溶解;②用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;③以淀粉为指示剂,逐滴加入物质的量浓度为1.0×10-3mol·L-1的Na2S2O3溶液20.0mL,恰好反应完全。则所测盐中碘的含量是(以含w的代数式表示) ▲ mg/kg。
14.下列所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是
|
|
a |
b |
c |
|
A |
Al |
AlCl3 |
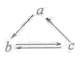 Al(OH)3 Al(OH)3 |
|
B |
NO |
NO2 |
HNO3 |
|
C |
Si |
SiO2 |
H2SiO3 |
|
D |
H2SO4 |
SO2 |
SO3 |
第Ⅱ卷(非选择题 共72分)
13.下列反应的离子方程式书写正确的是
A.硫酸铝溶液中加入过量氨水:Al3++3OH-=Al(OH)3↓
B.在氢氧化钡溶液中逐滴加入硫酸氢钠溶液至恰好呈中性:
Ba2++2OH-+2H++SO42- BaSO4↓+2H2O
C.氨水吸收少量的二氧化硫:NH3·H2O + SO2 = NH4+ + HSO3-
D.向硫酸铜溶液中滴加氢氧化钡溶液至SO4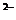 恰好沉淀完全:
恰好沉淀完全:
SO4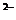 +Ba
+Ba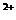 =BaSO4↓
=BaSO4↓
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com