
18.一些烷烃的燃烧热如下表:
|
化合物 |
燃烧热/kJ·mol-1 |
化合物 |
燃烧热/kJ·mol-1 |
|
甲烷 |
890.3 |
正丁烷 |
2878.0 |
|
乙烷 |
1560.8 |
异丁烷 |
2869.6 |
|
丙烷 |
2221.5 |
2-甲基丁烷 |
3531.3 |
下列表达正确的是:
A.乙烷燃烧的热化学方程式为:
2C2H6(g)+7O2(g)=4CO2(g)+6H2O(g) ;△H= -1560.8 kJ·mol-1
B.稳定性:正丁烷﹥异丁烷
C.正戊烷的燃烧热大于3531.3kJ·mol-1
D.相同质量的烷烃,碳的质量分数越大,燃烧放出的热量越多
17.右图装置(X、Y是直流电源的两极)分别进行下列各组实验,则下表中所列各项对应关系均正确的一组是:
|
选项 |
电源X极 |
实验前U形 管中液体 |
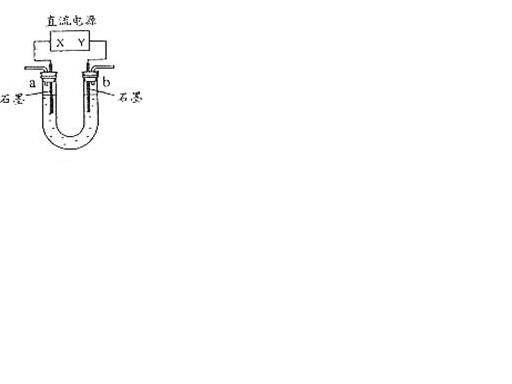 通电后现象及结论 通电后现象及结论 |
|
A |
正极 |
Na2SO4溶液 |
U形管两端滴入酚酞后,a管中呈红色 |
|
B |
正极 |
AgNO3溶液 |
b管中电极反应式是 4OH- -4e-=2H2O+O2↑ |
|
C |
负极 |
KCl和CuCl2混合溶液 |
相同条件下,a、b两管中产生的气体总体积可能相等 |
|
D |
负极 |
Fe(OH)3胶体和导电液 |
b管中液体颜色加深 |
16.以下实验能获成功的是:
A.将卤代烃和氢氧化钠溶液混合加热,充分反应后再加入硝酸银溶液观察沉淀的颜色判断卤素原子
B.将铁屑、溴水、苯混合制溴苯
C.在苯酚溶液中滴入少量稀溴水出现白色沉淀
D.将铜丝在酒精灯加热变黑后,立即伸入无水乙醇中,铜丝恢复成原来的红色
15.下列叙述正确的是:
A.0.1 mo1·L-1一氨水中,c(OH-)=c(NH4+)
B.在常温下,10mL 0.02mo1·L-1的HCl溶液与10mL0.02 mL mo1.L-1的Ba(OH)2溶液
充分混合,若混合后溶液的体积为20mL,则溶液的pH=11
C.在0.1 mol·L-1CH3COONa溶液中,c(OH一)= c(CH3COOH)+c(H+)
D.0.1 mo1·L-1某二元弱酸强碱盐NaHA溶液中,c(Na+) = 2 c(A2-)+c(HA)+c(H2 A)
14.将过量的气体通入到一种溶液中,一定能产生沉淀的是:
①二氧化硫通入到硝酸钡溶液中 ②二氧化碳通入偏铝酸钠溶液中
③二氧化碳通入到氯化钙溶液中 ④氨气通入到AgNO3溶液中
A.只有①②③ B.只有①② C.只有①②④ D.只有②③
13.已知NH4CuSO3与足量的2mol/L硫酸液混合微热,产生下列现象:①有红色金属生成 ②产生刺激性气味的气体 ③溶液呈现蓝色。据此判断下列说法正确的是:
A.反应中硫酸作氧化剂
B.NH4CuSO3中硫元素被氧化
C.1mol NH4CuSO3完全反应转移0.5mol电子
D.刺激性气味的气体是氨气
12.下列离子方程式正确的是:
A.向NaHSO4溶液中滴加过量Ba(OH)2溶液:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O
B.用碳酸钠溶液吸收少量二氧化硫:2CO32-+SO2+H2O=2HCO3-+SO32-
C.向FeCl3溶液中加入铜片:Fe3++Cu=Fe2++Cu2+
D.向碳酸氢钠溶液中加入氢氧化钠:HCO3-+ OH-=CO2↑+H2O
11.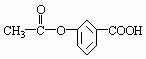 某有机物的结构是:
某有机物的结构是:
关于它的性质的描述正确的是:
①能发生加成反应;②能溶解于NaOH溶液中;③能水解生成两种酸; ④不能使溴水褪色;⑤能发生酯化反应;⑥有酸性
A.①②③ B.②③⑤ C.仅⑥ D.全部正确
10. 用试纸检验气体性质是一种重要的实验方法。如图所示的实验中(右加热),下列试纸的选用、现象、对应结论都正确的一项是:
用试纸检验气体性质是一种重要的实验方法。如图所示的实验中(右加热),下列试纸的选用、现象、对应结论都正确的一项是:
|
选项 |
试剂B |
湿润的试纸A |
现象 |
结论 |
|
A |
碘水 |
淀粉试纸 |
变蓝 |
碘具有氧化性 |
|
B |
浓氨水,生石灰 |
蓝色石蕊试纸 |
变红 |
氨气为碱性气体 |
|
C |
Na2SO3,硫酸 |
品红试纸 |
褪色 |
SO2具有漂白性 |
|
D |
Cu,浓硝酸 |
KI淀粉试纸 |
变蓝 |
NO2为酸性气体 |
9.下列各组离子在溶液中一定能大量共存的是:
A.能使蓝色石蕊试纸变红的溶液: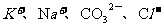
B.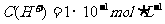 的溶液:
的溶液: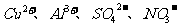
C.能使淀粉-KI试纸变蓝的溶液: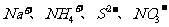
D.水电离出的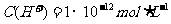 的溶液:
的溶液:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com