
3.(理)若纯虚数z满足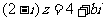 ,则实数b等于(
)
,则实数b等于(
)
A.2 B.8 C。-2 D.-8
(文)从某班学生中任意找出一人,如果该同学的身高小于160cm的概率为0.2,该同学的身高在[160,175]cm的概率为0.5,那么该同学的身高超过175cm的概率为( )
A.0.2 B.0.3 C.0.7 D.0.8
2.已知 的值是( )
的值是( )
A.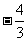 B.
B.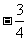 C.
C.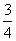 D.
D.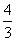
1.已知全集 等于( )
等于( )
A.{1,4} B.{2,6} C.{3,5} D.{2,3,5,6}
23.(1)Ag-e-=Ag+ (2分),PbO2+4H++SO42-+2e-=PbSO4+2H2O(2分)
(2)不变(1分),变大(1分) (3)108 (2分)
23. (8分)某同学查资料得知α-AgI是一种固体导体,导电率很高。他为了研究α-AgI究竟是Ag+ 离子导电还是I- 离子导电,设计一个如下图所示(用铅蓄电池做电源)的电化学实验。已知铅蓄电池总反应:
Pb+PbO2+2H2SO4  2PbSO4+2H2O
2PbSO4+2H2O
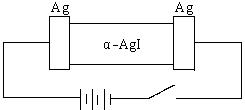
(1)该电解池的阳极电极反应式: ;
铅蓄电池的正极电极反应式: 。
(2)若Ag+ 导电,α-AgI本身质量将 。(填“不变、变大、或变小”)
若I- 导电,阳极附近的α-AgI晶体密度将会 。(填“不变、变大、或变小”)
(3)若通电一段时间后铅蓄电池中消耗了1molH2SO4,则电解池的阴极增重 g。(不要求写计算过程)

22.(10分)为了证明在实验室制备Cl2的过程中会有HCl挥发出来,甲同学设计了如下图所示的实验装置,按要求回答下列问题。
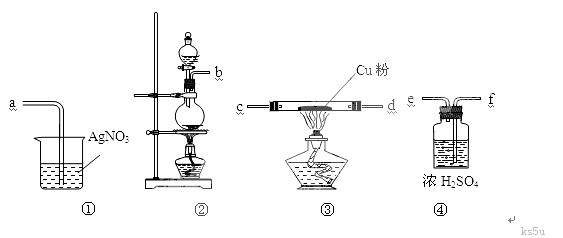
⑴请根据甲同学的意图,连接相应的装置,接口顺序:b接 , 接 , 接a 。
⑵装置中Cu的作用 (用化学方程式表示)。
 ⑶乙同学认为甲同学实验中有缺陷,不能证明最终通入AgNO3溶液中的气体只有
⑶乙同学认为甲同学实验中有缺陷,不能证明最终通入AgNO3溶液中的气体只有
一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液中的气体只有一
种,乙同学提出在某两个装置之间再加装置⑤。
你认为装置⑤应加在 之间(填序号)。瓶中可以放入
。如果实验结论可靠,应观察到的现象:
。
⑷丙同学看到乙同学设计的装置后提出无需多加装置,只需将原来烧杯中
的AgNO3溶液换掉。你认为应将溶液换成 ,如果观察
到 的现象,则说明甲的实验不可靠。
21.(14分)有一瓶澄清的溶液,其中可能含有 NH4+、K+、Na+、Mg2+、Ba2+、Al3+、
MnO4-、Cl-、I-、NO3-、CO32-、S2-、SO42-、、SO32-、AlO2-中的几种。取该溶液进行以下实验:
(1)取pH试纸检验,溶液呈强酸性,可排除 离子的存在。
(2)取出部分溶液,加入少量CCl4及数滴新制氯水,经振荡CCl4层呈紫红色,可排除 离子的存在。
(3)另取部分溶液,逐滴向其中加入NaOH溶液,使溶液从酸性逐渐变为碱性,在滴加过程中和滴加完毕后,均无沉淀产生。则又可排除 离子的存在。
(4) 取部分上述碱性溶液加Na2CO3溶液后,有白色沉淀生成,证明有 离子存在,又可排除 离子的存在。
(5)将(3)得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。
根据上述五步实验事实确定:①该溶液中肯定存在的离子是 ;②还不能确定是否存在的离子是_____________。
20.(14分)有A、B、C、D、E、F、G七种元素,试按下述所给的条件推断。
①A、B、C是同一周期的金属元素,已知原子核外有3个电子层,A的原子半径在所属周期中最大,且原子半径A>B>C。
②D、E是非金属元素,它们跟氢化合可生成气态氢化物HD和HE,在室温时,D的单质是液体,E的单质是固体。
③F在常温下是气体,性质稳定,是除氢外最轻的气体。
④G是除氢外原子半径最小的元素(不考虑稀有气体)。
(1)A的名称 ;B位于周期表中第__周期,第 族;C的原子结构示意图是 。
(2)E的单质颜色是 。
(3)A元素与D元素形成的化合物的电子式是 。
(4)G的单质与水反应的化学方程式是 。(5)F的元素符号是 。
(6)在上述七种元素中,最高价氧化物对应的水化物碱性最强的物质的化学式是 ;气态氢化物最稳定的物质的化学式是 。
(7)将C的氧化物对应的水化物投入到A的氧化物对应的水化物中反应的离子方程式是 。
19. (4分)下列说法正确的是________(选填字母) A.在进行物质检验时,一般先对试样进行外观观察,确定其状态、颜色、气味 等 B.一般在实验室点燃可燃性气体时,必须先要检验纯度 C.实验室制取氯气等有毒气体时,必须在密闭体系或通风橱中进行 D.中和热测定实验时,如果没有环形玻璃棒,可用环形铜质搅拌棒代替。 E.测定硫酸铜晶体结晶水的质量分数时,若用潮湿的坩埚会使测定结果偏大 F.可用过滤法除去氧氢化铁胶体中少量的氯化铁和盐酸。
18.(8分) 对于密闭容器中的反应:
N2(g)+3H2(g)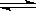 2NH3(g);△H <0,
2NH3(g);△H <0,
在673K,30MPa下n(NH3)和n(H2)随时间变化
的关系如右图所示。
(1).正反应速率点a处的比点b处的 ________ 。(填“大、小或相等”)
(2).点 c处的正反应速率比逆反应速率 ________。(填“大、小或相等”)
(3).点d (t1时刻) 的n(N2)______(填“大于、小于或等于”)点 e (t2时刻) 处的n(N2)。
(4).其他条件不变,773K下反应至t1时刻,此时画出的两根平行线间的距离将要变 ________ 。 (填“大、小或相等”)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com