
7.(天津市2009年中考化学冲刺模拟题八)将10g某物质溶解于90g水中形成溶液,所得的溶液中溶质质量分数是
A.一定等于10% B.一定大于10%
C.一定小于10% D.三种情况均有可能
6.(2009年甸南二中月考)20℃时,氯化钠的溶解度是36克。把20g氯化钠中加入 50g水,充分溶解后,溶液中溶质的质量分数为( )
A.36% B.40% C.26.5% D.28.6%
5、(2009年黄冈市九年级化学月考试题)
在4个小烧杯里分别盛有等质量的下列物质,在空气中放置一段时间后,烧杯内物质的总质量显著增加且溶质质量分数减小的是( )
A.浓盐酸 B.浓硫酸 C.石灰水 D.蔗糖溶液
4.(常州市礼河实验学校调研测试试卷)下列物质分别和等质量、等质量分数的硫酸恰好完全反应后,所得溶液中溶质质量分数最大的是
A.Zn B.Zn(OH)2 C.ZnO D.ZnCO3
3.(南阳市2009年中考模拟试题)
由Mg(OH)2和MgO组成的混合物,测得其中含镁元素的质量分数为48%。取该混合物10g,将其投入110g的稀硫酸中恰好完全反应,所得溶液中溶质的质量分数为............................................................ [ ]
A.12% B.24% C.20% D.30%
2.(天津市南开区2009年中考化学模拟试卷)
农业上常使用溶质质量分数为16%的氯化钠溶液来选种,如果要配制2000g这样的溶液,需要称量氯化钠的质量为
A. 160 g B.320 g C.32 g D.16 g
1.(安丘市2009年中考模拟化学试题)某同学在配制50g溶质量分数为5%的食盐溶液的实验中,称量时将砝码放在左盘(1g以下用游码),食盐放在右盘;量水时仰视液面读数。这样配制的食盐溶液中的质量分数
A.等于5% B.大于5% C.小于5% D.不能确定
42.(太原成成中学九年级第五次月考)在家庭生活中,自来水经过处理后,用途更加广泛。
(1)净水器可以净化自来水,获得更优质的饮用水。①净水器中装有活性炭,其作用是________________;②净水器接通电源时产生紫外线与自来水生产中加氯气的目的相同,其作用是________________。
(2)用自来水养金鱼时为除去其中少量的余氯,可放入少许大苏打(化学式为Na2S2O3·5H2O)。大苏打由___________种元素组成,其中硫元素的化合价为__________。
 (3)水溶液在生产,生活中有着广泛的应用。冬天在汽车的水箱中加入少量乙二醇,可使水溶液的凝固点_____________,以防止水结冰。
(3)水溶液在生产,生活中有着广泛的应用。冬天在汽车的水箱中加入少量乙二醇,可使水溶液的凝固点_____________,以防止水结冰。
专题十四 中考化学中的STS问题
1答案:B
2答案:B
3答案:A
4答案:C
5答案:C
6答案:B
7答案:C
8答案:B
9答案:B
10答案:C
11答案:D
12答案:D
13答案:D
14答案:D
15答案:C
16答案:D
17答案:B
18答案:D
19答案:D
20答案:B
21答案:D
22答案:(1)使聚胺脂的温度达到了着火点
(2)减少有害气体的吸入
(3)装修时加入阻燃剂材料
23答案:(1)提高化石燃料的燃烧效率 开发太阳能、水能、核能等无温室气体排放的能源
(2)①释放 ②CO2 + H2O = H2CO3
24答案:(1)甲 ;3 (2)甲 ;热值和营养成分都高
25答案:(9分)(1)(每空O.5分,共3分)A、F、C、E、H、G
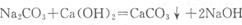
 (2)(每空1分,共4分)CO2、O2或H2、CH3COOH、Ca(OH)2
(2)(每空1分,共4分)CO2、O2或H2、CH3COOH、Ca(OH)2
(3)(每空1分,共2分)
26答案:减小;蛋白质
27答案:(1)①②④ (2)② (3)减少化石燃料的燃烧;多植树造林;开发新能源。
28答案:(1)NO和CO(2)这是一个开发性的问题,可能的答法有如下几类:
A. 限制汽车的数量,如限制私人汽车的数量,大力发展公共交通
B. 将汽车全部加装三效转换器等汽车环保设备,使汽车尾气得到净化。
C. 改用清洁环保型燃料,如酒精、液化气等
D.使用电力汽车
(3)这是一个开放性的问题,可能的答法有如下几种
A. 关于氢气的来源问题,如:如何获得大量而廉价的氢气?
B. 关于氢气的保存和运输问题,如:如何贮存和运输大量的氢气?
C. 关于氢气在汽车上的使用问题,如:汽车上如何安装一定量的氢气?
D. 关于氢气使用的安全性问题,如:如何防止氢气在使用、贮存和运输过程中的安全。
29答案:(1)取样,滴加紫色石蕊试液,观察颜色的变化。
(2)取样,滴加碳酸钠溶液,观察现象;另取样,滴加硫酸铜溶液,观察现象。
30答案:(1)+4; (2)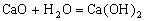 ; (3)45.5;4)浓硫酸具有很强的腐蚀性;
; (3)45.5;4)浓硫酸具有很强的腐蚀性;
(5)取少量该“双吸剂”于试管中,滴加稀盐酸,若有气泡产生,则“双吸剂”还有效;
否则无效。
(1)+4; (2)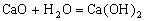 ; (3)45.5;4)浓硫酸具有很强的腐蚀性;
; (3)45.5;4)浓硫酸具有很强的腐蚀性;
(5)取少量该“双吸剂”于试管中,滴加稀盐酸,若有气泡产生,则“双吸剂”还有效;
否则无效。
31答案:(1)B (2)面食,土豆(马铃薯)红薯等。(3)2C3H4O+7O2==6CO2+4H2O
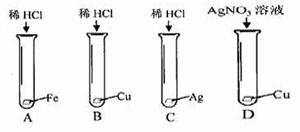
(4 (1)氯化钠溶液,硝酸银溶液 (2) 硝酸银溶液,有白色沉淀生成,氯化钠溶液过量
32答案:⑴物理;过滤;⑵蛋白质、糖类、脂肪;铁;⑶B、D
33答案:凉拌、生食、加醋;避光、避热、密封。
34答案:B
35答案:D
36答案:(1)盖上锅盖;(2)119
37答案:(11分)(1)有机 三 18 66.7%(2)B C (3)铁、铜、金(4) CO2 食醋(或乳酸饮料、酸性果汁等) (5)Fe2O3+6HCl=2FeCl3+3H2O
38答案:(13分)(1)CaCO3 CaO+CO2↑ Mg(OH)2+2HCl=Mg(OH)2↓+2H2O
CaO+CO2↑ Mg(OH)2+2HCl=Mg(OH)2↓+2H2O
②I、Ⅳ、V ③蒸发皿 玻璃棒 (本题答案不分先后顺序) ④电解产生的氯气用于生产HCI(合理答案均给分)
(2)①C ②活泼
(3)①完全反应后生成的固体的质量 有 ②充分反应后生成的氢气的质量(体积)
39答案:(4分) (各1分)⑴糖类、蛋白质 青菜(合理即可) ⑵缺铁性贫血
40答案:(3分) (各1分)⑴ ⑤ ⑵ ② ⑶火力发电厂燃煤生成的二氧化硫直接排放到空气中与水反应形成酸雨。
41答案:(1)① 2Cu + O2 加热 2CuO ; ② CuO + H2SO4 === CuSO4 + H2O ;
③ Fe + CuSO4 === FeSO4 + Cu 。
(第②个方程式“加热”条件不作要求)
(2)乙 。甲方案第一步“灼烧”会产生污染空气的气体、粉尘、烟雾。(关键词:“污染空气”)
(3)“确保CuSO4 用完”或“将Cu完全置换出来”,其他类似说法均可得分。
将所得铜粉酸洗后再洗涤、干燥;或过滤前在加适量的酸以除去剩余的铁粉。(关键词:“加酸”)
(4)蒸发 、降温 。 水污染或环境污染。
(5)4900 ,3060 。将浓硫酸沿玻璃棒加入水中(关键词“浓硫酸加入水中”,答对顺序即得分)。
(6)解:设所能处理的废料中纯铜质量为x。
 2Cu + 2H2SO4 + O2 2CuSO4 + 2H2O
2Cu + 2H2SO4 + O2 2CuSO4 + 2H2O
2×64 2×98
|
2×64 2×98
x 1000mL×1.84g/mL×98%
x = 1177.6g
答:所能处理的废料中含纯铜1177.6克。
42答案:(1)①吸附 ②杀菌消毒 (2)4 +2 (3)降低
41.(2009年江苏省中考化学调研卷一)
某集团是一家以生产电缆类产品为主的国家大型企业。在电缆生产过程中,不可避免地会产生一定量的含铜废料(如:零碎电缆)。某化学兴趣小组的四位同学得知这一情况后,围绕“从含铜废料中回收铜”提出了各自的看法。
甲同学根据已学知识,提出了一套回收方案:

 乙同学在查阅资料后得知:在通入空气并加热的条件下,铜可与稀硫酸在溶液中发生反应(方程式为:2Cu + 2H2SO4
+ O2
2CuSO4 + 2H2O),于是他提出了另一套方案:
乙同学在查阅资料后得知:在通入空气并加热的条件下,铜可与稀硫酸在溶液中发生反应(方程式为:2Cu + 2H2SO4
+ O2
2CuSO4 + 2H2O),于是他提出了另一套方案:

(1)甲方案的①②③三个步骤中,与铜或铜的化合物有关的化学反应方程式分别是:
① ;② ;
③ 。
(2)从环保角度对两套方案的不同部分进行比较,你认为 (填“甲”或“乙”)的方案更合理。理由是: 。
(3)丙认为,无论是甲还是乙的方案,在“加铁屑”这一步时,应该加入略过量的铁屑。你认为丙这么说的道理是: 。(2分)
丁又提出了疑问:“如果铁过量,剩余的铁会混在红色粉末中,该怎么处理呢?”。请提出你的想法: 。
(4)最后,老师肯定了同学们的积极思考,但同时指出:方案最后一步所得浅绿色滤液结晶后,会得到一种俗称“绿矾”的工业产品,可增加经济效益。请写出使“绿矾”结晶的两种可能方法: 、 (“绿矾”溶解度随温度升高而增大)。如果直接排放掉滤液,不仅造成了浪费,还会 。
(5)若上述方案所用的稀硫酸溶质质量分数为36.8%,问每1000mL98%的浓硫酸(密度为1.84g/mL)能配制出这种稀硫酸 g,需水 mL(水的密度为1.0g/mL)。在实验室中稀释浓硫酸时,是如何操作的: 。(2分)
 (6)根据乙同学查出的方程式(2Cu + 2H2SO4
+ O2
2CuSO4 + 2H2O)计算:如果1000mL98%的浓硫酸(密度为1.84g/mL)稀释后全部参加了反应(假设硫酸不和碎电缆皮、其他杂质反应),所能处理的废料中含纯铜多少克?(请写出计算过程,结果精确到0.1克。5分)
(6)根据乙同学查出的方程式(2Cu + 2H2SO4
+ O2
2CuSO4 + 2H2O)计算:如果1000mL98%的浓硫酸(密度为1.84g/mL)稀释后全部参加了反应(假设硫酸不和碎电缆皮、其他杂质反应),所能处理的废料中含纯铜多少克?(请写出计算过程,结果精确到0.1克。5分)
40.(3分)某农场附近新建了一座燃煤火力发电厂后该农场的小麦产量急剧下降。经农场技术员测定:雨水pH约为4、土壤pH约为5。已知一些重要作物最适宜生长的土壤的pH如下表:
|
作物 |
①水稻 |
②小麦 |
③玉米 |
④油菜 |
⑤马铃薯 |
|
pH |
6-7 |
6.3-7.5 |
6-7 |
6-7 |
4.8-5.5 |
⑴根据上表数据,你认为这种土壤最适合种植的作物是(填编号) 。
⑵若继续种小麦,你认为最好选用以下(填编号) 试剂来改良土壤。
①工业盐酸 ②熟石灰 ③纯碱
⑶该地区形成酸雨的主要原因是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com