
20.(14分)有A、B、C、D、E、F、G七种元素,试按下述所给的条件推断。
①A、B、C是同一周期的金属元素,已知原子核外有3个电子层,A的原子半径在所属周期中最大,且原子半径A>B>C。
②D、E是非金属元素,它们跟氢化合可生成气态氢化物HD和HE,在室温时,D的单质是液体,E的单质是固体。
③F在常温下是气体,性质稳定,是除氢外最轻的气体。
④G是除氢外原子半径最小的元素(不考虑稀有气体)。
(1)A的名称 ;B位于周期表中第__周期,第 族;C的原子结构示意图是 。
(2)E的单质颜色是 。
(3)A元素与D元素形成的化合物的电子式是 。
(4)G的单质与水反应的化学方程式是 。(5)F的元素符号是 。
(6)在上述七种元素中,最高价氧化物对应的水化物碱性最强的物质的化学式是 ;气态氢化物最稳定的物质的化学式是 。
(7)将C的氧化物对应的水化物投入到A的氧化物对应的水化物中反应的离子方程式是 。
19. (4分)下列说法正确的是________(选填字母) A.在进行物质检验时,一般先对试样进行外观观察,确定其状态、颜色、气味 等 B.一般在实验室点燃可燃性气体时,必须先要检验纯度 C.实验室制取氯气等有毒气体时,必须在密闭体系或通风橱中进行 D.中和热测定实验时,如果没有环形玻璃棒,可用环形铜质搅拌棒代替。 E.测定硫酸铜晶体结晶水的质量分数时,若用潮湿的坩埚会使测定结果偏大 F.可用过滤法除去氧氢化铁胶体中少量的氯化铁和盐酸。
18.(8分) 对于密闭容器中的反应:
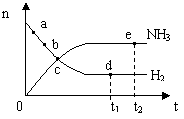
N2(g)+3H2(g)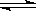 2NH3(g);△H <0,
2NH3(g);△H <0,
在673K,30MPa下n(NH3)和n(H2)随时间变化
的关系如右图所示。
(1).正反应速率点a处的比点b处的 ________ 。(填“大、小或相等”)
(2).点 c处的正反应速率比逆反应速率 ________。(填“大、小或相等”)
(3).点d (t1时刻) 的n(N2)______(填“大于、小于或等于”)点 e (t2时刻) 处的n(N2)。
(4).其他条件不变,773K下反应至t1时刻,此时画出的两根平行线间的距离将要变 ________ 。 (填“大、小或相等”)
17.HgCl2稀溶液可用作手术刀的消毒剂,已知:HgCl2晶体熔点是2270C;HgCl2在
熔融状态下不能导电;HgCl2在水溶液中可发生微弱电离,下列关于HgCl2的叙述
正确的是
①HgCl2属于离子化合物 ②HgCl2属于共价化合物
③HgCl2属于非电解质 ④HgCl2属于弱电解质
A.①③ B.①④ C.②③ D.②④
 第Ⅱ卷(非选择题,共计58分)
第Ⅱ卷(非选择题,共计58分)
16.离子检验常用的方法有三种:
|
检验方法 |
沉淀法 |
显色法 |
气体法 |
|
含义 |
反应中有沉淀产生或溶解 |
反应中有颜色变化 |
反应中有气体产生 |
下列离子检验的方法不合理的是
A.NH4+- 气体法 B.I-- 沉淀法
C.Fe3+- 显色法 D.Ca2+- 气体法
15.X+、Y+、M2+、N2-均为含有一定数目电子的短周期元素的简单离子,离子半
大小关系是:N2->Y+、Y+> X+、Y+> M2+,下列说法正确的是
A.原子半径:N可能比Y大,也可能比Y小
B.M2+、N2-核外电子数:可能相等,也可能不等
C.原子序数:N>M>X>Y
D.碱性:M(OH)2>YOH
14.类推的思维方法在化学学习与研究中有时会产生错误的结论,因此类推的结论最终要经过实践的检验,才能决定其正确与否,下列几种类推结论中错误的是:
①钠与水反应生成NaOH和H2;所有金属与水反应都生成碱和H2
②Fe3O4可写成FeO·Fe2O3;Pb3O4也可写成PbO·Pb2O3
③铝和硫直接化合可以得到Al2S3;铁和硫直接化合也可以得到 Fe2S3
④不能用电解熔融的AlCl3来制取金属铝;也不能用电解熔融的MgCl2来制取金属镁
A.①③④ B.②③④ C.④ D.①②③④
13.下列反应的离子方程式正确且表示复分解反应的是
A.钠跟水的反应:2Na +2H2O = 2Na+ +2OH -+ H2↑
B.次氯酸钙溶液中通入过量CO2:Ca2+ +2ClO- + H2O + CO2 = CaCO3↓+2HClO
C.碳酸氢钠溶液中加入盐酸:HCO3-+ H+ = CO2↑+H2O
D.碳酸氢钙溶液中加入过量的氢氧化钠溶液:HCO3-+OH- = CO32-+H2O
12.化学用语是学习化学的重要工具。下列用来表示物质变化的化学用语中,错误的是
A.钢铁腐蚀时可能发生的正极反应:2H2O + O2 + 4e-= 4OH一
B.明矾水解的离子方程式:Al3+ + 3H2OAl(OH)3 + 3H+
C.向KHSO4溶液中滴入Ba(OH)2溶液至溶液pH=7 :
SO42-+ 2H+ + Ba2++ 2OH- = BaSO4↓+ 2H2O
D.1L 0.5mol·L-1 H2SO4 稀溶液与1L 1mol·L-1 NaOH稀溶液反应放出57.3kJ的热量:H2SO4(aq)+2NaOH(aq) = Na2SO4(aq)+2H2O(1);ΔH=-57.3kJ•mol-1
11.现有常温下的四份溶液:①0.01 mol·L-1CH3COOH;②0.01 mol·L-1HCl;③pH=12的氨水; ④pH=12的NaOH溶液。下列说法正确的是
A.①中水的电离程度最小,③中水的电离程度最大
B.将②、③混合,若使混合液pH=7,则消耗溶液的体积:②>③
C.将四份溶液稀释相同倍数后,溶液的pH:③>④,②>①
D.将①、④混合,若有c(CH3COO-)>c(H+),则混合液一定呈碱性
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com