
15.根据右图所示的A、B、C、D、E五种物质的相互转化关系,按如下要求填写相应的物质和有关反应的化学方程式。

(1)当A是气体单质时,A是 ,B是 ,C是 ,D是 ,E是 。
(2)当A是固体单质时,A是 ,B是 ,C是 ,D是 ,E是 。
答案:(1)N2;NH3;NO;NO2;HNO3;(2)S;H2S;SO2;SO3;H2SO4
解析:根据一系列的转化关系,进行有关物质成分的推断,必须找到合适的突破点。本题已知A是单质,A既能与O2反应,又能与H2反应,应是活泼性不很强的非金属单质。A经两步与O2的反应,产物D应为最高价氧化物。该氧化物对应的水化物E能与位于金属活动顺序表中H之后的金属Cu反应,E应是强氧化性酸,如浓H2SO4或HNO3。和HNO3对应的单质A是气体N2;和H2SO4对应的单质A是固体S。且N和S的氢化物都能跟O2反应,生成N和S的氧化物。知如上推断正确。
提高篇
14.汽车尾气主要含有CO2、CO、SO2、NO及汽油、柴油等物质,这种尾气越来越成为城市空气污染的主要来源,必须予以治理。治理的方法之一是在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂)。它的特点是使CO与NO反应,生成可参与大气生态环境循环的无毒气体,并促使汽油、柴油等物质充分燃烧及SO2的转化。
(1)汽车尾气中NO的来源是 。
A.汽油、柴油中含氮,是其燃烧产物
B.是空气中的N2与汽油、柴油的反应产物
C.是空气中的N2与O2在汽车气缸内的高温环境下的反应产物
D.是汽车高温尾气导致了空气中N2与O2的化合反应
(2)写出CO与NO反应的化学方程式: 。
(3)“催化转化器”的缺点是在一定程度上提高了空气的酸度,其原因是 。
(4)控制或者减少城市汽车尾气污染的方法可以有 。(多选)
A.开发氢能源 B.使用电动车 C.限制车辆行驶 D.使用乙醇汽油
答案:(1)C;(2)2CO+2NO 2CO2+N2;(3)SO2转化为SO3,产生了硫酸酸雾;(4)ABD
2CO2+N2;(3)SO2转化为SO3,产生了硫酸酸雾;(4)ABD
解析:(1)汽车尾气中NO的来源是汽车气缸内火花塞放电引起空气中N2与O2化合生成的,故选C。
(2)CO与NO反应生成的无毒气体是CO2+N2,写出方程式配平就行了。
(3)SO2转化为SO3,产生了硫酸酸雾;
(4)开发氢能源、使用电动车、使用乙醇汽油都能控制或者减少城市汽车尾气污染的,故选ABD。
13.利用图4-3所示装置收集以下8种气体(图中烧瓶的位置不得变化)
①H2 ②Cl2 ③CH4 ④HCl ⑤NH3 ⑥NO ⑦H2S ⑧SO2
(1)若烧瓶是干燥的,则由B口进气收集的气体有________(写序号);
(2)若烧瓶充满水,可收集的气体有________,这时气体由________进入。
(3)若烧瓶是干燥的,则由A口进气,可收集的气体有________。
(4)若在烧瓶内装入浓硫酸使气体干燥,则可用此装置来干燥的气体有________,这时气体由________口进入。
答案:(1)②④⑦⑧(2)①③⑥(3)①③⑤(4)①②③④⑥⑧B
解析:由B口进入适宜于比空气重的气体,由A口进入适宜于比空气轻的气体。
0.0lmol 0.0lmol 0:005mol
故V(气)=(0.0lmol+0.005m01)×22.4L/mol=0.336L
12.硫在加热时能被N2O氧化成SO2,现用3.2g硫粉和224mL(标准状况) N2O在加热条件下充分反应,反应结束后,气体混合物在标准状况下的体积为 ( )
A.112mL B.224mL C.336mL D.448mL
C解析:依题意,有:S+2N2O=2N2+SO2,要计算生成物的体积,首先必须判断哪种的反应物过量。为简化计算,可将有关量转换为物质的量。
n(S)= =0.1mol,n(N2)=
=0.1mol,n(N2)=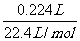 =0.01mol
=0.01mol
由化学方程式可知,0.0lmol N2O可与0.005mol S反应,而n(S)= 0.1mol>0.005mol,所以硫过量,应以N2O的量作计算依据。
S+2N2O=2N2+SO2
11.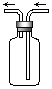 右图是化学实验常用装置之一,若气体从右管进入,可用来收集的气体是 ( )
右图是化学实验常用装置之一,若气体从右管进入,可用来收集的气体是 ( )
A.NO B. NO2 C. CO D.SO2
B D解析:从图中气流方向可知,本装置采用向上排空气法收集气体,气体的密度要比空气大,而NO会与空气中的氧气反应,故选B D。
10.酸雨给人类带来了种种灾祸,严重地威胁着地球生命生存的生态环境,下列有关减少或者防止酸雨形成的措施中可行的是( )
①对燃煤进行脱硫;②对含SO2、NO2等工业废气进行无害处理后,再排放到大气中;③人工收集雷电作用所产生的氮的氧化物;④飞机、汽车等交通工具采用清洁燃料,如天然气、甲醇等。
A.①②③④ B.①②③ C.①②④ D.①③④
C解析:只有③人工收集雷电作用所产生的氮的氧化物是不可行的;
9.(改编)下列气体溶解于水,没有发生氧化还原反应的是( )
A.SO2溶解于水 B.NO2溶解于水 C.F2溶解于水 D.Cl2溶解于水
A解析:NO2溶解于水、F2溶解于水、Cl2溶解于水都发生了氧化还原反应。
8.在常温常压下,下列各组气体不能共存的是 ( )
A.SO2与O2 B.NO2与NO C.O2与N2 D.NO与O2
D 解析:NO与O2反应生成NO2。
7.下列气体中,无色无味的是 ( )
A.SO2 B.NO2 C.Cl2 D.N2
D 解析:SO2、NO2、Cl2都是有气味的气体。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com