
24.(8分)(2005年广东卷)下图中,A、C是工业上用途很广的两种重要化工原料,B为日常生活中常见的金属,H、G是正四面体结构的非极性分子,H是一种重要的能源,J是一 种耐高温材料,K是由两种常见元素组成的化合物(图中部分反应物或生成物没有列出)。
种耐高温材料,K是由两种常见元素组成的化合物(图中部分反应物或生成物没有列出)。
请按要求回答:
(1)写出B的化学式_______________,
G的电子式_________________。
(2)反应①的离子方程式为_______________________________________。
(3)反应③的化学方程式为________________________________________。
23.(6分)已知某溶液中只含有4种离子:A+、B-、H+、OH-,对这4种离子浓度的大小比较,有以下3种说法。请判断离子浓度的大小顺序是否正确,你认为正确的请在相应的空格内填上符合这种情况的A+和B-组成物质的化学式(只写一种情况,可以是一种溶质或两种溶质);你认为一定不正确的,请在相应的空格内填上你选择“不正确”的理由。供选择的离子有:Na+、Ag+、NH4+、Cl-、NO3-、CH3COO-、H+、OH-
(1)c(B-)>c(A+)>c(H+)>c(OH-):
(2)c(A+)>c(B-)>c(OH-)>c(H+):
(3)c(H+)>c(B-)>c(A+) >c(OH-):
22.(10分)以石墨做电极电解200mL 0.5mol/L的CuSO4溶液,在标准状况下,阴极上收集到2.24L气体时,停止通电。请回答下列问题:
(1)电解过程中阴极的电极反应式为 、 ;(2分)
(2)电解过程中共收集到气体的体积为 ;
(3)若电解前后溶液的体积变化忽略不计,电解后溶液的pH值约为 ;
(4)电解结束后,欲使溶液恢复到电解前溶液的组成和浓度,可加入 mol ;(2分)
(5)电解时的电流强度为20安培,理论上所需电解时间为 分。(设1mol电子的电量为96500库仑)
21.(6分)下列三组试剂已失去标签,分别用一种试剂可以鉴别。
A、AlCl3、NaCl、Na2CO3三种溶液
B、Na2CO3、Na2SO4、K2S、Na2SO3、BaCl2、NaAlO2六种溶液;
C、CaC2、NaCl、CuSO4、CaCO3、Al2S3五种固体;
A组可选用 (填名称,下同);
B组可选用 ;
C组可选用 。
20.甲、乙两烧杯中分别盛放500mL等物质的量浓度的稀硫酸,向甲烧杯中加入mg铁粉,向乙烧杯加mg锌粒,完全反应后发现有一烧杯中仍有金属剩余,若H2SO4的物质的量浓度为xmol·L-1,则x的范围是
A. B.
B.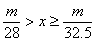
C. D.
D.
第Ⅱ卷(非选择题,共50分)
19.碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌一锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+ H2O(l)=Zn(OH)2(s)+Mn2O3(s)下列说法正确的是
A.电池工作时,锌为正极
B.电池负极的电极反应式为:2MnO2(s)+ H2O(l)+2e-= Mn2O3(s)+2OH-(aq)
C.电池工作时,电子由负极通过外电路流向正极
D.外电路中每通过0.1mol电子,锌的质量理论上减小6.5g
18.下列实验数据记录正确的是
A.用天平称取4.0克NaOH固体,用100ml量筒配制1.0000mol/L的NaOH溶液
B.用25mL的滴定管(内装有标准NaOH溶液)滴定未知浓度的盐酸用去NaOH溶液 22.32mL
C.用pH试纸测得新制氯水的pH为4
D.常温下,用气球收集500mlNO2气体,求得NO2气体的物质的量为0.5/22.4mol
17.已知常温常压和催化剂条件下,N2(g)和H2(g)生成2molNH3(g)放出92.4kJ的热量。在上述条件下向密闭容器中通入1molN2和3molH2,达到平衡时放出热量为Q1kJ;向另一体积相同的容器中通入0.9molN2、2.7molH2和0.2molNH3,相同条件下达到平衡时放出热量为Q2kJ.则下列关系式正确的是
A.2Q=Q1=92.4 B.Q2<Q1<92.4
C.Q1<Q2<92.4 D.Q1=Q2=92.4
16.下列叙述正确的是
A.任何晶体中,若含有阳离子也一定含有阴离子
B.原子晶体中只含有共价键
C.离子晶体中只含有离子键
D.分子晶体中只存在分子间作用力,不含有其它化学键
15.有两种短周期元素X和Y,可以组成XY3,当Y的原子序数为M时,X的原子序数可能为①M-4 ②M+4 ③M+8 ④M-2 ⑤M+6,其中正确的是
A.①②④ B.①②③⑤ C.①②③④⑤ D.①②⑤
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com