
(五)实验假设(实验中可能会得到的结论);
(四)实验中要检测的指标(衡量实验结果的标准);
(三)实验方法(常用对比实验法);
(二)实验原理(实验所应用到的生物学知识或原理);
(一)实验目的(要解决的问题);
30.计算题:
配制1mol·L-1H2SO4溶液200mL需溶质质量分数为98%(ρ=1.84g·/cm3)的浓H2SO4多少毫升?
29.归纳整理是科学学习的重要方法之一。在学习了氧族元素的各种性质后,可归纳整理出如下表所示的表格(部分)。
|
性质\元素 |
8O |
16S |
34Se |
52Te |
|
单质熔点(℃) |
-218.4 |
113 |
|
450 |
|
单质沸点(℃) |
-183 |
444.6 |
685 |
1390 |
|
主要化合价 |
-2 |
-2,+4,+6 |
-2,+4,+6 |
|
|
原子半径 |
逐渐增大 |
|||
|
单质与H2反应情况 |
点燃时易化合 |
加热化合 |
加热难化合 |
不能直接化合 |
请根据表回答下列问题:
(1) 硒的熔点范围可能是___________ (2) 碲的化合价可能有_________________
(3) 硫、硒,碲的氢化物水溶液的酸性由强至弱顺序是_________________(填化学式),
其中H2S的电子式为
(4) 氢硒酸有较强的_________(填“氧化性”或“还原性”),因此放在空气中长期保存易变质,其可能发生的化学方程式为__________________________________。
(5) 工业上Al2Te3可用来制备H2Te,完成下列化学方程式:
( )A12Te3+( ) 一( )A1(OH)3↓+( )H2Te↑
(6)已知在常温下,H2和S反应生成17g H2S气体放出56.1KJ的热量,
 试写出硫化氢气体分解的热化学方程式:
试写出硫化氢气体分解的热化学方程式:
_______________________ __________
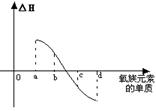
(7) 右图为氧族元素单质与H2反应过程中的能量变化示意图,
其中a、b、c、d分别表示氧族中某一元素的单质,△H为相同
物质的量的单质与H2反应的反应热。则:b代表
________________,d代表_____________(均写单质名称)。
28.⑴ 在右面元素周期表中画出
金属元素与非金属元素的分界线。
⑵ 有人认为形成化合物最多的
元素不是IVA族的碳元素,而是
另一种短周期元素,请你根据学
过的化学知识判断这一元素是
__________。
⑶ 现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。
①写出甲的元素符号 其在元素周期表中对应的位置
② 甲、乙两元素相比较,金属性较强的是_______(填名称), 可以验证该结论的实验是__________。(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中
(b)将这两种元素的单质粉末分别和同浓度的盐酸反应
(c)将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
(d)比较这两种元素的气态氢化物的稳定性
27. 实验室欲配制80mL 1.4mol/L的NaNO3溶液,试回答:

(1) 用不到的仪器是: ;
A.烧杯 B.500mL容量瓶 C.量筒 D.胶头滴管 E.玻璃棒 F.100mL容量瓶
(2) 配制时应称取NaNO3 g;
(3)下列操作的顺序是(用字母表示) ;
A.放置至室温 B.称量 C.洗涤 D.定容 E.溶解 F.摇匀 G.转移
(4)在配制一定物质的量浓度溶液的实验中,下列操作对所配得溶液无影响的是(写序号) ;会使所配溶液的浓度偏大的是 ;会使所配溶液的浓度偏小的是 。
A.在烧杯中溶解溶质,搅拌时不慎溅出少量溶液;
B.未将洗涤烧杯内壁的溶液转移入容量瓶;
C.容量瓶中所配的溶液液面未到刻度线便停止加水;
D.将配得的溶液从容量瓶转移到干燥、洁净的试剂瓶中时,有少量溅出;
E.将烧杯中溶液转移到容量瓶之前,容量瓶中有少量蒸馏水;
F.将容量瓶中液面将达到刻度线时,俯视刻度线和液面。
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
26.某一反应体系中存在以下五种物质:Na3AsO3、H2O、I2、Na3AsO4、HI。
(1)用这五种物质组成一个合理的未配平的方程式:
(2)若水是产物,请配平该反应的方程式,并标出电子转移方向与数目: 。
(3)pH为5-9时,体系中的氧化反应为HI→I2;当pH < 4时,反应方向改变,此时体系中的氧化反应为:_______ → ________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com